Chemie (vom ägyptischen ch'mi = schwarz) ist eine Naturwissenschaft. Sie ist die Lehre von den Stoffen, ihrem Aufbau, ihren Eigenschaften und ihren Reaktionen.
1.1 Körper und Stoff
Körper: Die Gegenstände unserer Umwelt heißen Körper. Jeder Körper hat eine bestimmte Masse und nimmt einen Raum ein.
Stoff: nennt man das Material, aus dem die Körper bestehen.
1.2 Eigenschaften der Stoffe
Stoffeigenschaften lassen sich auf drei Arten erfassen:
a) Mit den Sinnen wahrnehmbar:
Aussehen (Farbe, Oberflächenglanz, Kristallform) · Geruch · Geschmack
b) Mit Geräten messbar:
Elektrische Leitfähigkeit · Schmelztemperatur · Siedetemperatur · Härte
c) Weitere Eigenschaften:
Löslichkeit · Magnetismus · Wärmeleitfähigkeit · Brennbarkeit · Dichte
1.2.1 Dichte und Dichtebestimmung
Die Dichte (Formelzeichen: ρ, griechisch: Rho) ist eine physikalische Eigenschaft eines Materials. Sie ist eine Stoffkonstante — unabhängig vom Ort, aber abhängig von Temperatur und Druck.

a) Dichtebestimmung von Flüssigkeiten
[Schülerexperiment: Dichtebestimmung von Alkohol und Wasser]
Schritt 1: Volumen mit dem Messzylinder ermitteln.
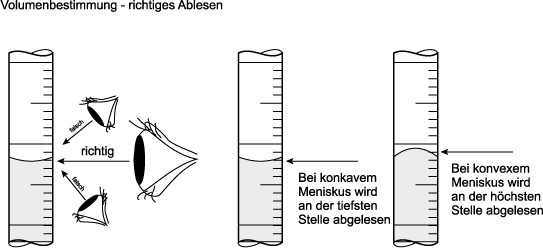
Schritt 2: Masse durch Wägung bestimmen.
Schritt 3: Dichte berechnen (ρ = m ÷ V)
Ergebnis: Dichte von Wasser ≈ 1,00 g/cm³ · Dichte von Ethanol ≈ 0,79 g/cm³
b) Dichtebestimmung von Feststoffen
[Schülerexperiment: Dichtebestimmung von Kupfer und Eisen]
Schritt 1: Masse der Stoffportion bestimmen (Waage)
Schritt 2: Volumen bestimmen (Wasserverdrängung im Messzylinder)
Schritt 3: Dichte berechnen
Ergebnis: Dichte von Kupfer = 8,93 g/cm³ · Dichte von Eisen = 7,87 g/cm³
c) Dichtebestimmung von Gasen
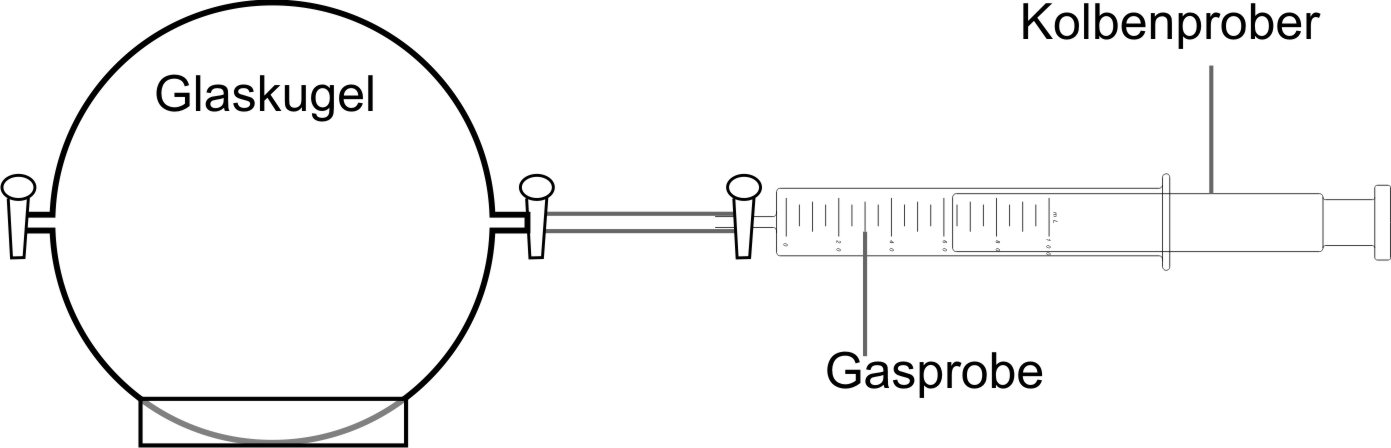
Eine Gaswägekugel wird mit der Wasserstrahlpumpe luftleer gepumpt und gewogen. Mit einem Kolbenprober wird eine Gasportion bekannten Volumens (100 ml) eingefüllt. Die Kugel wird erneut gewogen — aus Massenzunahme und Volumen ergibt sich die Dichte.
Ergebnis: Dichte von Luft bei 20 °C und 1013 hPa ≈ 0,00129 g/cm³
Übungsaufgaben zur Dichte
Klicke auf eine Karte um die Lösung zu sehen — klicke erneut um zurückzublättern.
Chemie Klasse 8 · Stoffe und ihre Eigenschaften · Dichte und Dichtebestimmung · Gymnasium Baden-Württemberg · Bildungsplan 2016
- Details
- Geschrieben von: Wolfram Hölzel
1.3 Atommodelle:
1.3.1 Demokrit (400 vor Chr.; Athen):
- Atome sind die kleinsten, unteilbare Einheiten
1.3.2 Kugelteilchenmodell (KTM), Kugelmodell (John Dalton, 1803)
Jeder Stoff ist aus kleinsten Teilchen aufgebaut, die nicht sichtbar gemacht werden können.
Man benutzt deshalb eine Modellvorstellung: das Kugelteilchenmodell. Für die kleinsten Teilchen gilt:
a) sie sind kugelförmig und unteilbar;
b) jeder Reinstoff besitzt für ihn charakteristische Teilchen mit bestimmter Masse und Größe;
c) zwischen den Teilchen tritt leerer Raum auf;
d) zwischen den Teilchen wirken Anziehungskräfte;
e) die Teilchen sind ständig in Bewegung;
f) mit steigender Temperatur bewegen sich die Teilchen kräftiger.
Experiment:
Beobachtung:

Bei der Mischung von Alkohol und Wasser ist das Gesamtvolumen der Mischung kleiner als die Summe der beiden Teilvolumina.
Hypothese:
Die kleineren kugelförmige Teilchen setzen sich in die Lücken der größeren kugelförmigen Teilchen (Bsp. Senf + Erbsen)
Beachte:
- Das Kugelteilchenmodell soll den Aufbau der Stoffe veranschaulichen.
- Das KTM ist keine Darstellung oder Kopie der Wirklichkeit.
- Das KTM erfasst nur wenige Aspekte der Wirklichkeit.
- Jedes Modell in den Naturwissenschaften hat seine Grenzen; es ist mehr oder weniger brauchbar, je nachdem, wie viele Beobachtungen es vereinigt und Voraussagen es zulässt.
- Details
- Geschrieben von: Wolfram Hölzel
1.3.3 Kugelteilchenmodell und Aggregatzustände
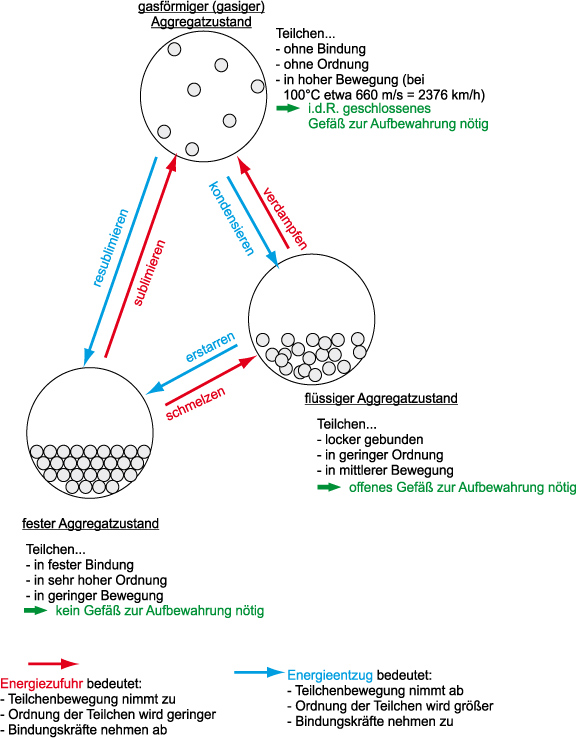
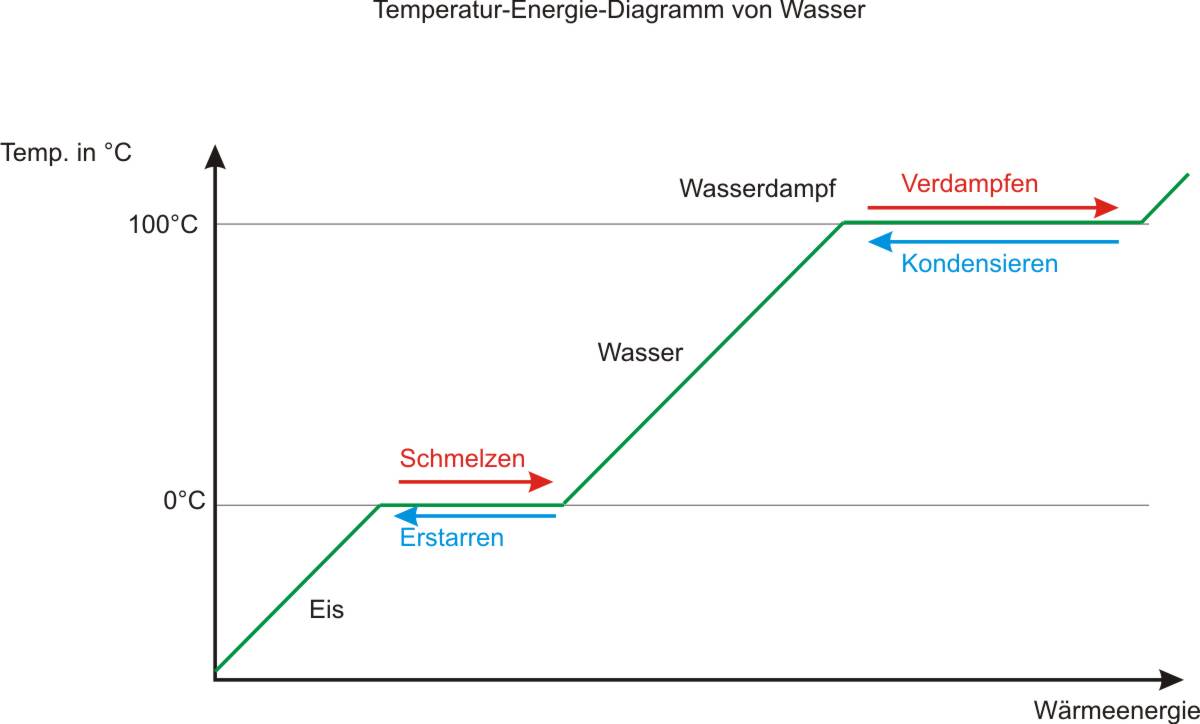
Sublimieren: Flasche mit Jod:
Über dem festen Jod befindet sich in der Flasche violetter Joddampf, aus dem sich langsam an den Wänden Jodkristalle bilden.
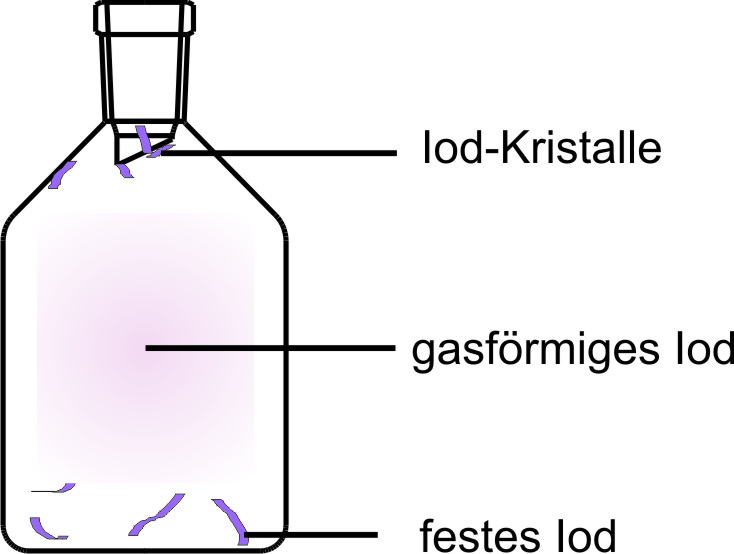
Übergänge zwischen den Aggregatzuständen verlaufen manchmal erst nach einem gewissen „Anstoßen“.
- „Siedeverzug“: beim Sieden (oft fast explosionsartig);
- „Unterkühlung“ beim Auskristallisieren aus einer Schmelze;
- „Übersättigung“ beim Auskristallisieren aus einer heißen gesättigten Lösung.
border=„Siedeverzug“: beim Sieden (oft fast explosionsartig);
- Details
- Geschrieben von: Wolfram Hölzel
1.4 Brownsche Molekularbewegung
Versuch 1:
Durchführung:
1. Schritt: Vollmilch und Wasser wird im Verhältnis 1:1 vermischt.
2. Schritt: 1 Tropfen wird auf dem Objektträger gegeben und mit einem Deckgläschen bedeckt.
3. Milch-Wasser-Tropfen wird mikroskopiert.
Beobachtung: Die Fetttropfen bewegen sich (zittern).
Ergebnis:
Brownsche Molekularbewegung: Bewegung, die die Teilchen in allen Aggregatzuständen (fest, flüssig, gasförmigen) ausüben.
1.5 Diffusion
vgl. Versuche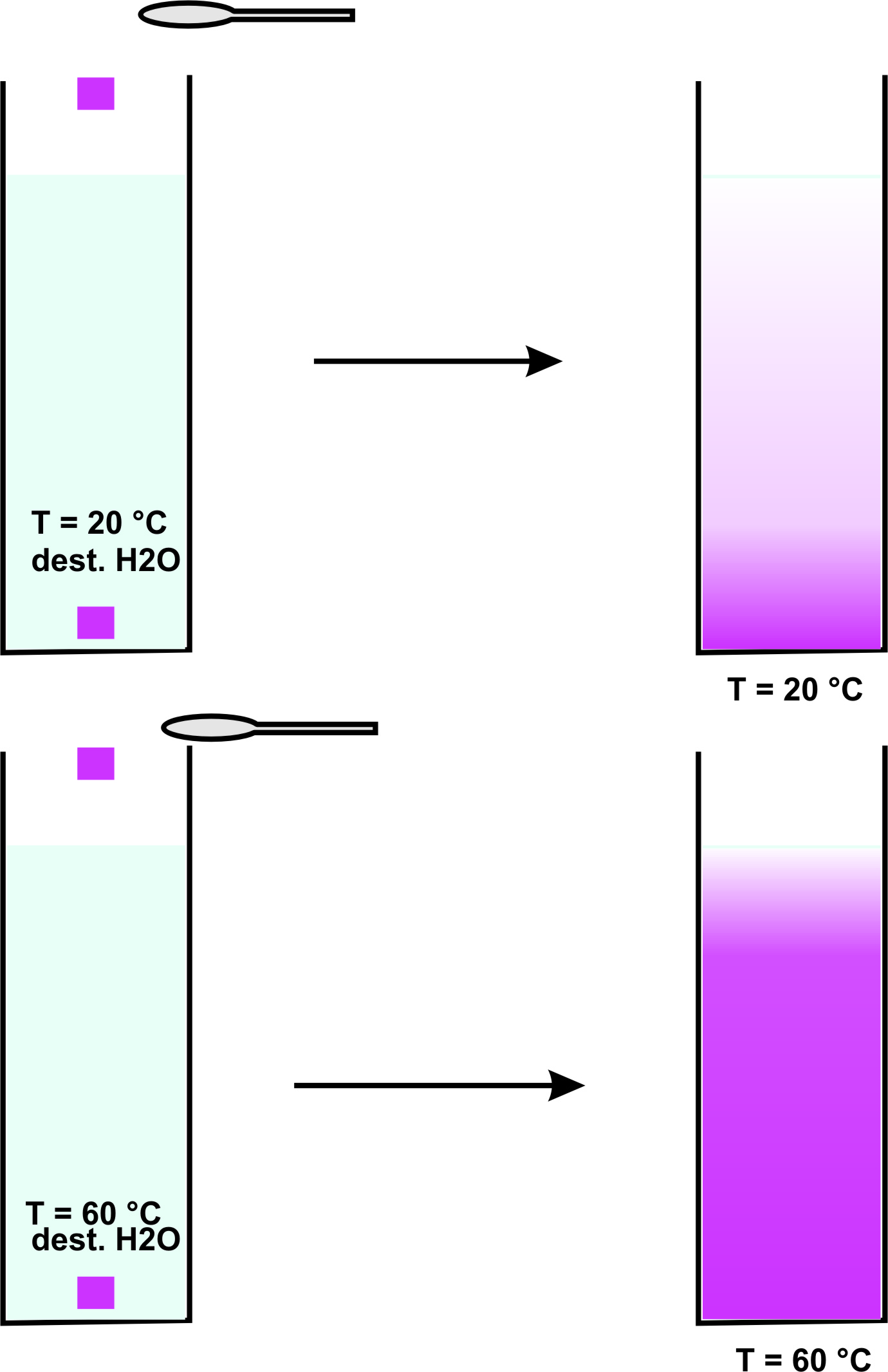
Beobachtung:
Die Kristalle lösen sich unter Schlierenbildung auf. Mit der Zeit verteilen sich die Ionen (= geladene Teilchen) gleichmäßig.
Dabei läuft die Verteilung im warmen Wasser schneller ab als im kalten.
Die Teilchengeschwindigkeit ist umso höher, je höher die Temperatur ist.
Die Diffusion erfolgt umso schneller, je
- höher die Temperatur
- kleiner die Teilchen
- kürzer die Strecke
Diffusion ist in einem Gas schneller als in einer Flüssigkeit.
1.6 Löslichkeit
Flüssigkeiten (z.B. Wasser, Brennspiritus), die Stoffe (z.B. Zucker, Kaliumnitrat) lösen, heißen Lösungsmittel. Gelöst werden können Feststoffe, Flüssigkeiten und Gase. Ein Lösungsmittel kann nicht jeden Stoff lösen. Nimmt die Lösung keinen weiteren Stoff mehr auf, so ist die Lösung gesättigt.
• Leicht löslich: Lösungsmittel: 100 g Wasser, bei 20 °C: es lösen sich 204 g Zucker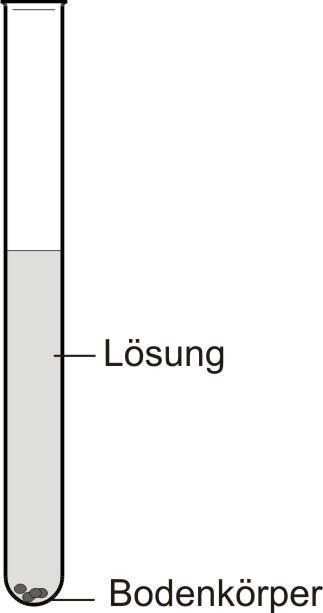
• Schwer löslich: Lösungsmittel: 100 g Wasser, bei 20 °C: es lösen sich 0,2 g Gips
• Bodenkörper: fester Stoff, der sich nicht weiter löst.
Bei vielen festen und flüssigen Stoffen nimmt die Löslichkeit mit steigender Temperatur zu.
Bei Gasen nimmt die Löslichkeit mit steigender Temperatur ab.
KTM-Erklärung für das Lösen von Zucker in Wasser:
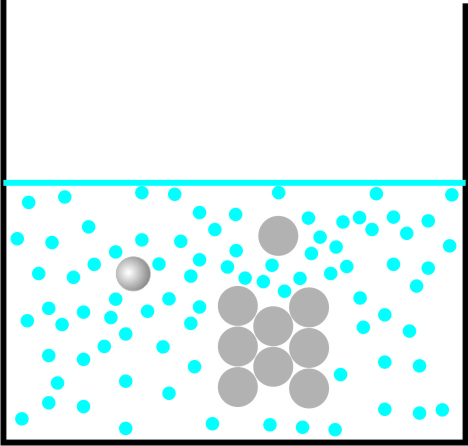
Die sich bewegende Wasserteilchen schieben sich zwischen die Zucker-Teilchen und lösen sie aus dem Kristall.
1.6.1 Kristalle
- Kristalle sind gekennzeichnet durch geometrisch regelmäßige Anordnung ihrer Außenflächen und Kanten. Kristalle sind immer durch Ebenen begrenzt.
Nichtkristalline (amorphe) Stoffe haben dagegen gekrümmte Flächen als Begrenzung (Bsp. Glas, Kunststoff) - Entstehung von Kristallen:
- aus heißgesättigten Lösungen durch Abkühlen (z.B. Kupfersulfat)
- aus kaltgesättigten Lösungen durch Verdunsten des Lösungsmittel [möglichst langsam] (z.B. Zucker)
- aus Dämpfen durch Erstarren
- aus Schmelzen durch Erstarren
- Details
- Geschrieben von: Wolfram Hölzel
Hier findet sich das erste Kapitel der Chemie der 8. Klasse. Folgende Nummerierungen können von der Heftnummerierung abweichen, weil ich bei Zeitmangel mal ein unwichtigeres Thema weggelassen oder ein aktuelles Thema dazu genommen habe. Für mögliche Konfusionen bitte ich jetzt schon um Entschuldigung.
Das erste Kapitel der Chemie Klasse 8 am Gymnasium Baden-Württemberg behandelt grundlegende Begriffe der Chemie: Was sind Stoffe, welche Eigenschaften haben sie, und wie lassen sie sich beschreiben und unterscheiden? Die Inhalte orientieren sich am Bildungsplan 2016 BW.
Chemie Klasse 8 · Kapitel 1: Stoffe und ihre Eigenschaften · Gymnasium Baden-Württemberg · Bildungsplan 2016 · Mitschriften von Wolfram Hölzel
- Details
- Geschrieben von: Wolfram Hölzel
