4.1.3 Ringstruktur der Monosaccharide
Widersprüche:
- Schiffsche Reagenz (typ. Nachweis für Aldehyde) zeigt keine Farbreaktion.
- Drehwinkel in wässriger Lsg. 52,7° statt 112,2°.
- Tollens (1883) schloss daraus, dass Glucose nicht in der offenen Aldehydform vorliegt.
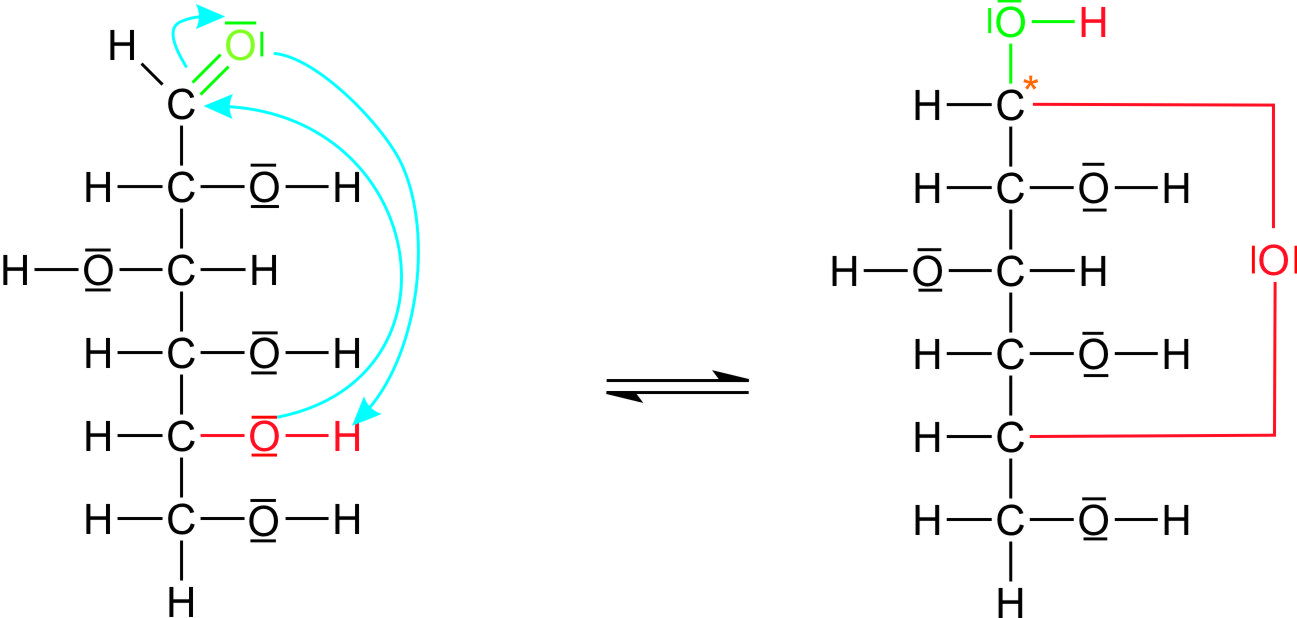
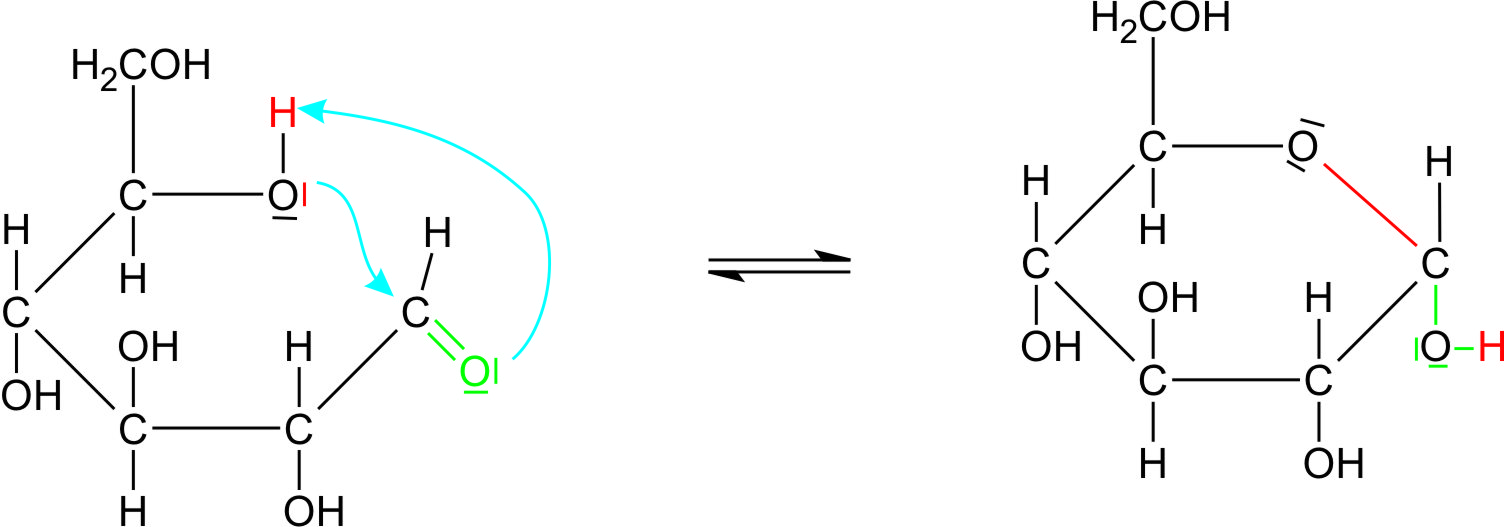
- Die Ursache hierfür ist in der intramolekularen Verknüpfung der Carbonylgruppe mit einer Hydroxylgruppe des gleichen Zuckermoleküls zu suchen. Es kommt also zu einer innermolekularen Halbacetalbildung.
Haworth-Schreibweise
- zyklisches Glucose Molekül wird als liegendes Sechseck [Pyranosen] oder Fünfeck [Furanosen] gezeichnet;
- Ringsauerstoffatom findet sich in der rechten hinteren Ecke [Pyranosen] bzw. im hinteren Eck [Furanosen];
- Substituenten, die in der FISCHERprojektion nach links weisen, stehen in der HAWORTH-Projektion oben ["Kommunistenregel"]
Erklärung der negativen Reaktion der Glucose mit der Schiffschen Reagenz: Es liegt ein Gleichgewicht zwischen der offenen Kette und dem Ring vor, wobei der Anteil der offenen Kette, bei der wirklich ein Aldehyd vorliegt verschwindend gering ist (< 1%):
Aldehydform (offenkettig) ⇌ Halbacetalform (Ring)
- Fuchsinschweflige Säure (Schiffsches Reagenz) bildet mit dem Aldehyd eine reversible (umkehrbare) Reaktion, daher findet kein Entzug des Aldehyds statt. Das heißt, es gibt keine GG-Verschiebung und damit keinen wirklichen Aldehydnachweis (der Anteil an offener aldehydhaltigen Glucose ist zu gering).
- Bei der Fehling-Probe und der Tollens-Probe (Silberspiegel) findet eine GG-Verschiebung statt! Die offene Form wird laufend entzogen, neue Ringe gehen auf und es findet langsam der Aldehydnachweis statt.
Durch Ringbildung entstehen 2 Strukturisomere der D-(+)-Glucose (keine Spiegelbildisomere).
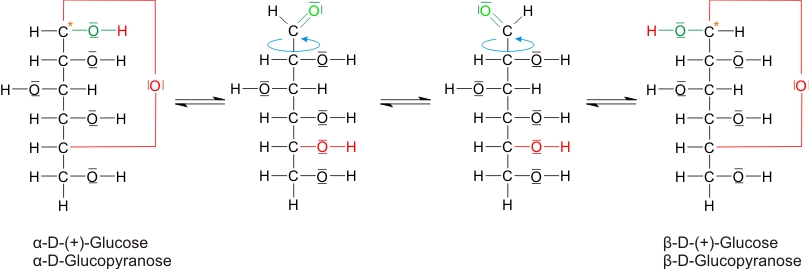
In wässriger Lösung liegen vor:
36% 0,26% 64%
Drehwinkel: 112,2° 18,7°
Es entsteht ein neues asymmetrisches C-Atom (= anomeres Kohlenstoffatom) und damit 2 Diasteromere. Anomere = Isomere, die sich nur durch die Stellung der Hydroxylgruppen am anomeren Kohlenstoffatom unterscheiden.
α-Form: OH-Gruppe am neuen asymmetrischen C-Atom liegt auf derselben Seite wie die am untersten asymmetrischen C-Atom.
Muta1rotation: Drehwinkel einer Lösung einer optisch aktiven Substanz ändert sich vom Zeitpunkt des Ansetzens der Lösung kontinuierlich bis zum Erreichen eines festen Wertes. Grund dafür ist, dass man z.B. α-Glucose in eine wässrige Lösung gibt. Sobald sich das Molekül in Wasser löst, öffnen sich einige wenige Moleküle. Bei der erneuten Ringbildung, bildet sich auch β-Glucose. Erst wenn sich der Anteil wie oben angegeben einstellt, ändert sich der Drehwinkel nicht mehr.
Glucose α-Form ⇌ offene Form ⇌ β-Form
Bei Glucose ist der Endwert: 0,36 * 112,2° + 0,64 * 18,7° = 52,36°
Haworth-Schreibweise
Achtet auf die Durchnummerierung der C-Atome. Am C1 war ursprünglich die Aldehydgruppe.

α-D-Glucose β-D-Glucose
Nachweis von Glucose: GOD-Test (Glucose-Oxidase-Stäbchen); Achtung beim schriftlichen Abitur: Fehling oder Tollens ist kein Nachweis für Glucose, sondern nur für Aldehydgruppen!
- Glucose-Oxidase = Enzym: Oxidiert Glucose am C1-Atom zu Gluconsäure und Wasserstoffperoxid (H2O2).
- Durch das Enzym Peroxidase (z.B. aus Meerettich) wird das Wasserstoffperoxid zu Wasser reduziert.
- je mehr Glucose, umso intensiver die Farbe.
Im Handel als Teststreifen für Diabeteserkrankung.
-----
