Was du auf dieser Seite lernst
Ein chemisches Gleichgewicht ist nicht unveränderlich: Konzentration, Temperatur und Druck können es verschieben. Du lernst an konkreten Beispielen – dem Eisenrhodanid-Gleichgewicht und dem Chlorethan-Versuch – wie und warum sich die Gleichgewichtslage ändert.
Grundlagen aus diesem Kapitel
Diese Seite baut auf den Grundlagen des chemischen Gleichgewichts auf: → Merkmale eines chemischen Gleichgewichts · → Kollisionsmodell · → Benzoesäure-Gleichgewicht
2.10 Verschiebung des Gleichgewichts
Die Lage des Gleichgewichts ergibt sich aus dem Zusammenwirken von Hinreaktion und Rückreaktion. Das Gleichgewicht verschiebt sich, wenn beide Reaktionen verschieden stark geändert werden.
Das ist häufig der Fall bei einer Änderung von
- Konzentration (Konzentration = Stoffmenge / Volumen)
- Temperatur
- Druck
2.10.1 Änderung der Konzentration und Temperatur
α) Einmaliger Zusatz von Stoff D
Es erfolgen mehr Rückreaktionen (Wichtig, das über das Kollisionsmodell zu verstehen: durch mehr
Teilchen wird häufiger ein Zusammenstoß zwischen C und D erfolgen); dadurch stellt sich ein neues
Gleichgewicht ein. Man sagt: „Das GG wird nach links verschoben."
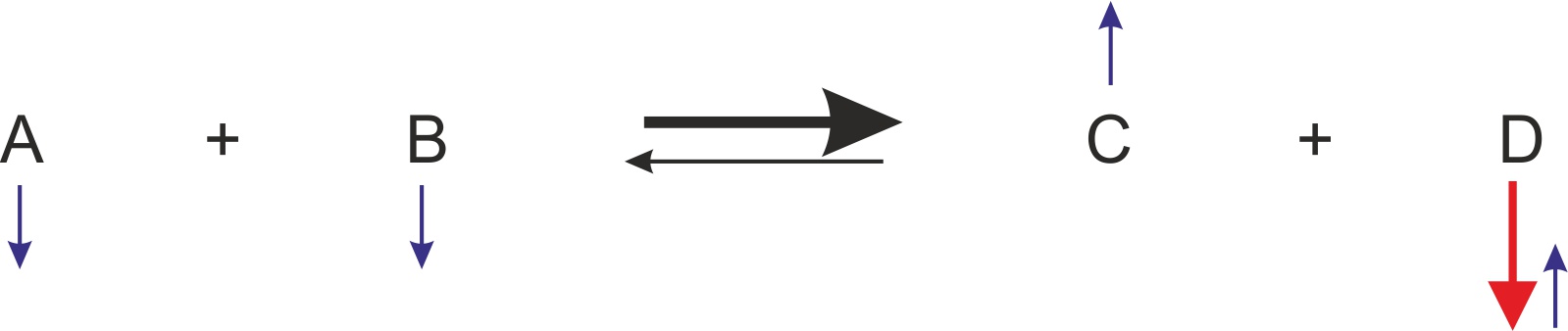
Roter Pfeil: Zugabe von Stoff D → Stoff D kollidiert häufiger mit C und reagiert. Dadurch werden es etwas weniger Stoffe C und D (blaue Pfeile auf der Produktseite); gleichzeitig entstehen etwas mehr Stoffe A und B. Bitte immer daran denken: Bei einem Gleichgewicht gibt es immer alle Stoffe – hier also A, B, C und D gleichzeitig! Man kann sich das schnell veranschaulichen, wenn man bei einer Reaktionsgleichung die Pfeile einzeichnet.
↑ Zum Vergrößern klicken
✕
β) Einmalige Wegnahme von Stoff D
Jetzt seid ihr dran: Wie ändert sich das Gleichgewicht, wenn man einmalig den Stoff D wegnimmt? Macht eine analoge Reaktionsgleichung mit Pfeilen wie oben.
Lösung: Wegnahme von Stoff D
Es erfolgen mehr Hinreaktionen; dadurch stellt sich ein neues Gleichgewicht ein. Man sagt: „Das GG wird nach rechts verschoben."
↑ Zum Vergrößern klicken
γ) Dauernde Wegnahme von Stoff D (z. B. als Gas)
Wie ändert sich das Gleichgewicht bei dauerhafter Wegnahme, wenn der entstehende Stoff D permanent aus dem System verdampft?
Lösung: Dauernde Wegnahme – offenes System
In einem offenen System kann sich kein Gleichgewicht einstellen; die Reaktion läuft vollständig ab.
↑ Zum Vergrößern klicken

Eisenrhodanid-Gleichgewicht
Vergleich dazu Arbeitsblatt zum Experiment.
Vereinfachte Reaktionsgleichung:
↑ Zum Vergrößern klicken
✕
a) Das 1. Reagenzglas bleibt unverändert und dient zum Vergleich!
b) Ein Spatellöffel NH4Cl (Ammoniumchlorid) wird in Reagenzglas 2
gegeben.
Beobachtung: Die Lösung wird heller.
Wie kann man das mithilfe der Verschiebung des Gleichgewichts deuten?
Lösung: Zugabe von NH₄Cl
Deutung: Das Gleichgewicht wird nach links verschoben. Die Konzentration des Produkts NH4Cl wird erhöht → mehr Rückreaktionen → weniger Fe(SCN)3 → Lösung entfärbt sich (wird heller).
c) Eine Spatelspitze FeCl3 (Eisenchlorid) wird in Reagenzglas 3 gegeben.
Nenne die mögliche Beobachtung und Deutung:
Lösung: Zugabe von FeCl₃
Beobachtung: Die Lösung wird dunkelrot.
Deutung: Das Gleichgewicht wird nach rechts verschoben. Die Konzentration
des Edukts Fe3+ wird erhöht → mehr Hinreaktionen → mehr Fe(SCN)3
→ Lösung wird dunkler.
d) Ein Spatellöffel NH4SCN (Ammoniumrhodanid = Ammoniumthiocyanat) wird in Reagenzglas 4 gegeben.
Lösung: Zugabe von NH₄SCN
Beobachtung: Die Lösung wird dunkelrot.
Deutung: Das Gleichgewicht wird nach rechts verschoben. Die Konzentration
des Edukts SCN− wird erhöht → mehr Hinreaktionen → mehr Fe(SCN)3.
Ergebnis (Konzentration): Konzentrationserhöhung eines Reaktionspartners begünstigt die Reaktion, die diesen Stoff verbraucht.
e) Reagenzglas 5 wird in heißes Wasser gestellt.
Beobachtung: Die Lösung wird heller.
Lösung: Temperaturerhöhung (heißes Wasser)
Deutung: Das Gleichgewicht wird nach links verschoben. Temperaturerhöhung begünstigt die endotherme Reaktion (die Rückreaktion). Da ΔH < 0 für die Hinreaktion, ist die Rückreaktion endotherm → weniger Fe(SCN)3 → Lösung wird heller.
f) Reagenzglas 6 wird in Eiswasser gestellt.
Überlegt, was jetzt die Beobachtung sein könnte:
Lösung: Temperaturerniedrigung (Eiswasser)
Beobachtung: Die Lösung wird dunkler.
Deutung: Das Gleichgewicht wird nach rechts verschoben.
Temperaturerniedrigung begünstigt die exotherme Reaktion (die Hinreaktion) → mehr
Fe(SCN)3 → Lösung wird dunkler.
Ergebnis (Temperatur):
• Temperaturerhöhung begünstigt die endotherme Reaktion.
• Temperaturerniedrigung begünstigt die exotherme Reaktion.
b) Weiteres Beispiel
H2O (l) ⇌ H2O (g) ΔH = +41 kJ
flüssig gasförmig
Temperaturerhöhung → mehr Wasser verdampft (endotherme Reaktion wird begünstigt).
2.10.2 Änderung des Drucks
a) Chlorethandampf – Chlorethanflüssigkeit (Kältespray; genau: Monochlorethan)
C2H5Cl (g) ⇌ C2H5Cl (l)
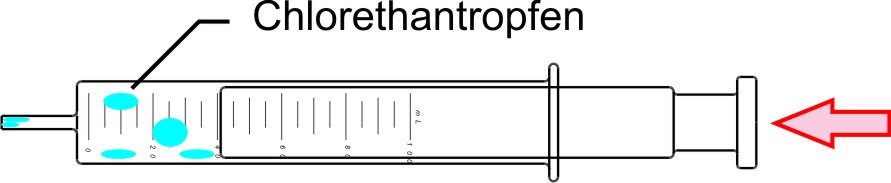
α) Bei Druckerhöhung bilden sich im Kolbenprober Chlorethantröpfchen:
↑ Zum Vergrößern klicken
✕
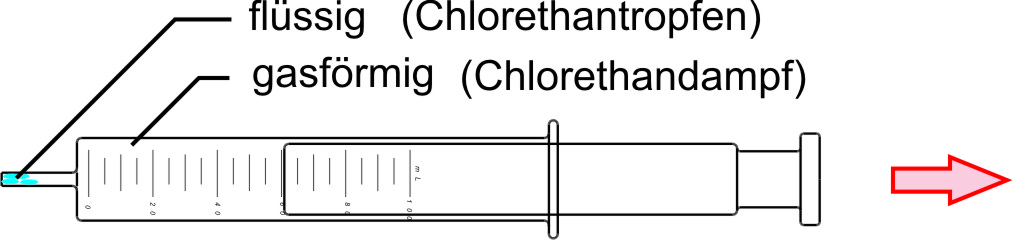
β) Bei Druckerniedrigung verschwinden die Chlorethantröpfchen wieder:
↑ Zum Vergrößern klicken
✕
Ergebnis (Druck): Druckerhöhung begünstigt die Reaktion mit Volumenabnahme.
b) Weiteres Beispiel
H2O (s) ⇌ H2O (l)
fest (solid) flüssig (liquid)
Druckerhöhung verschiebt das Gleichgewicht nach rechts: Wasser wird flüssig.
Grund: Flüssiges Wasser hat eine größere Dichte (kleineres Volumen) als Eis – deshalb schwimmt
Eis auf Wasser.
FeCl3 + 3 NH4SCN ⇌ Fe(SCN)3 + 3 NH4Cl ΔH < 0
Auf einen Blick – die wichtigsten Aussagen
KONZENTRATION
Konzentrationserhöhung eines Stoffs begünstigt die Reaktion, die diesen Stoff verbraucht.
TEMPERATUR
Temperaturerhöhung begünstigt die endotherme, Kühlung die exotherme Reaktionsrichtung.
DRUCK
Druckerhöhung begünstigt die Reaktionsrichtung mit Volumenabnahme (weniger Gasteilchen).
OFFENES SYSTEM
Wird ein Produkt dauerhaft entfernt, kann sich kein Gleichgewicht einstellen – die Reaktion läuft vollständig ab.
Häufige Fragen – Verschiebung des Gleichgewichts
Was bedeutet es, dass ein Gleichgewicht „verschoben" wird?
Ein chemisches Gleichgewicht liegt vor, wenn Hin- und Rückreaktion gleich schnell ablaufen. Greift man von außen ein – z. B. durch Zugabe eines Stoffs – laufen beide Reaktionen vorübergehend unterschiedlich schnell. Bis sich ein neues Gleichgewicht einstellt, überwiegt eine der beiden Richtungen. Man sagt: Das Gleichgewicht wird nach links oder rechts verschoben. Mehr zu den Grundlagen: → Merkmale des chemischen Gleichgewichts.
Wie wirkt die Zugabe eines Reaktionspartners auf das Gleichgewicht?
Wird die Konzentration eines Stoffs erhöht, begünstigt das die Reaktionsrichtung, die diesen Stoff verbraucht. Erklärt wird das über das Kollisionsmodell: Mehr Teilchen bedeutet häufigere Zusammenstöße in der entsprechenden Reaktionsrichtung. Beispiel: Gibt man zum Eisenrhodanid-Gleichgewicht FeCl3 zu, steigt die Fe3+-Konzentration → das GG verschiebt sich nach rechts → Lösung wird dunkler.
Warum läuft eine Reaktion im offenen System vollständig ab?
Im offenen System werden Produkte permanent aus dem Reaktionsgemisch entfernt (z. B. durch Verdampfen). Dadurch kann die Rückreaktion nicht stattfinden – denn sie benötigt die Produkte als Edukte. Das Gleichgewicht wird so weit nach rechts verschoben, bis alle Edukte verbraucht sind. Dieses Prinzip ist z. B. in der Ammoniaksynthese technisch genutzt.
Warum verschiebt Erhitzen des Eisenrhodanid-Gleichgewichts die Lage nach links?
Die Hinreaktion des Eisenrhodanid-Gleichgewichts ist exotherm (ΔH < 0). Die Rückreaktion ist damit endotherm. Temperaturerhöhung begünstigt die endotherme Reaktionsrichtung – also die Rückreaktion. Infolgedessen zerfällt mehr Fe(SCN)3, und die rote Farbe verblasst. Umgekehrt: Kühlung (Eiswasser) begünstigt die exotherme Hinreaktion → Lösung wird dunkler.
Wie beeinflusst Druck ein Gleichgewicht zwischen Gasen?
Druckerhöhung begünstigt die Seite mit dem kleineren Volumen (weniger Gasteilchen). Beim Chlorethan-Gleichgewicht C2H5Cl (g) ⇌ C2H5Cl (l) bedeutet Druckerhöhung, dass mehr Dampf kondensiert (Flüssigkeit nimmt weniger Volumen ein). Bei Gasen mit unterschiedlicher Molzahl auf beiden Seiten (z. B. der Ammoniaksynthese: N2 + 3 H2 ⇌ 2 NH3) begünstigt Druck die Seite mit weniger Gasteilchen (hier die Produktseite mit 2 mol statt 4 mol).
Lernkarten – Verschiebung des Gleichgewichts
Klicke auf eine Karte, um die Antwort zu sehen.
Was passiert beim einmaligen Zusatz von Stoff D zum Gleichgewicht A + B ⇌ C + D?
Das GG verschiebt sich nach links: Mehr Kollisionen zwischen C und D führen zu mehr Rückreaktionen. A und B nehmen zu, C und D (abzüglich Zugabe) nehmen ab.
Was passiert, wenn ein Produkt im offenen System dauerhaft entfernt wird?
Die Rückreaktion kann nicht mehr stattfinden. Das GG wird so weit nach rechts verschoben, bis alle Edukte verbraucht sind – die Reaktion läuft vollständig ab.
Das Eisenrhodanid-GG (ΔH < 0). Was beobachtet man beim Erwärmen – und warum?
Lösung wird heller: Temperaturerhöhung begünstigt die endotherme Rückreaktion → GG verschiebt sich nach links → weniger Fe(SCN)3.
Was beobachtet man beim Druckerhöhen im Chlorethan-Kolbenprober – und warum?
Es entstehen Chlorethantröpfchen: Druckerhöhung begünstigt die Reaktionsrichtung mit Volumenabnahme → Gas kondensiert zu Flüssigkeit.
Zusammenfassung: Nenne alle Maßnahmen, die das exotherme Eisenrhodanid-GG nach rechts verschieben, und erkläre jeweils warum.
① Fe³⁺ oder SCN⁻ zugeben (Edukt-Konzentration ↑) · ② NH₄Cl entfernen (Produkt-Konzentration ↓) · ③ Abkühlen (exotherme Hinreaktion wird begünstigt) – in allen Fällen: mehr Fe(SCN)3, Lösung wird dunkler.
Weiter im Kapitel Gleichgewichtsreaktionen
← 2.9 Benzoesäure-Gleichgewicht → 2.11 Prinzip von Le Chatelier
→ 2.12 Massenwirkungsgesetz → 2.15 Ammoniaksynthese
🔁 Grundlagen: Merkmale des chemischen GG · Kollisionsmodell
