1.7 Stoffklassen
Kennmerkmale der Stoffe in den drei Stoffklassen:
| Stoffklasse | Beispiele | Eigenschaften, Kennmerkmale |
| metallische Stoffklasse | Kupfer, Eisen, Aluminium, Blei, Silber, Gold, Zink, Quecksilber, ... | metallischer Glanz; verformbar durch Biegen, Hämmern; leitet den elektrischen Storm im festen und flüssigen Zustand; gute Wärmeleitfähigkeit; bei ZT sind außer Quecksilber alle Metalle fest. |
| salzartige Stoffklasse | Kochsalz; Natriumnitrat; Kupfersulfat; Kaliumpermanganat; ... | leitet den elektrischen Strom im festen Zustand nicht; oft in Wasser löslich; diese Lösung leitet den elektrischen Strom; geschmolzene Salze leiten den Strom; Kristallbildung, spröde. |
| flüchtige Stoffe | Benzin; Wasser; Alkohol; Iod, ... | niedrige Schmelz- und Siedetemperatur; bei Zimmertemperatur meist flüssig oder gasig; keine (bzw. schlechte) elektrische Leitfähigkeit. |
Achtung:
Viele Stoffe lassen sich jedoch keiner dieser drei Stoffklassen zuordnen: Gummi, Diamant, Zucker, Kunststoff (PVC), Cellulose, ... (z.B. Makromoleküle).
Man kann auch die Metalle weiter unterteilen:
- Edelmetalle (z.B. Gold...),
- Halbedelmetalle (z.B. Kupfer...),
- unedle Metalle (z.B. Eisen...).
1.8 Reinstoffe
Reinstoffe besitzen einheitliche spezifische Eigenschaften. Schmelz- und Siedetemperatur (bei Normdruck) sind für jeden Reinstoff eine charakteristische, messbare Stoffeigenschaft.
Reinstoffe sind einheitlich zusammengesetzt, sie sind homogen.
Reinstoffe können durch physikalische Methoden nicht mehr in weitere Stoffe zerlegt werden.
Beispiele für Reinstoffe: Gold, Kupfer, Kochsalz, ....
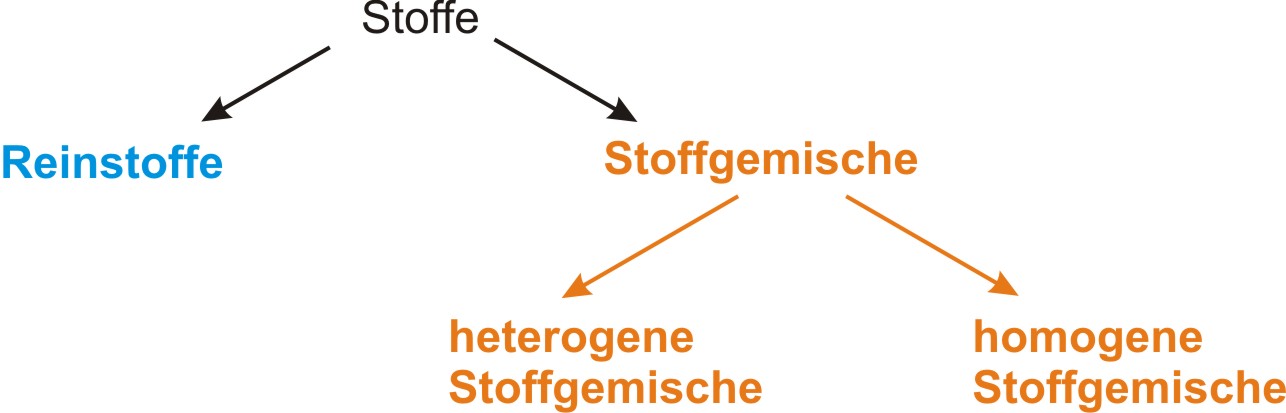
1.9 Gemische (Stoffgemische)
Gemische bestehen aus verschiedenen Reinstoffen.
In den Gemischen fester Stoffe liegen die Bestandteile (Reinstoffe) in beliebigen Mischungsverhältnissen vor; die Eigenschaften der Bestandteile sind unverändert.
1.9.1 Heterogenes Gemisch
In diesem Gemisch sind die verschiedenen Bestandteile zu erkennen, es ist nicht einheitlich aufgebaut.
Jeden Stoffbereich, der sich dabei von einem anderen Bereich durch eine erkennbare Trennfläche abgrenzt, nennen wir zwei Phasen.
Ein heterogenes Gemisch besteht somit aus mindestens zwei Phasen.
|
Aggregatzustand der Bestandteile |
Bezeichnung | Beispiele |
| fest/fest | Gemenge | Eisen-Zucker-Gemisch, Rohsalz, Granit |
| fest/flüssig | Suspension | Lehmwasser |
| fest/gasig | Aerosol | Rauch, staubhaltige Luft |
| flüssig/flüssig | Emulsion |
Öl in Wasser |
| flüssig/gasig | Aerosol | Nebel (Flüssigkeitströpfchen in Gas) Seifenschaum (Gasblasen in Flüssigkeit) |
1.9.2 Homogenes Gemisch
Dieses Gemisch erscheint völlig einheitlich.
Man kann mit dem Mikroskop keine verschiedenen Bestandteile feststellen.
Homogene Gemische bestehen also aus einer Phase.
| Aggregatzustand der Bestandteile | Zustand der Phase | Bezeichnung | Beispiele |
| fest/fest | fest | Amalgam, Legierung | Silber-Zinn-Kupfer-Quecksilbergemisch |
| fest/flüssig | flüssig | Lösung (Feststofflösung) | Zuckerwasser, Kochsalzwasser, Kaliumpermanganatlösung |
| flüssig/flüssig | flüssig | Lösung (Flüssigkeitsgemisch) | Branntwein, Schnaps |
| fest/flüssig/gasig | flüssig gasig | Lösungen (Feststoff-Gas-Lösung) | Mineralwasser |
| gasig | gasig | Gasgemisch | Luft |
1.9.3 Trennverfahren zur Gewinnung von Reinstoffen
Zur Trennung eines Gemisches können die unterschiedlichen Eigenschaften seiner Bestandteile benutzt werden.
1.9.3.1 Heterogene Gemische
| Zustand der Phasen | Beispiel |
zur Trennung genutzte |
Trennverfahren |
| fest/fest | Sand-Salz | Löslichkeit | Extrahieren (Herauslösen) des Salzes, anschließend filtrieren und eindampfen |
| fest/fest | Sand-Sägemehl | Dichte | Sedimentieren (Sand sinkt ab), dekantieren (Abgießen des Sägemehls), filtrieren |
| fest/fest | Schwefel-Eisen | Magnetismus | Magnetscheiden |
| fest/fest | Sand-Schwefel | Schmelzpunkt | Ausschmelzen des Schwefels |
| fest/flüssig | Sand-Wasser | Teilchengröße | Filtrieren |
| flüssig/flüssig | Wasser-Benzin | Dichte | Scheidetrichter (Waser mit höheren Dichte wird zuerst abgelassen). |
1.9.3.2 Homogene Gemische
| Zustand der Phasen | Beispiele | zur Trennung genutzte Eigenschaften | Trennverfahren |
| flüssig | Kochsalzlösung | Siedetemperatur Siedetemperatur |
Destillation Eindampfen |
| flüssig | Alkohol-Wasser (Brennspiritus) | Siedetemperatur | Destillation |
Merke: Die Trennung eines Stoffgemisches durch Verdampfen und anschließendes Kondensieren heißt Destillation. Stoffe mit nahe beieinander liegenden Siedetemperaturen werden nur unvollständig voneinander getrennt.
