Was du auf dieser Seite lernst
Wärme und Temperatur sind nicht dasselbe. Wie viel Wärmeenergie ein Stoff aufnimmt, hängt von seiner spezifischen Wärmekapazität c ab. Die zentrale Formel lautet Qp = c · m · ΔT (massenbezogen) bzw. Qp = Cm · n · ΔT (molbezogen). Diese Größen sind die Grundlage für alle Kalorimetrie-Messungen.
6 spezifische Wärme und spezifische Wärmekapazität
Zunächst einige Beispiele, um das Problem zu verdeutlichen:
a) Zusammenhang zwischen Q und ΔT
Häufig wird die Wärmemenge mit der Temperatur verwechselt. Stoffe (wie beim ersten Beispiel der Kupferklotz) besitzen eine gewisse Wärmemenge. Taucht man den 80 °C warmen und 100 g schweren Kupferklotz in 500 g Wasser, welches 20 °C warm ist und wartet eine geringe Zeit, so haben beide Stoffe anschließend 21,1 °C.
Vorher:
↑ Zum Vergrößern klicken
Nachher:
↑ Zum Vergrößern klicken
- Temperaturausgleich beim Berühren;
- Die Wärmeenergie fließt so lange von der warmen Stoffportion in die kältere, bis beide dieselbe Temperatur haben.
b) Zusammenhang zwischen Q, m und ΔT
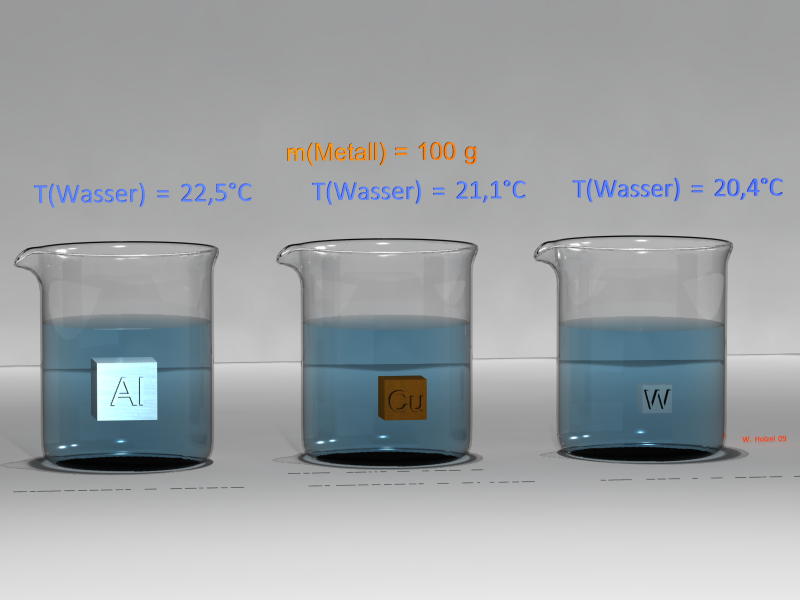
Wie ändert sich eigentlich die Temperatur, wenn man immer die gleiche Masse unterschiedlicher Metalle mit gleicher Temperatur nimmt.
Vorher:
⚠️ Hinweis: In dieser Abbildung ist ein Fehler unterlaufen. Die Temperatur des Wassers muss 20 °C betragen!
↑ Zum Vergrößern klicken
Nachher:
↑ Zum Vergrößern klicken
- Wärme und Temperatur sind unterschiedliche Dinge. Wären sie das Gleiche, wären die Mischungstemperaturen auch gleich.
- Die drei Würfel enthalten unterschiedliche Wärmemengen.
c) Zusammenhang zwischen Q, n (Stoffmenge) und ΔT
Vorher:
↑ Zum Vergrößern klicken
Nachher:
↑ Zum Vergrößern klicken
- Gleiche Stoffmengen transportieren bei Metallen die gleiche Wärmemenge.
d) Zusammenhang zwischen Q, n (Stoffmenge), Teilchenart und ΔT
Vorher:
↑ Zum Vergrößern klicken
Nachher:
↑ Zum Vergrößern klicken
- Die Wärmemenge und die Wärmekapazität Cp [= Wärmespeichervermögen] (auch die molare) sind von den verschiedenen Teilchenarten abhängig.
Spezifische Wärme einer Substanz ist die Wärmemenge, die benötigt wird, um 1 g der Substanz um 1 °C zu erwärmen.
Oder: Die Wärmekapazität gibt an, wie viel thermische Energie ein Körper bezogen auf die Temperaturänderung speichern kann:
Wärme Q ist direkt proportional der Temperaturänderung:
Qp ~ ΔT
Proportionalitätsfaktor für ein System = Wärmekapazität C:
Qp = C · ΔT
Für eine bestimmte Temperaturänderung ist umso mehr Wärme erforderlich, je größer die Masse m des Systems ist
Qp ~ m · ΔT
spezifische Wärmekapazität c (Wärmekapazität bezogen auf die Masse):
c = C / m ⇔ C = c · m
Qp = c · m · ΔT
Molare Wärmekapazität Cm (bezogen auf die Stoffmenge n):
Cm = C / n ⇔ C = Cm · n
Qp = Cm · n · ΔT
Spezifische Wärmemenge c eines Stoffes: entspricht der Wärme Q, die zur Erwärmung von 1 g dieses Stoffes um 1 K bei konstantem Druck auf diesen Stoff übertragen werden muss.
Bsp.: cp(Wasser) = 4,184 J · g⁻¹ · K⁻¹
Frage: Welche Wärmeenergie wird benötigt, um 125 g Wasser von 20 °C auf 25 °C zu erwärmen?
Lösung:
Qp = cp · m · ΔT = 4,184 J · g⁻¹ · K⁻¹ · 125 g · 5 K = 2615 J = 2,615 kJ
⇒ Die Wärmekapazität von Wasser ist wichtig, um andere Reaktionsenthalpien messen zu können.
Auf einen Blick – die wichtigsten Formeln
Massenbezogen
Qp = c · m · ΔT
c = spez. Wärmekapazität [J·g⁻¹·K⁻¹]
Molbezogen
Qp = Cm · n · ΔT
Cm = molare Wärmekapazität [J·mol⁻¹·K⁻¹]
Wasser – Referenzwert
cp(H₂O) = 4,184 J·g⁻¹·K⁻¹
Grundlage aller Kalorimetrie
Wichtig
Wärme Q ≠ Temperatur T –
verschiedene Stoffe, gleiche Masse → verschiedene Q
Häufige Fragen zur Wärmekapazität
Was ist der Unterschied zwischen Wärme Q und Temperatur T?
Die Temperatur gibt an, wie „heiß" ein Körper ist – sie ist eine Zustandsgröße. Die Wärme Q ist die Energie, die bei einem Temperaturunterschied übertragen wird. Dass Wärme ≠ Temperatur ist, zeigt das Kupferklotz-Experiment: 100 g Kupfer bei 80 °C erwärmen 500 g Wasser nur auf 21,1 °C – obwohl der Kupferklotz viel heißer ist, überträgt er wegen seiner geringen Wärmekapazität nur wenig Energie.
Was ist die spezifische Wärmekapazität c?
Die spezifische Wärmekapazität c gibt an, wie viel Wärme (in Joule) nötig ist, um 1 g eines Stoffes um 1 K zu erwärmen. Sie ist eine stoffspezifische Konstante. Wasser hat mit cp = 4,184 J·g⁻¹·K⁻¹ einen ungewöhnlich hohen Wert – das macht es zum idealen Wärmeträger in Kalorimetern und im Alltag (Heizungen, Klimaregulation).
Worin unterscheiden sich C, c und Cm?
C (Wärmekapazität) ist die Wärme, die ein konkretes System (z. B. ein bestimmter Kolben voll Wasser) für ΔT = 1 K benötigt – systemspezifisch, in J/K. c (spezifische Wärmekapazität) bezieht C auf die Masse, also J·g⁻¹·K⁻¹ – damit wird die Größe massenunabhängig und vergleichbar. Cm (molare Wärmekapazität) bezieht C auf die Stoffmenge n, in J·mol⁻¹·K⁻¹ – praktisch für chemische Reaktionsberechnungen.
Warum ist cp(Wasser) so wichtig für die Kalorimetrie?
Im Kalorimeter (→ 7 Kalorimetrie) wird die Temperaturänderung des Wassers gemessen, um Reaktionsenthalpien zu bestimmen. Da cp(H₂O) genau bekannt ist, lässt sich aus Qp = cp · m · ΔT direkt auf die freigesetzte oder aufgenommene Wärmemenge schließen. Wasser ist außerdem das Lösungsmittel vieler Reaktionen.
Wie berechnet man Q bei einer Erwärmung?
Formel: Qp = c · m · ΔT mit ΔT = Tend − Tstart. Beispiel: 125 g Wasser von 20 °C auf 25 °C → ΔT = 5 K → Q = 4,184 · 125 · 5 = 2615 J = 2,615 kJ. Wichtig: Einheiten prüfen – c in J·g⁻¹·K⁻¹, m in g, ΔT in K (oder °C, da Δ identisch).
Lernkarten – Wärmekapazität
Klicke auf eine Karte, um die Antwort zu sehen.
Nenne die Formel für Qp mit spezifischer Wärmekapazität c.
Qp = c · m · ΔT
c in J·g⁻¹·K⁻¹
m in g, ΔT in K
Nenne die Formel für Qp mit molarer Wärmekapazität Cm.
Qp = Cm · n · ΔT
Cm in J·mol⁻¹·K⁻¹
n in mol, ΔT in K
Wie groß ist cp von Wasser – und warum ist dieser Wert bedeutsam?
cp(H₂O) = 4,184 J·g⁻¹·K⁻¹
Sehr hoch → Wasser speichert viel Wärme → Grundlage für Kalorimetrie-Messungen
Warum sind Wärme Q und Temperatur T nicht dasselbe?
Gleiche Masse verschiedener Stoffe bei gleicher Temperatur enthält verschiedene Wärmemengen – weil c stoffabhängig ist.
Hohe T ≠ viel Q!
200 g Wasser werden von 20 °C auf 30 °C erwärmt.
Wie groß ist Qp?
Qp = 4,184 · 200 · 10
= 8368 J = 8,368 kJ
Weiter im Kapitel Energetik
← 5 Reaktionswärme Q → 7 Kalorimetrie → 8 Enthalpie H ↑ 3 Innere Energie U