Was du auf dieser Seite lernst
Wie viel Wärme wird bei einer chemischen Reaktion freigesetzt – und warum hängt das davon ab, ob das Gefäß offen oder geschlossen ist? Bei konstantem Volumen gilt QV = ΔU, bei konstantem Druck gilt Qp = ΔH = ΔU + p·ΔV. Der Unterschied ist die Volumenarbeit, die das entstehende Gas gegen den Atmosphärendruck verrichtet.
5 Reaktionswärme – Q
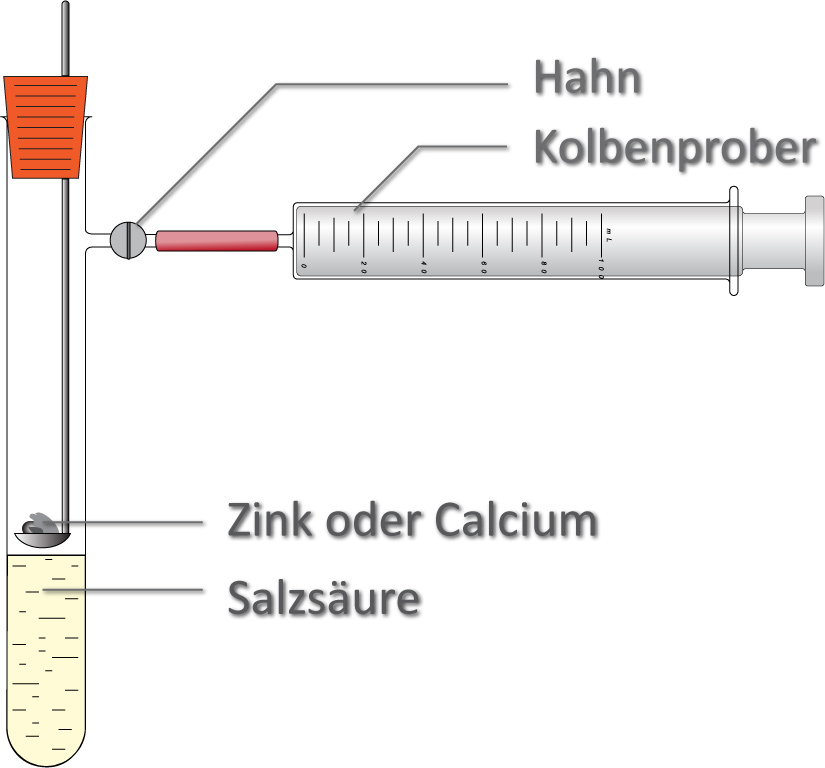
Bestimmung der Reaktionswärme – Q.
Bsp: Quantitative Umsetzung von Zink (n(Zn) = 1 mol, M(Zn) = 65,4 g/mol).
Bildung eines gasförmigen Reaktionsproduktes
- bei konstantem Volumen = Hahn geschlossen
- bei konstantem Druck = Hahn geöffnet
↑ Zum Vergrößern klicken
Teilchengleichung:
Zn + 2 H₃O⁺ (aq) + 2 Cl⁻ (aq) → Zn²⁺ (aq) + 2 Cl⁻ (aq) + 2 H₂O + H₂
Freigesetzte Reaktionswärme:
bei konstantem Volumen: QV = -156,5 kJ/mol = ΔU
Änderung der Inneren Energie = Reaktionswärme + Volumenarbeit
ΔU = QV + W
ΔU = QV - p ∙ ΔV
QV = ΔU + p ∙ 0
QV = ΔU
bei konstantem Druck: Qp = -154,0 kJ/mol = ΔH
Bei konstantem Druck gilt:
ΔU = Qp + W
ΔU = Qp – p ∙ ΔV Umstellen nach Q:
Qp = ΔU + p ∙ ΔV (= Qp = [U₂ + p ∙ V₂] – [U₁ + p ∙ V₁] )
Enthalpie H ist die spezielle Wärmeenergie bei konstantem Druck
(H von „heat"; Enthalpie: griech: En = darin; thalpos = Wärme)
Definition der Enthalpie: H = U + p ∙ V
→ Qp = H₂ – H₁ = ΔH
Prozessgrößen: Sind vom Weg abhängig (Bsp. Arbeit und Wärme) ⇨ unterschiedliche Werte, je nachdem ob man isobar oder isochor arbeitet.
a) Offene Systeme
- die meisten chemischen Reaktionen
- Volumenarbeit
- nicht alles fällt als Wärmeenergie an:
↑ Zum Vergrößern klicken
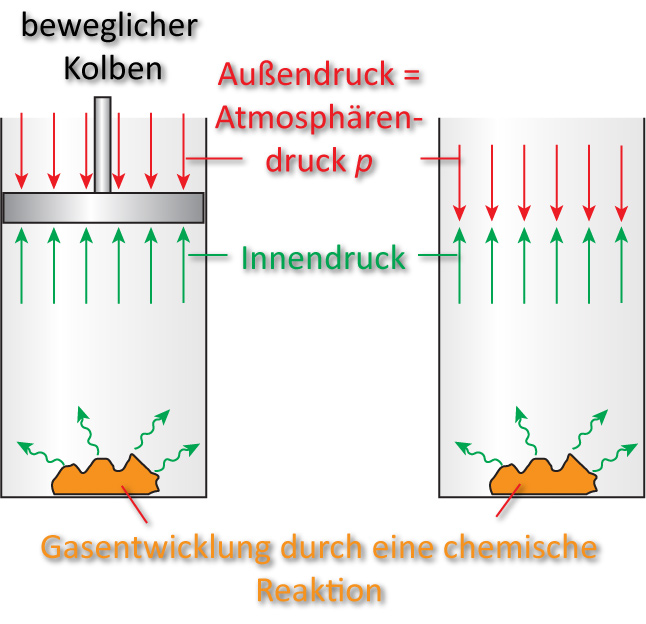
Das entstehende Gas leistet mech. Arbeit gegen den Atmosphärendruck. Die gleiche Arbeit wird auch geleistet, wenn der Kolben fehlt (Außenluft wird verdrängt).
Die Arbeit des Kolbens beträgt: p ∙ ΔV = Volumenarbeit
Änderung Reaktionsenthalpie = Änderung Reaktionsenergie + Volumenarbeit
ΔH = ΔU + p ∙ ΔV
Beispiel:
H₂SO₄ (l) + CaCO₃ (s) → CaSO₄ (s) + H₂O (l) + CO₂ (g)
Vm (CO₂) = 24,5 L/mol (bei 25 °C und 101,3 kPa = 101 300 N/m²);
ΔU = -96,1 kJ/mol
Bei der Reaktion von 1 mol Schwefelsäure:
p ∙ ΔV = 101 ∙ 10³ N/m² ∙ 24,5 ∙ 10⁻³ m³/mol
= 2,5 ∙ 10³ J/mol ( J = N ∙ m )
= 2,5 kJ/mol
ΔH = ΔU + p ∙ ΔV
= -96,1 kJ/mol + 2,5 kJ/mol
= -93,6 kJ/mol
b) Geschlossene Systeme
• keine mechanische Arbeit ⇨ ΔV = 0
• Die bei einer chemischen Reaktion gesamte freigesetzte Energie kann als Wärmeenergie anfallen (Ausnahme: z.B. Lichtenergie)
• Gesamtenergie = Reaktionsenergie ΔU (vgl. oben)
Q = ΔU + p ∙ 0
Q = ΔU
Merke: Die Energiemenge, die ein System bei konstantem Druck als Wärme an die Umgebung abgibt oder von ihr aufnimmt, wird Reaktionsenthalpie ΔH genannt.
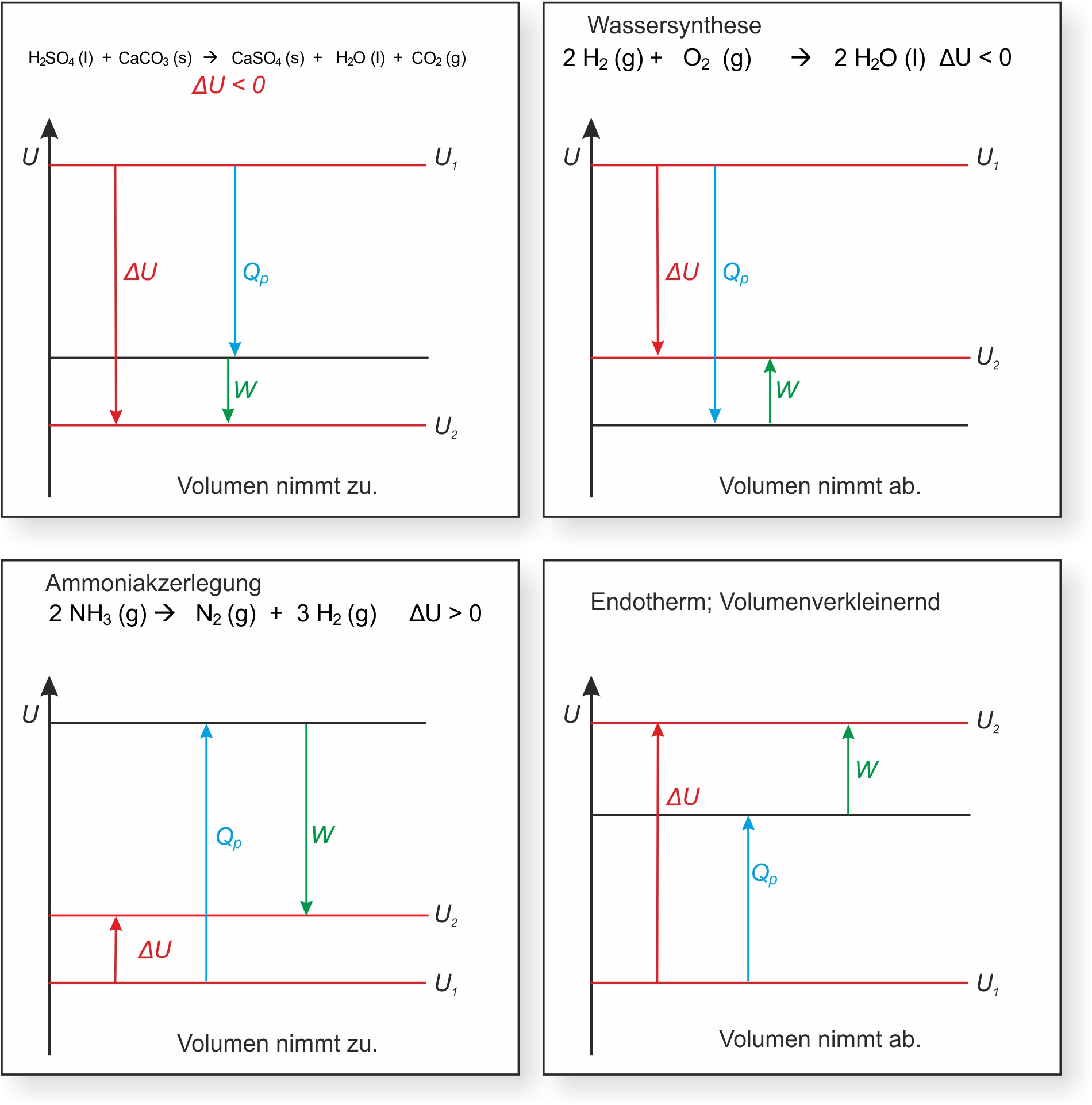
Beispiele für chemische Reaktionen mit Volumenarbeit:
↑ Zum Vergrößern klicken
Auf einen Blick – die wichtigsten Aussagen
Isochor (V = const.)
QV = ΔU
Keine Volumenarbeit, gesamte Energie als Wärme
Isobar (p = const.)
Qp = ΔH
Wärme + Volumenarbeit p·ΔV
Enthalpie
H = U + p·V
→ ΔH = ΔU + p·ΔV
Prozessgrößen
Q und W sind wegabhängig – kein Δ-Symbol, kein fester Zustandswert
Häufige Fragen zur Reaktionswärme
Was ist der Unterschied zwischen QV und Qp?
QV ist die Reaktionswärme bei konstantem Volumen (isochor, z. B. im verschlossenen Bombenkalorimeter). Dabei ist keine Volumenarbeit möglich, daher gilt QV = ΔU. Qp ist die Reaktionswärme bei konstantem Druck (isobar, z. B. im offenen Laborgefäß). Hier wird zusätzlich Volumenarbeit geleistet, wenn Gase entstehen oder verbraucht werden. Deshalb gilt Qp = ΔH = ΔU + p·ΔV.
Warum ist Q keine Zustandsgröße und warum schreibt man kein ΔQ?
Wärme Q ist eine Prozessgröße – ihr Wert hängt davon ab, auf welchem Weg ein Zustandsübergang stattfindet (isobar oder isochor liefern verschiedene Q-Werte für dieselbe Reaktion). Zustandsgrößen wie U, H oder T beschreiben den aktuellen Zustand unabhängig vom Weg – sie erhalten daher das Δ-Symbol. Q selbst ist kein Zustand, sondern eine übertragene Energiemenge – daher schreibt man Q, nicht ΔQ.
Warum unterscheiden sich QV und Qp beim Zink-Versuch?
Bei der Reaktion Zn + 2 HCl → ZnCl₂ + H₂ entsteht 1 mol H₂-Gas. Dieses Gas dehnt sich aus und verrichtet Volumenarbeit gegen den Atmosphärendruck: p·ΔV ≈ 2,5 kJ/mol. Diese Energie steht nicht als Wärme zur Verfügung – daher ist Qp = −154,0 kJ/mol betragsmäßig kleiner als QV = −156,5 kJ/mol. Die Differenz beträgt genau 2,5 kJ/mol.
Was ist die Definition der Enthalpie H?
Die Enthalpie ist definiert als H = U + p·V. Sie fasst innere Energie und den Druckterm p·V zusammen. Bei isobaren Prozessen gilt ΔH = ΔU + p·ΔV. Die Enthalpieänderung ΔH entspricht genau der bei konstantem Druck messbaren Reaktionswärme Qp. Deshalb ist ΔH die in der Laborchemie gebräuchlichste thermodynamische Größe (→ 8 Enthalpie).
In welchem System gilt Q = ΔU, und warum?
Im geschlossenen (isochoren) System gilt ΔV = 0, daher ist die Volumenarbeit W = −p·ΔV = 0. Aus ΔU = Q + W folgt dann ΔU = Q. Die gesamte Energieänderung des Systems tritt als Wärme in Erscheinung – nichts geht als mechanische Arbeit verloren. Das ist der Messprinzip des Bombenkalorimeters.
Lernkarten – Reaktionswärme Q
Klicke auf eine Karte, um die Antwort zu sehen.
Was gilt für QV bei konstantem Volumen (isochor)?
QV = ΔU
ΔV = 0 → keine Volumenarbeit →
gesamte Reaktionsenergie als Wärme messbar
Was gilt für Qp bei konstantem Druck (isobar)?
Qp = ΔH = ΔU + p·ΔV
Ein Teil der Energie geht als Volumenarbeit ab –
Qp ≠ ΔU
Wie lautet die Definition der Enthalpie H?
H = U + p·V
→ ΔH = ΔU + p·ΔV
→ Qp = H₂ − H₁ = ΔH
Warum ist Q eine Prozessgröße und warum schreibt man kein ΔQ?
Q ist wegabhängig – isobar und isochor geben verschiedene Q-Werte.
Nur Zustandsgrößen erhalten ein Δ.
Richtig: Q, nicht ΔQ!
QV = −156,5 kJ/mol bei Zn + 2 HCl.
Wie groß ist Qp?
p·ΔV (1 mol H₂) ≈ 2,5 kJ/mol
Qp = ΔU + p·ΔV
= −156,5 + 2,5 = −154,0 kJ/mol
Weiter im Kapitel Energetik
← 4 Volumenarbeit W → 6 Wärmekapazität → 8 Enthalpie H ↑ 3 Innere Energie U