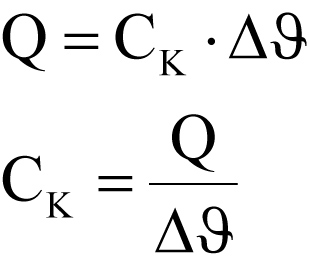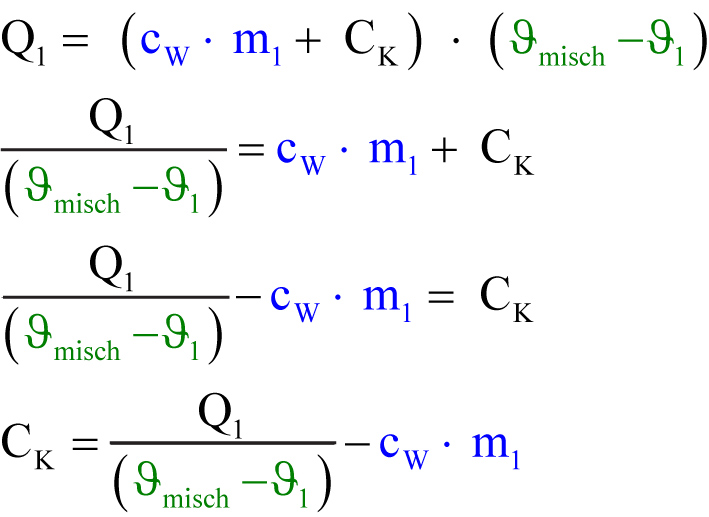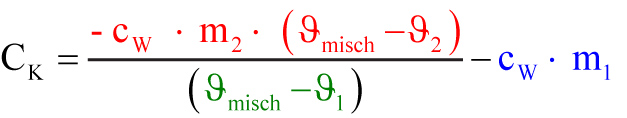Was du auf dieser Seite lernst
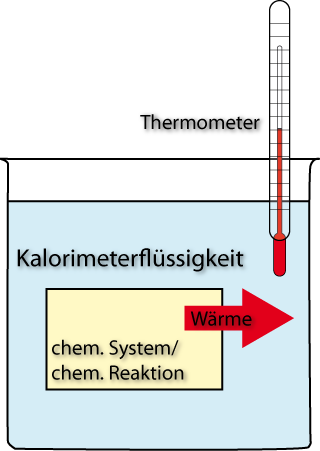
Das Kalorimeter misst Reaktionswärmen, indem es die Temperaturänderung einer bekannten Wassermenge erfasst. Grundlage ist der nullte Hauptsatz und die Beziehung Qab = −Qauf. Damit CK des Gefäßes bekannt ist, wird es vorab durch einen Mischversuch kalibriert. ΔT wird stets grafisch aus Vor- und Nachperiode bestimmt.
7 Kalorimetrie
„Nullter" Hauptsatz der Thermodynamik:
↑ Zum Vergrößern klicken
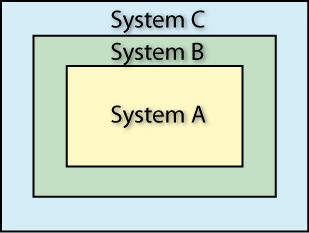
Wenn ein System A sich mit einem System B sowie B sich mit einem System C im thermischen Gleichgewicht befindet, so befindet sich auch A mit C im thermischen Gleichgewicht.
↑ Zum Vergrößern klicken
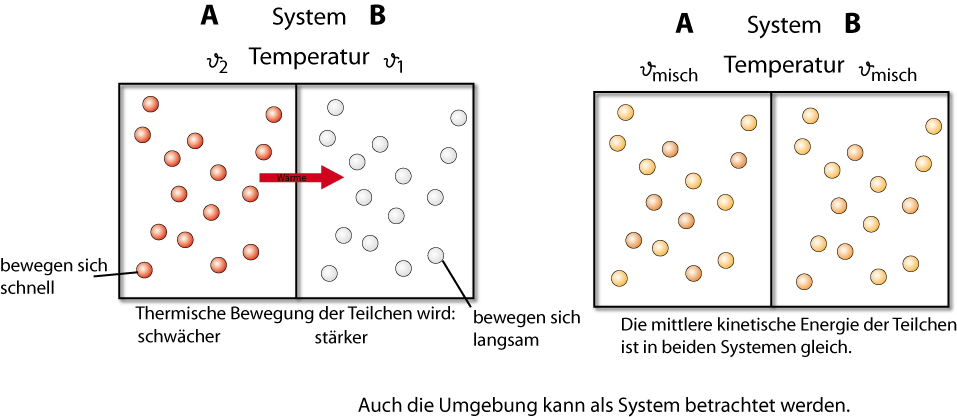
Wärme wird dabei vom System höherer Temperatur zum System niedrigerer Temperatur übertragen.
Bsp: 2 Systeme: System 1 und System 2
Es gilt:
Abgegebene Wärme (Q₁) = entgegengesetzt gleich der aufgenommenen Wärme (Q₂)
Bzw: Qab = − Qauf Q₁ = − Q₂
↑ Zum Vergrößern klicken
↑ Zum Vergrößern klicken
Δϑ = ϑ₂ − ϑ₁ = Temperaturdifferenz
mW = Masse des Wassers
cW = spezifische Wärmekapazität des Wassers (4,1868 J · g⁻¹ · K⁻¹)
— präziser historischer Wert; gerundet oft 4,184 J · g⁻¹ · K⁻¹
CK = Wärmekapazität des Kalorimetergefäßes
7.1 Bestimmung der Wärmekapazität eines Kalorimeters – CK
↑ Zum Vergrößern klicken
Die restliche Wärme nimmt das Kalorimeter auf.
Δϑ ist proportional zur aufgenommenen Wärmemenge.
↑ Zum Vergrößern klicken
Bestimmung von CK
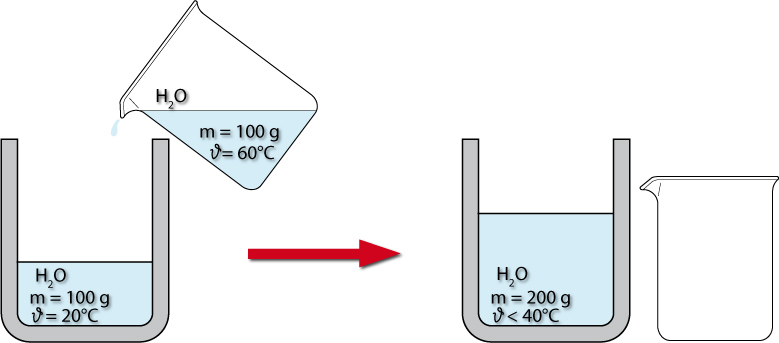
- Wasser der Masse m₁ und der Temperatur ϑ₁ eingefüllt (damit das Kalorimeter eine bestimmbare Temperatur hat).
- Wasser der Masse m₂ (gleichviel) und der Temperatur ϑ₂ eingefüllt.
- Messung von ϑmisch
Das warme Wasser gibt die Wärme Q₂ ab (Q₂ < 0)
Q₂ = cW · m₂ · (ϑmisch − ϑ₂)
↑ Zum Vergrößern klicken
Das kältere Wasser und das Gefäß nehmen Wärme auf:
Q₁ = QW + QK
Q₁ = cW · m₁ · (ϑmisch − ϑ₁) + CK · (ϑmisch − ϑ₁)
Es gilt Qab = −Qauf bzw. Q₁ = −Q₂
Q₁ + Q₂ = 0 (Energieerhaltung)
Q1 einsetzen:
↑ Zum Vergrößern klicken
Für die kalorimetrische Bestimmung müssen chemische Reaktionen folgende Voraussetzungen erfüllen:
- schnell ablaufen
- vollständig (oder weitgehend vollständig) ablaufen
- eine ausreichend große Reaktionswärme besitzen
⇨ Veresterung ist ungeeignet
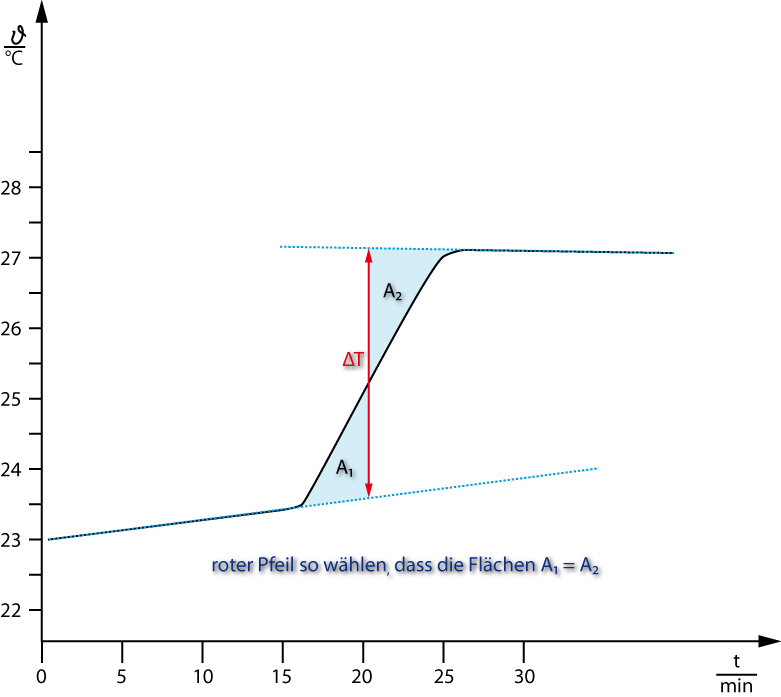
Idealfall: Kein Austausch von Wärme zwischen Kalorimeter und Umgebung. Leider ist das nicht der Fall. Während der Vorperiode und Nachperiode ist die Temperatur nicht konstant. Deshalb findet eine grafische Auswertung statt, wobei man die Temperaturlinien entsprechend verlängert (vgl. Abb).
↑ Zum Vergrößern klicken
Vorperiode = Zeit vor der chemischen Reaktion
Hauptperiode = chemische Reaktion bis zum Endpunkt des Wärmeübergangs
Nachperiode = Zeit nach beendetem Wärmeübergang
ΔT: wird grafisch bestimmt ⇨ Temperatur-Zeit-Kurven werden verlängert ⇨ senkrechte Linie wird so eingezeichnet, dass die Flächen A1 = A2 sind.
Dewargefäße:
- Doppelte Glaswand (dazwischen evakuiert) ⇨ keine Konvektion
- Wärmeabstrahlung wird minimiert durch Verspiegelung
- Kalorimeter: Meist wird Wasser benutzt.
Auf einen Blick – die wichtigsten Aussagen
Nullter Hauptsatz
A ⇌ B und B ⇌ C
→ A ⇌ C im therm. Gleichgewicht
Energieerhaltung
Qab = −Qauf
Q₁ + Q₂ = 0
Kalibrierung
CK des Gefäßes wird vorab durch Mischversuch mit zwei Wasserportionen bestimmt
ΔT grafisch
Wegen Wärmeverlusten: ΔT aus Vor-/Nachperiode grafisch bestimmen (A1 = A2)
Häufige Fragen zur Kalorimetrie
Was besagt der „nullte" Hauptsatz der Thermodynamik?
Wenn System A mit System B und System B mit System C im thermischen Gleichgewicht ist, dann ist auch A mit C im thermischen Gleichgewicht. Dieser Satz klingt trivial, ist aber die logische Grundlage für alle Temperaturmessungen: Er begründet, warum ein Thermometer (System B) als Vermittler zwischen zwei Systemen A und C funktioniert.
Warum nennt man ihn den „nullten" und nicht den dritten Hauptsatz?
Die drei klassischen Hauptsätze (Energieerhaltung, Entropiezunahme, absoluter Nullpunkt) waren bereits etabliert, als man erkannte, dass das thermische Gleichgewicht eine noch fundamentalere Voraussetzung darstellt. Da er logisch vor den anderen steht, aber erst nachträglich formuliert wurde, erhielt er die Nummer „0".
Warum muss CK des Kalorimeters bestimmt werden?
Das Kalorimetergefäß selbst nimmt ebenfalls Wärme auf (oder gibt sie ab). Würde man CK nicht berücksichtigen, würde man zu wenig Wärme messen – die Reaktionsenthalpie wäre falsch. Durch einen Mischversuch mit zwei Wasserportionen bekannter Temperatur lässt sich CK berechnen, bevor das eigentliche Experiment durchgeführt wird.
Warum wird ΔT grafisch und nicht direkt abgelesen?
In der Praxis ist kein Kalorimeter perfekt isoliert – es gibt immer einen kleinen Wärmeaustausch mit der Umgebung. Dadurch steigt oder fällt die Temperatur auch ohne Reaktion leicht (Vor- und Nachperiode). Die grafische Methode verlängert die Geraden der Vor- und Nachperiode und zieht eine senkrechte Linie so, dass die Flächen A1 = A2 sind. Damit wird das „wahre" ΔT der Reaktion unabhängig von den Wärmeverlusten ermittelt.
Was macht ein Dewargefäß besser als ein normales Gefäß?
Ein Dewargefäß minimiert alle drei Wärmeübertragungsmechanismen: Das Vakuum zwischen den Glaswänden verhindert Konvektion und Wärmeleitung durch Luft. Die Verspiegelung der Innenwände reduziert Wärmestrahlung. Dadurch verhält sich das Dewargefäß näherungsweise wie ein abgeschlossenes System – es ist das gebräuchlichste Kalorimetergefäß im Schullabor (→ 1 Systeme).
Lernkarten – Kalorimetrie
Klicke auf eine Karte, um die Antwort zu sehen.
Was besagt der nullte Hauptsatz der Thermodynamik?
A ⇌ B und B ⇌ C im therm. GGW
→ A ⇌ C im therm. GGW
Grundlage jeder Temperaturmessung
Wie lautet die Energiebilanz im Kalorimeter?
Qab = −Qauf
bzw. Q₁ + Q₂ = 0
(Energieerhaltung im abgeschlossenen System)
Warum muss CK des Kalorimeters bestimmt werden?
Das Gefäß nimmt selbst Wärme auf.
Ohne CK würde man zu wenig Wärme messen.
→ Kalibrierung durch Mischversuch
Was bedeuten Vor-, Haupt- und Nachperiode?
🔵 Vorperiode: vor der Reaktion
🟡 Hauptperiode: Reaktion bis Wärmeübergang
🟢 Nachperiode: nach dem Wärmeübergang
Welche drei Voraussetzungen muss eine Reaktion für die Kalorimetrie erfüllen?
1. Schnell ablaufen
2. Vollständig ablaufen
3. Ausreichend große Reaktionswärme
→ Veresterung: ungeeignet!
Weiter im Kapitel Energetik
← 6 Wärmekapazität → 7.2 Neutralisationsenthalpie → 8 Enthalpie H ↑ 1 Systeme