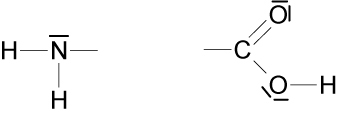5 Proteine
5.1 Aminosäure
5.1.1 Vorkommen
Die Aminosäuren kommen im pflanzlichen und tierischen Organismus frei und gebunden vor. Aminosäuren sind Bauelemente der Eiweißstoffe (Proteine).
5.1.2 Funktionelle Gruppen
Aminosäuren enthalten (formal) Amino- und Carboxyl-Gruppen.
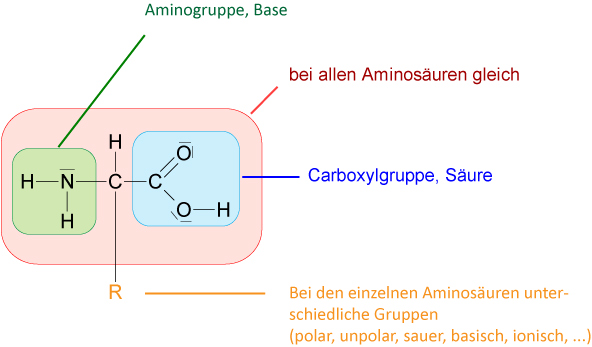
5.1.3 Aminoessigsäure (Glycin)
[1819 entdeckt]
Fischer-Projektion
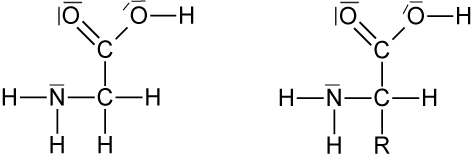
L-Glycin α-L-Aminosäuren
Merke: Alle Aminosäuren, die in Proteinen gefunden werden, besitzen die L-Konfiguration. Weiterhin steht die Aminogruppe bei allen Aminosäuren, die aus natürlich vorkommenden Proteinen gewonnen werden, am α-C-Atom (2-Aminocarbonsäuren sind α-Aminsäuren).
Enantiomere (optische Antipoden) Verhalten sich wie Bild und Spiegelbild
5.1.4 Gleichgewicht

Aminosäureform Zwitterionenform
Die Zwitterionenform wird begünstigt:
- im Kristall (100 %) durch höhere Gitterenergie;
- in wässriger Lösung (99%) durch höhere Hydrationsenergie
Für das Vorliegen der Zwitterionenform im Kristall spricht u.a. der abnorm hohe Schmelzpunkt von Glycin (bei 230 °C unter Zersetzung).
Zum Vergleich die Schmelzpunkte von:
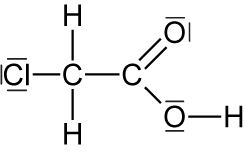
Chloressigsäure: 62°C

Hydroxyessigsäure: 78°C
5.1.5 Herstellung von Glycin aus Chloressigsäure + Ammoniak
In der 1. Stufe wird Chloressigsäure deprotoniert:
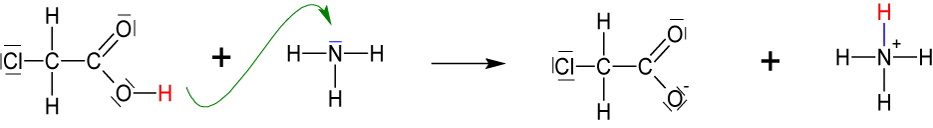
Das entstandene Anion reagiert mit dem überschüssigen Ammoniak weiter: