Säurestärke
-
2.6 Phenole
2.6 Phenole = Hydroxybenzole
Vorkommen:
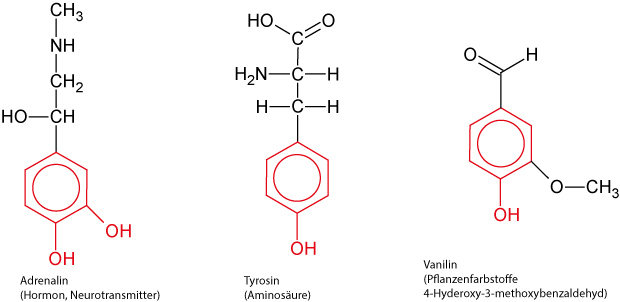
2.6.1 Monohydroxybenzol = Phenol
a) Physikalische Eigenschaften
- Smp.: 40,9; Sdp.: 181,9 °C
- In Wasser nur mäßig löslich (bildet bei ZT eine Emulsion)
- Starkes Zellgift, durch Haut resorbiert
b) Chemische Eigenschaften
- Oxidiert an Luft leicht ⇨ rötliche Färbung
- Karbolsäure“: 2 %ige Säure; Desinfektion
- Im Gegensatz zu Ethanol sauer:
1. Phenol als schwache Säure
pKS = 9,95
Grenzformeln des Phenolations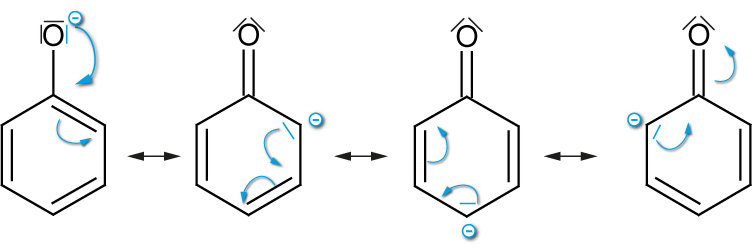
Phenol Ethanol Säurestärke höher niedriger Induktiver Effekt 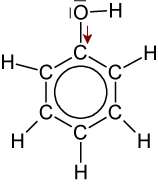
schwacher -I-Effekt ⇨ elektronenziehend
⇨ H⁺-Abgabe ist erleichtert
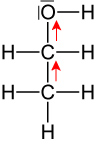
+I-Effekt ⇨ Elektro-nenschiebend
H⁺-Abgabe ist er-schwert.Anion: Mesomeriestabilisiert konjungierte Base (Phenolat): negative Ladung ist über den ganzen Ring delokalisiert ⇨ stabilisiert! Keine Stabilisierung durch Mesomerien Brønsted-Säure stärker schwächer Brønsted-Base schwächer stärker 2.6.3 Synthese
90% der Weltproduktion nach der Hock-Synthese
Wirtschaftliches Verfahren, da auch Aceton nutzbar ist.
siehe Heftaufschrieb
2.6.4 Verwendung
Herstellung von Kunststoffen (Polyamide, Phenoplasten, Phenolharzen und Polycarbonaten)
-
6 Chlorwasserstoff-Gas und Wasser
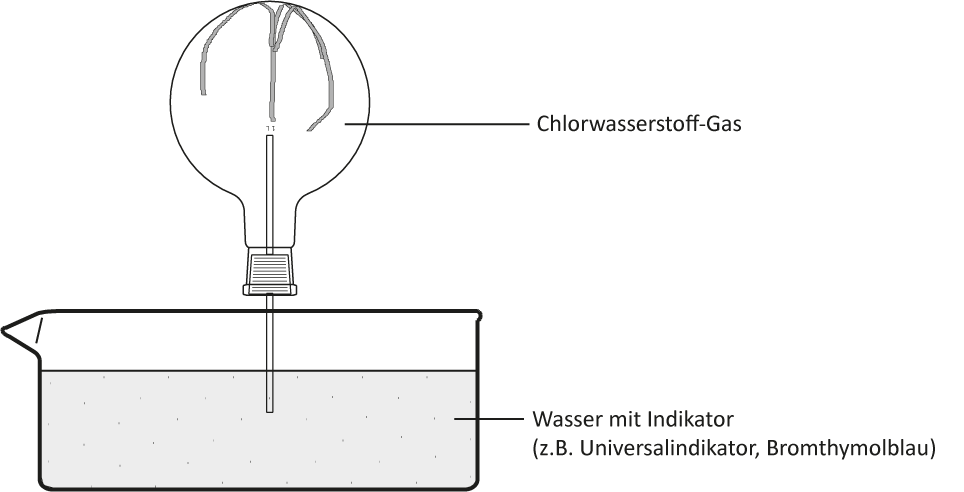
6 Chlorwasserstoff-Gas und Wasser (Springbrunnen)
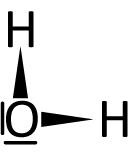
Chlorwasserstoff: Summenformel HCl, polare Atombindung, Gas, stechender Geruch
Wasser: Summenformel H₂O, polare Atombindung, Flüssigkeit, geruchslos
a) Versuch:
b) Beobachtung:
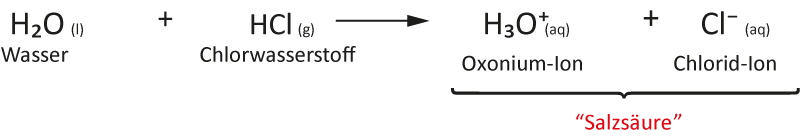
Das Wasser „schießt“ bergauf in den Rundkolben. Die Indikatorfarbe schlägt nach rot/gelb um. Die rote wässrige Lösung ist geruchlos.c) Reaktionsgleichung – Struktur/Lewisformel:
Theoretisch gibt es zwei Möglichkeiten, wie Wasser und Chlorwasserstoff reagieren können.
- Formuliere einmal diese zwei Möglichkeiten als Reaktionsgleichung mit Strukturformeln.
- Entscheide, welche dieser beiden möglichen Reaktionen tatsächlich abläuft. Falls du nicht drauf kommst, gehe zurück zum Thema: Säure-Stärke
{slider title="Lösung" open="false" class="icon"}
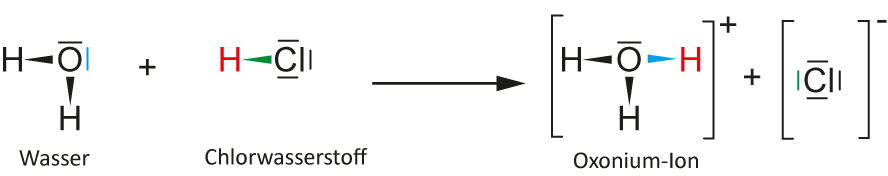
1. Möglichkeit:
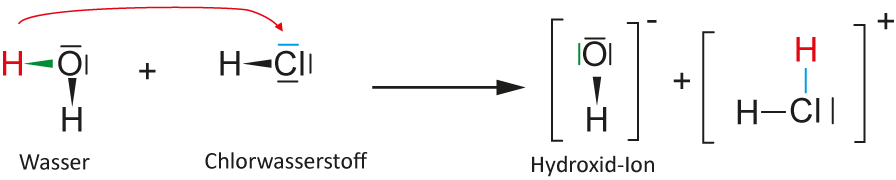
2. Möglichkeit:
Chlorwasserstoff ist die stärkere Säure, da Chlor ein größeres Atom ist, als Wasserstoff. Außerdem ist das Hydroxid-Ion ist eine sehr starke Base.
{/sliders}
Nachweis der gebildeten Ionen:
- Leitfähigkeitsmessung
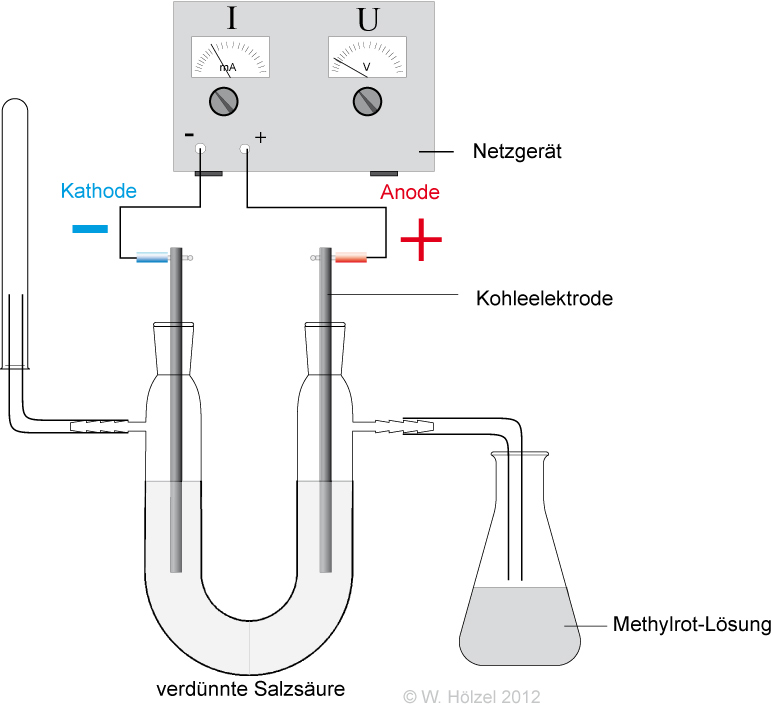
- durch Elektrolyse: An der Anode (+-Pol) entsteht dabei Cl₂-Gas. Somit müssen in der verdünnten Salzsäure Chlorid-Ionen (Cl⁻-Ionen) vorliegen.
- durch Indikator: Die Gelbfärbung bei Bromthymolblau zeigt Oxonium-Ionen (H₃O⁺) an.
Reaktionsgleichung Zusammenfassung
{slider title="Lösung" open="false" class="icon"}
Begründung:
Chlor (vom Chlorwasserstoff) ist ein größeres Atom als Sauerstoff (vom Wasser). Deshalb ist Chlorwasserstoff eine stärkere Säure und gibt das Proton (H⁺) und Wasser nimmt das Proton auf.
verdünnte Salzsäure enthält hydratisierte Oxonium- und Chlorid-Ionen und Wassermoleküle.{/sliders}
Verdünnte Salzsäure enthält hydratisierte Oxonium- und Chlorid-Ionen und Wassermoleküle.
d) ProtolyseschemaFormuliere für diese Reaktion einmal das Protolyseschema:
{slider title="Lösung" open="false" class="icon"}
{/sliders}
e) Erklärung:
Chlorwasserstoff-Gas reagiert mit Wasser. Im Zylinder entsteht ein Unterdruck. Die Oxonium-Ionen färben den Universalindikator/Bromthymolblau rot/gelb.Salzsäure: = wässrige Lösung des Gases Chlorwasserstoff Wenn man sehr viel HCl-Gas in Wasser einleitet, reagieren nicht mehr alle HCl-Moleküle mit den H₂O-Molekülen. Diese HCl-Moleküle liegen „gelöst“ vor. Es ist so „rauchende“ bzw. konzentrierte Salzsäure entstanden.
Leitfähigkeit Geruch Indikatorpapier Teilchen verdünnte Salzsäure + - rot H₂O, H₃O⁺, Cl⁻ rauchende Salzsäure + + rot H₂O, H₃O⁺, Cl⁻, HCl