Was du auf dieser Seite lernst
Du lernst, wie man die Lage eines Gleichgewichts mit verschieden langen Pfeilen sichtbar macht. Das Kollisionsmodell erklärt, warum die Reaktionsgeschwindigkeit vom Produkt der Konzentrationen abhängt – und warum ein Katalysator zwar schneller zum Gleichgewicht führt, es aber nicht verschiebt.
Grundlagen aus diesem Kapitel
Die Merkmale des dynamischen Gleichgewichts: → Merkmale eines chemischen Gleichgewichts · Konkret am Beispiel des Estergleichgewichts: → Estergleichgewicht
2.6 Schreibweise für Gleichgewichtsreaktionen
Die Lage des Gleichgewichts lässt sich durch unterschiedlich lange Gleichgewichtspfeile visualisieren. Am Beispiel des Estergleichgewichts (S = Säure, A = Alkohol, E = Ester, W = Wasser):
↑ Zum Vergrößern klicken
✕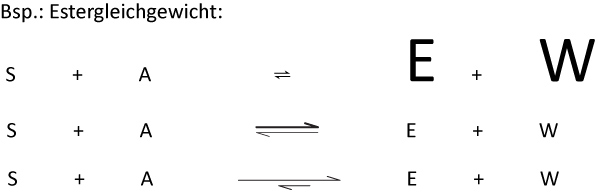
Merksatz – Pfeilnotation
- Gleich lange Pfeile (⇌): Gleichgewicht liegt in der Mitte – ähnlich viele Edukte wie Produkte.
- Längerer Pfeil nach rechts (⟹): Gleichgewicht liegt auf der Produktseite – Produkte überwiegen.
- Längerer Pfeil nach links (⟸): Gleichgewicht liegt auf der Eduktseite – Edukte überwiegen.
2.7 Kollisionsmodell und Reaktionsgeschwindigkeit
Das Kollisionsmodell erklärt, warum die Reaktionsgeschwindigkeit vom Produkt der Konzentrationen der Reaktionspartner abhängt. Entscheidend ist die Anzahl der möglichen Zusammenstöße (Treffermöglichkeiten) zwischen Edukt-Teilchen:
↑ Zum Vergrößern klicken
✕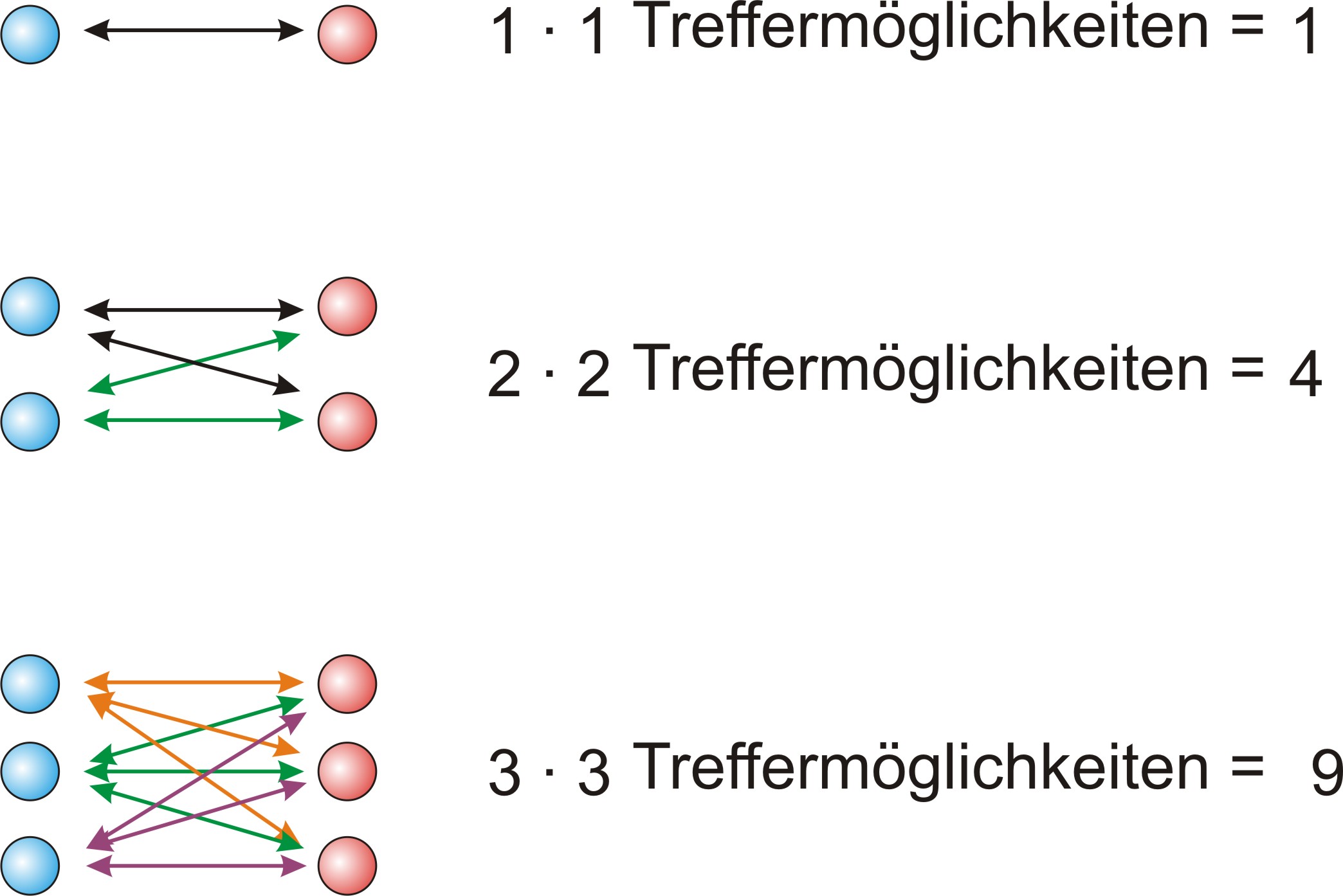
Das Kollisionsmodell liefert die Grundlage für das Massenwirkungsgesetz: Die Geschwindigkeit der Hinreaktion ist proportional zum Produkt der Edukt-Konzentrationen, die der Rückreaktion proportional zum Produkt der Produkt-Konzentrationen.
Aktivierungsenergie und Katalysator
Das Energiediagramm zeigt, wie ein Katalysator die Aktivierungsenergie senkt und damit die Reaktion beschleunigt:
↑ Zum Vergrößern klicken
✕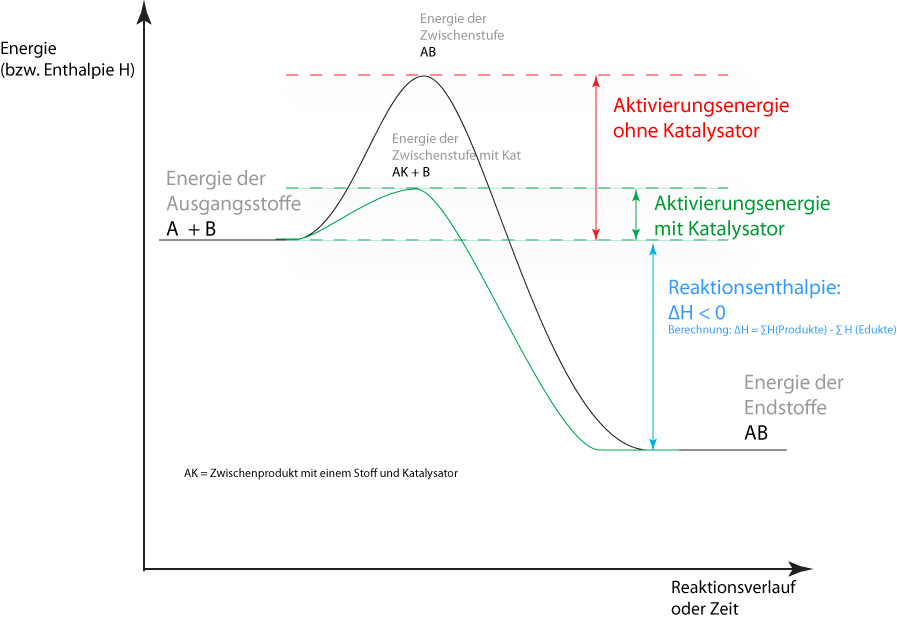
Wichtiger Hinweis zum Katalysator: Ein Katalysator senkt die Aktivierungsenergie für Hin- und Rückreaktion gleichermaßen. Er beschleunigt das Erreichen des Gleichgewichts – verschiebt es aber nicht. Die Lage des Gleichgewichts (Kc-Wert) bleibt durch einen Katalysator unverändert.
Auf einen Blick – die wichtigsten Aussagen
Pfeilnotation
Die Länge der Gleichgewichtspfeile zeigt die Lage des Gleichgewichts: Längerer Pfeil = bevorzugte Reaktionsrichtung.
Kollisionsmodell
Treffermöglichkeiten = n(A) · n(B). Verdoppelt man beide Konzentrationen, vervierfacht sich die Reaktionsrate (2·2 = 4).
Aktivierungsenergie
Ein Katalysator senkt die Aktivierungsenergie über ein energieärmeres Zwischenprodukt (AK). Die Reaktionsenthalpie ΔH bleibt unverändert.
Katalysator ≠ Verschiebung
Ein Katalysator beschleunigt Hin- und Rückreaktion gleichermaßen. Er bringt das System schneller ins Gleichgewicht – verschiebt es aber nicht.
Häufige Fragen – Schreibweise und Kollisionsmodell
Was bedeutet es, wenn ein Gleichgewichtspfeil länger ist als der andere?
Ein längerer Pfeil zeigt die bevorzugte Reaktionsrichtung an. Zeigt der längere Pfeil nach rechts (→⇌), liegt das Gleichgewicht auf der Produktseite – es bilden sich mehr Produkte als Edukte. Zeigt er nach links (⇌←), überwiegen die Edukte. Gleich lange Pfeile (⇌) bedeuten: ähnlich viele Edukte und Produkte im Gleichgewicht. Das genaue Verhältnis beschreibt der Kc-Wert.
Was besagt das Kollisionsmodell für Gleichgewichtsreaktionen?
Die Geschwindigkeit einer Reaktion hängt davon ab, wie oft sich Teilchen treffen und zusammenstoßen. Die Anzahl der Treffermöglichkeiten ist proportional zum Produkt der Teilchenzahlen (bzw. Konzentrationen) der Reaktionspartner: Wenn n(A) = 2 und n(B) = 2, gibt es 2 · 2 = 4 Treffermöglichkeiten. Bei n(A) = 3 und n(B) = 3 sind es 3 · 3 = 9. Dieses Prinzip bildet die Grundlage des Massenwirkungsgesetzes.
Was passiert mit der Reaktionsgeschwindigkeit, wenn man eine Konzentration verdoppelt?
Für die Reaktion A + B → Produkte gilt nach dem Kollisionsmodell: v ∝ [A] · [B]. Verdoppelt man nur [A] (von 1 auf 2), verdoppeln sich die Treffermöglichkeiten. Verdoppelt man beide Konzentrationen, vervierfachen sich die Treffermöglichkeiten (2 · 2 = 4). Die Reaktionsgeschwindigkeit steigt also quadratisch, wenn man beide Eduktkonzentrationen verdoppelt. Wichtig: Das gilt analog für die Rückreaktion mit den Produktkonzentrationen.
Wie wirkt ein Katalysator auf die Aktivierungsenergie – und warum verschiebt er das Gleichgewicht nicht?
Ein Katalysator bildet ein energieärmeres Zwischenprodukt (AK) mit einem der Reaktionspartner.
Dadurch ist die Aktivierungsenergie für die Hinreaktion und für die Rückreaktion
gleichermaßen kleiner. Beide Reaktionen werden schneller – aber im gleichen Verhältnis.
Da sich beide Geschwindigkeiten proportional ändern, bleibt das Gleichgewicht (Kc) unverändert.
Merksatz: Ein Katalysator verändert nicht, wo das Gleichgewicht liegt, sondern nur, wie schnell es erreicht wird.
Mehr zur Verschiebung des Gleichgewichts:
Prinzip von Le Chatelier.
Was ist der Unterschied zwischen Reaktionsenthalpie ΔH und Aktivierungsenergie EA?
Die Reaktionsenthalpie ΔH ist der Energieunterschied zwischen Edukten und Produkten – sie beschreibt, ob eine Reaktion exotherm (ΔH < 0) oder endotherm (ΔH > 0) ist. Die Aktivierungsenergie EA ist die Energiebarriere, die Teilchen überwinden müssen, damit die Reaktion überhaupt abläuft. Ein Katalysator senkt EA, ändert aber nicht ΔH. Die thermodynamischen Hintergründe zu ΔH findest du in der Energetik: Enthalpie H.
Lernkarten – Schreibweise und Kollisionsmodell
Klicke auf eine Karte, um die Antwort zu sehen.
Was zeigt ein längerer Pfeil auf der rechten Seite des Gleichgewichtspfeils (A ⇌⟹ B) an?
Das Gleichgewicht liegt auf der Produktseite. Es überwiegen die Produkte. Kc > 1.
Wie viele Treffermöglichkeiten gibt es bei 4 blauen und 4 roten Teilchen?
4 · 4 = 16 Treffermöglichkeiten. Allgemein: Treffermöglichkeiten = n(A) · n(B).
Erkläre: Warum ändert ein Katalysator die Lage des Gleichgewichts nicht?
Ein Katalysator senkt die Aktivierungsenergie für Hin- UND Rückreaktion gleichermaßen. Beide Geschwindigkeiten steigen im gleichen Verhältnis → Kc bleibt unverändert.
Was ändert ein Katalysator, was ändert er nicht?
Ändert: Aktivierungsenergie EA (senkt sie) · Reaktionsgeschwindigkeit (erhöht sie) · Zeit bis zum GG (verkürzt sie)
Ändert nicht: ΔH · Kc · Gleichgewichtslage
Bei 25 °C beträgt Kc für A ⇌ B = 9. Im GG gilt [A] = 0,3 mol/L. Berechne [B] und zeichne die passenden Gleichgewichtspfeile.
Kc = [B]/[A] = 9
[B] = 9 · 0,3 = 2,7 mol/L
Produkte überwiegen stark → längerer Pfeil rechts (A ⇌⟹ B)
Weiter im Kapitel Gleichgewichtsreaktionen
← Estergleichgewicht → Benzoesäure-Gleichgewicht
🔁 Verwandte Seiten: Massenwirkungsgesetz · Prinzip von Le Chatelier · Enthalpie H (Energetik)
