Brønsted-Säure
-
02 Gleichgewichte
Was du auf dieser Seite lernst
Konzentrierte Schwefelsäure ist hygroskopisch – sie nimmt begierig Wasser aus der Luft auf. Auf dieser Seite untersuchst du, wie sich dabei ein dynamisches Gleichgewicht einstellt, und lernst die zweistufige Protolyse der Schwefelsäure mit Wasser kennen.
Grundlagen aus der 9. Klasse
Die Grundlagen zu Säure-Base-Reaktionen und der Bronsted-Definition hast du bereits in der 9. Klasse kennengelernt: → Säure-Base-Definition nach Brønsted (Kl. 9)
2.1 Schwefelsäure – Wasserdampf – Gleichgewicht
a) konzentrierte Schwefelsäure (H2SO4)
- enthält Schwefelsäuremoleküle
- zeichnet einmal die Strukturformel(n) (unter Berücksichtigung, dass die Edelgas-Regel erfüllt sein muss):
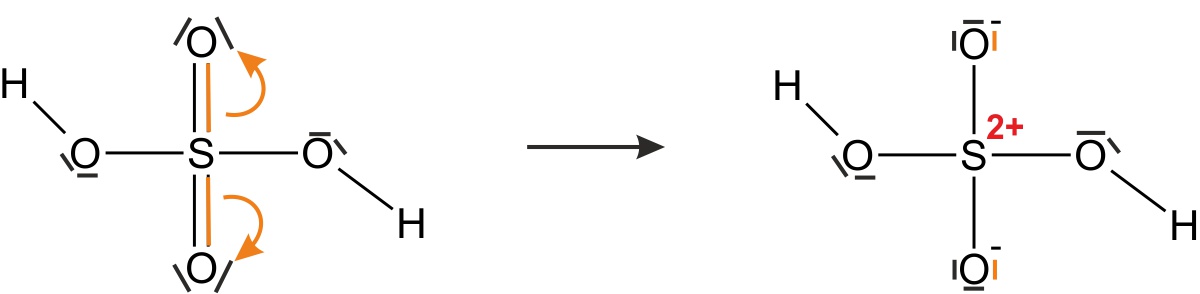
- Konzentrierte Schwefelsäure ist geruchlos.
- Siedetemperatur beträgt 300 °C.
- Konzentrierte Schwefelsäure reagiert heftig mit Wasser unter Ionenbildung (Protolyse-Reaktion).
Formuliert für die Reaktion der Schwefelsäure mit Wasser in zwei Stufen die Reaktionsgleichung in Summenformeln:
Lösung: Reaktionsgleichungen (zweistufige Protolyse)
H2SO4 + H2O → HSO4− + H3O+
HSO4− + H2O → SO42− + H3O+b) Verdünnte Schwefelsäure
Verdünnte Schwefelsäure enthält folgende Ionen und Moleküle; nennt diese:Lösung: Bestandteile verdünnter Schwefelsäure
- H3O+ (Oxonium-Ion; früher Hydronium-Ion oder „Hydroxonium-Ion")
- HSO4− (Hydrogensulfat-Ion)
- SO42− (Sulfat-Ion; in geringer Konzentration)
- H2O (Wasser; in großer Menge vorhanden)
2.2 Langzeitversuch: Konzentrierte Schwefelsäure
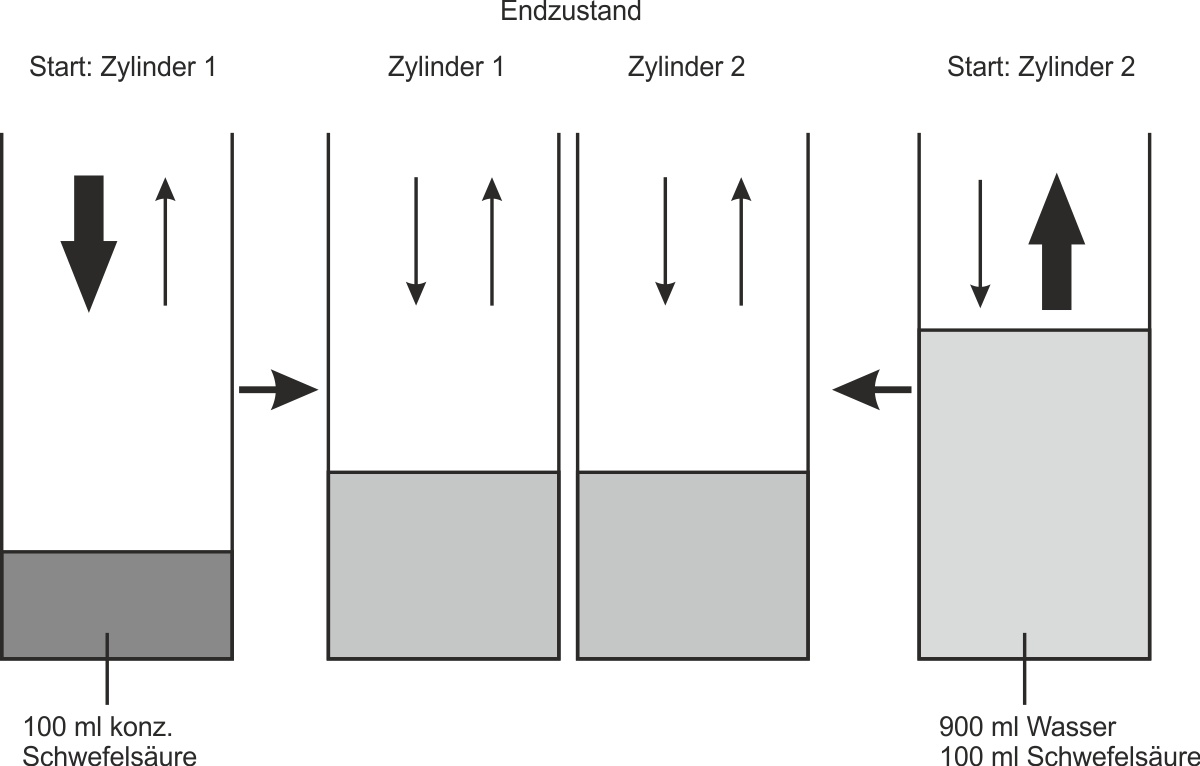
Versuchsdurchführung: In einen Zylinder 1 werden 100 ml konzentrierte Schwefelsäure gegeben. In einen Zylinder 2 werden zunächst 900 ml Wasser und dann vorsichtig 100 ml konzentrierte Schwefelsäure gegeben. Beide Zylinder werden mehrere Jahre offen im gleichen Zimmer stehengelassen.
↑ Zum Vergrößern klicken
✕
Versucht eine Deutung dieses Versuchs:
Lösung: Deutung des Langzeitversuchs
- Zylinder 1 (konz. H2SO4) nimmt mehr H2O-Moleküle aus der Umgebungsluft auf, als er abgibt.
- Zylinder 2 (verdünnte H2SO4) gibt mehr H2O-Moleküle an die Umgebungsluft ab, als er aufnimmt.
- Nach einigen Jahren hat sich ein Gleichgewichtszustand eingestellt: Pro Zeiteinheit werden gleich viele H2O-Moleküle an die Umgebung abgegeben wie H2O-Moleküle in die Lösung aufgenommen werden.
Auf einen Blick – die wichtigsten Aussagen
Hygroskopie
Konzentrierte H2SO4 ist hygroskopisch – sie zieht Wasser aus der Luft an. Je konzentrierter die Lösung, desto stärker diese Eigenschaft.
Dynamisches Gleichgewicht
Im Gleichgewicht sind Auf- und Abgabe von H2O-Molekülen gleich groß – es herrscht mikroskopische Aktivität bei makroskopischer Konstanz.
Zweistufige Protolyse
H2SO4 gibt in zwei Stufen je ein Proton ab. Im zweiten Schritt ist HSO4− eine schwächere Säure als H2SO4.
Siedepunkt 300 °C
Der hohe Siedepunkt von 300 °C erklärt sich durch starke zwischenmolekulare Kräfte (Wasserstoffbrücken und van-der-Waals-Kräfte).
Häufige Fragen – Schwefelsäure-Gleichgewicht
Was bedeutet „hygroskopisch" und warum ist konzentrierte Schwefelsäure so wassergierig?
Als hygroskopisch bezeichnet man Stoffe, die Wasser aus der Umgebungsluft aufnehmen. Konzentrierte H2SO4 reagiert heftig mit Wasser unter starker Wärmefreisetzung (Protolyse). Da diese Reaktion sehr exotherm ist, liegt das Gleichgewicht stark auf der Seite der Produkte – die Säure „zieht" Wassermoleküle regelrecht aus der Luft, bis sich ein dynamisches Gleichgewicht eingestellt hat.
Warum gibt verdünnte Schwefelsäure Wasser an die Luft ab, konzentrierte aber nicht?
Der entscheidende Faktor ist der Wasserdampfdruck der Lösung. Verdünnte Schwefelsäure hat einen höheren Wasserdampfdruck als die Umgebungsluft → H2O-Moleküle verdunsten. Konzentrierte H2SO4 hat dagegen einen sehr niedrigen Wasserdampfdruck → sie nimmt Wasser auf. Im Langzeitversuch gleichen sich beide Zylinder auf einen gemeinsamen Gleichgewichtszustand an. Mehr dazu auf der Seite Verschiebung des Gleichgewichts.
Was ist ein chemisches Gleichgewicht und woran erkennt man es?
Ein chemisches Gleichgewicht liegt vor, wenn Hin- und Rückreaktion gleich schnell ablaufen. Äußerlich scheint die Reaktion zum Stillstand gekommen zu sein (makroskopische Konstanz), auf molekularer Ebene laufen aber ständig beide Richtungen ab (dynamisches Gleichgewicht). Im Langzeitversuch erkennt man das Gleichgewicht daran, dass sich die Füllhöhen der Zylinder nicht mehr verändern. Weitere Merkmale findest du auf der Seite Merkmale eines chemischen Gleichgewichts.
Wie läuft die zweistufige Protolyse der Schwefelsäure mit Wasser ab?
H2SO4 ist eine zweiprotonige Säure und gibt ihre Protonen in zwei Schritten ab:
1. Stufe (vollständig):
H2SO4 + H2O → HSO4− + H3O+2. Stufe (unvollständig):
HSO4− + H2O ⇌ SO42− + H3O+Da HSO4− eine schwächere Säure ist, läuft die zweite Stufe nicht vollständig ab → daher enthält verdünnte Schwefelsäure sowohl SO42−- als auch HSO4−-Ionen. Die Grundlagen zur Protolyse hast du in der 9. Klasse kennengelernt: Bronsted-Definition (Kl. 9).
Warum darf man niemals Wasser zu konzentrierter Schwefelsäure geben?
Die Reaktion von konz. H2SO4 mit Wasser ist stark exotherm. Gibt man Wasser zu Säure, kann sich das Wasser an der Oberfläche spontan in Dampf verwandeln, was zu einem explosionsartigen Verspritzen der Säure führt. Richtig ist daher: immer Säure langsam in Wasser geben, nie umgekehrt! Die thermodynamischen Hintergründe (Reaktionsenthalpie) findest du in der Einheit Enthalpie H (Energetik).
Lernkarten – Schwefelsäure-Gleichgewicht
Klicke auf eine Karte, um die Antwort zu sehen.
1Was bedeutet „hygroskopisch" und welcher bekannte Stoff zeigt diese Eigenschaft besonders stark?
Hygroskopisch = Wasser aus der Luft aufnehmend. Konzentrierte H2SO4 ist ein typisches Beispiel: Sie kann sogar organische Stoffe durch Wasserentzug verkohlen.
2Nenne die vier Teilchenarten, die in verdünnter Schwefelsäure vorhanden sind.
H3O+ (Oxonium-Ion) · HSO4− (Hydrogensulfat-Ion) · SO42− (Sulfat-Ion, wenig) · H2O (viele Wassermoleküle)
3Was passiert mit Zylinder 1 (konz. H2SO4) und Zylinder 2 (verd. H2SO4) im Langzeitversuch?
Zylinder 1 nimmt H2O auf → Füllstand steigt. Zylinder 2 gibt H2O ab → Füllstand sinkt. Nach Jahren: gleiche Konzentration → dynamisches Gleichgewicht.
4Schreibe die zweistufige Protolyse von H2SO4 mit Wasser auf.
H2SO4 + H2O → HSO4− + H3O+
HSO4− + H2O ⇌ SO42− + H3O+
(Stufe 1 vollständig, Stufe 2 unvollständig)5Berechne die Stoffmenge H2SO4 in 100 ml konz. Schwefelsäure (ρ = 1,84 g/ml; w = 98 %; M = 98 g/mol).
m(Lösung) = 100 ml · 1,84 g/ml = 184 g
m(H2SO4) = 184 g · 0,98 = 180,3 g
n = 180,3 g ÷ 98 g/mol ≈ 1,84 molWeiter im Kapitel Gleichgewichtsreaktionen
← Calciumhydroxid-Gleichgewicht → Modellexperiment: Stechheberversuch
🔁 Verwandte Seiten: Merkmale eines chemischen Gleichgewichts · Prinzip von Le Chatelier · Brønsted-Definition (Kl. 9)
-
2.6 Phenole
2.6 Phenole = Hydroxybenzole
Vorkommen:
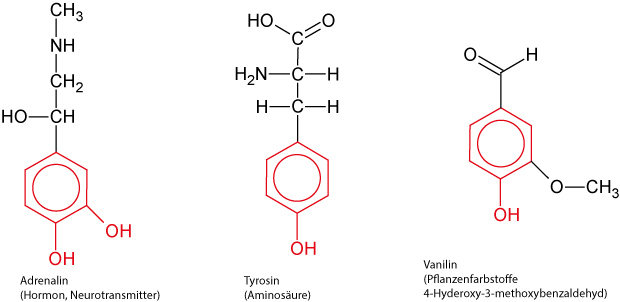
2.6.1 Monohydroxybenzol = Phenol
a) Physikalische Eigenschaften
- Smp.: 40,9; Sdp.: 181,9 °C
- In Wasser nur mäßig löslich (bildet bei ZT eine Emulsion)
- Starkes Zellgift, durch Haut resorbiert
b) Chemische Eigenschaften
- Oxidiert an Luft leicht ⇨ rötliche Färbung
- Karbolsäure“: 2 %ige Säure; Desinfektion
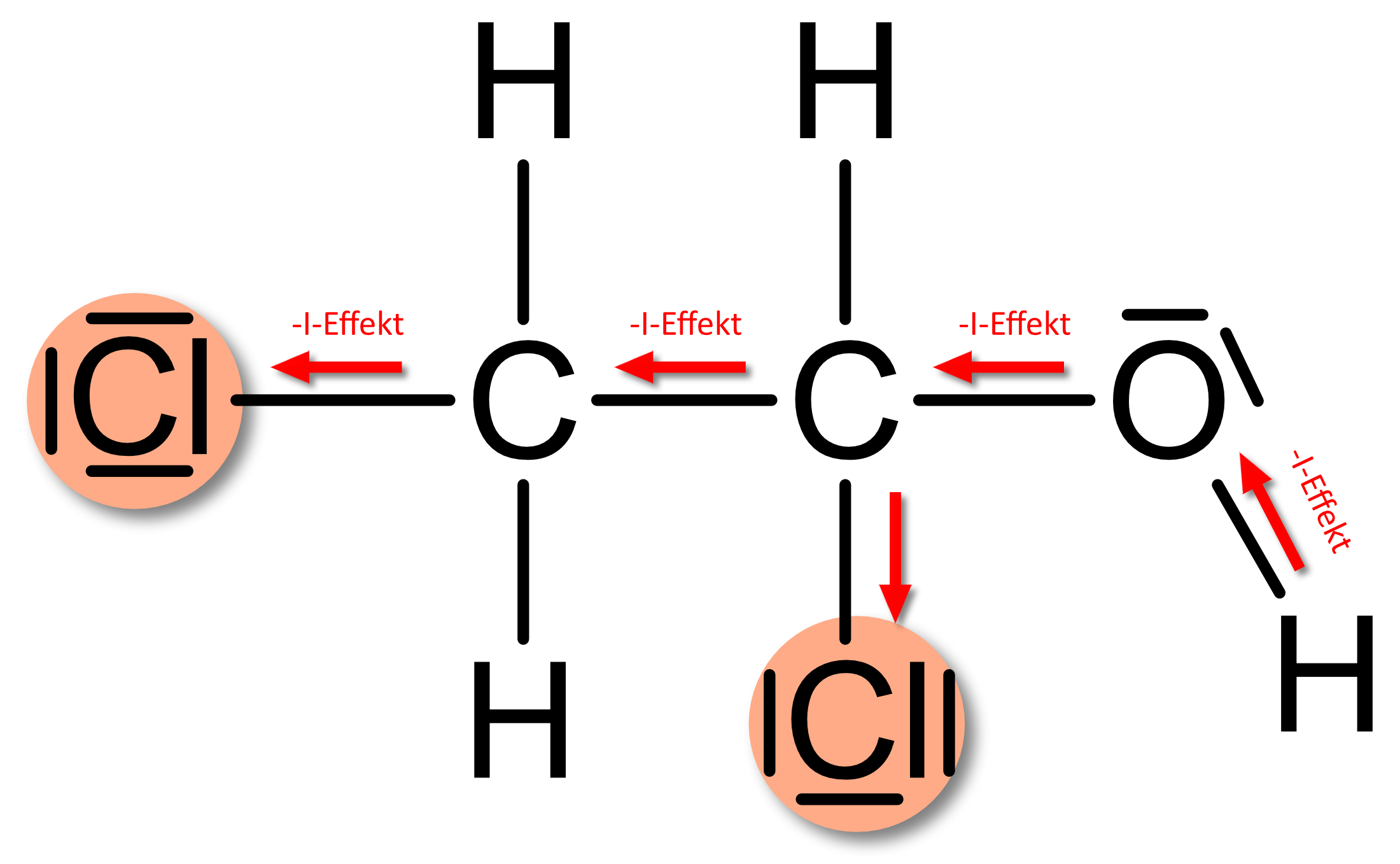
- Im Gegensatz zu Ethanol sauer:
1. Phenol als schwache Säure
pKS = 9,95
Grenzformeln des Phenolations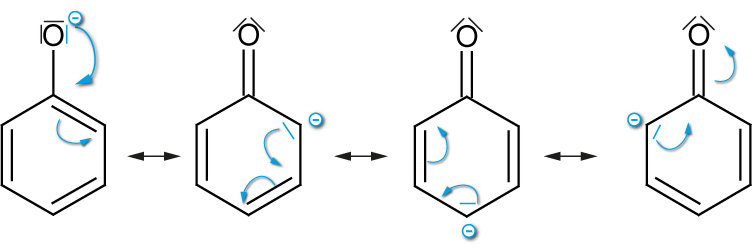
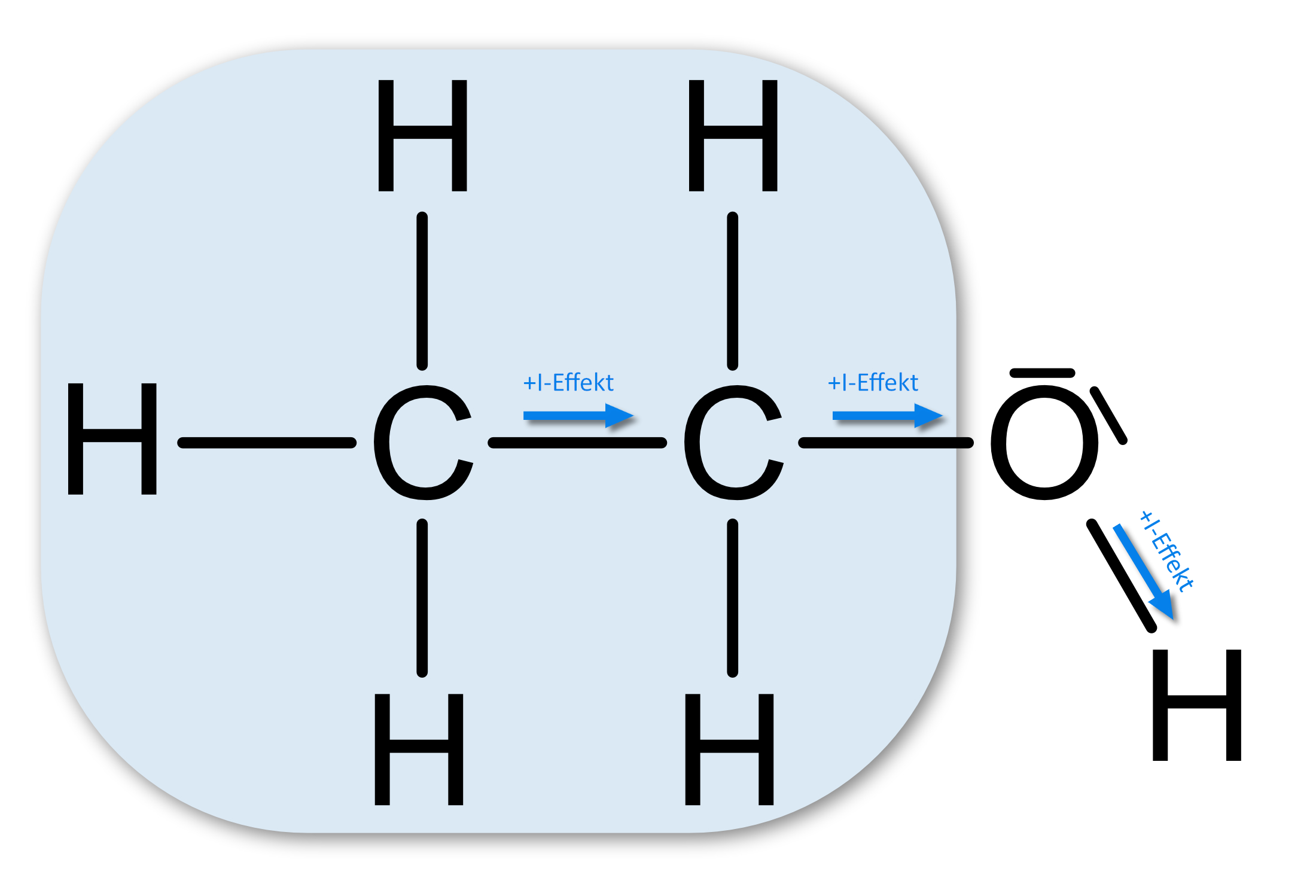
Phenol Ethanol Säurestärke höher niedriger Induktiver Effekt 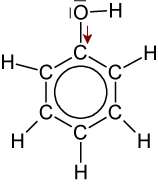
schwacher -I-Effekt ⇨ elektronenziehend
⇨ H⁺-Abgabe ist erleichtert
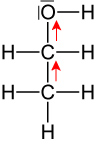
+I-Effekt ⇨ Elektro-nenschiebend
H⁺-Abgabe ist er-schwert.Anion: Mesomeriestabilisiert konjungierte Base (Phenolat): negative Ladung ist über den ganzen Ring delokalisiert ⇨ stabilisiert! Keine Stabilisierung durch Mesomerien Brønsted-Säure stärker schwächer Brønsted-Base schwächer stärker 2.6.3 Synthese
90% der Weltproduktion nach der Hock-Synthese
Wirtschaftliches Verfahren, da auch Aceton nutzbar ist.
siehe Heftaufschrieb
2.6.4 Verwendung
Herstellung von Kunststoffen (Polyamide, Phenoplasten, Phenolharzen und Polycarbonaten)
-
2.9 Säure-Base-Reaktion mit Benzoesäure
Was du auf dieser Seite lernst
Am Beispiel der Benzoesäure lernst du, wie chemische Gleichgewichte in der Säure-Base-Chemie konkret aussehen. Du verstehst, warum schwache Säuren nicht vollständig reagieren, warum Benzoesäure sich kaum in Wasser löst – und wie die Zugabe einer starken Base oder starken Säure das Gleichgewicht vollständig auf eine Seite verschiebt.
Grundlagen aus der 9. Klasse
Die Grundlagen zu Säure-Base-Reaktionen hast du bereits in der 9. Klasse kennengelernt: → Säure-Base-Definition nach Brønsted (Kl. 9) · → Stärke von Säuren und Basen (Kl. 9)
2.8 Allgemeines Zahlenbeispiel
A + B ⇌ C + D Vorher 1000 1000 0 0 Nachher 1000 − X 1000 − X X X z.B. im GG 800 800 200 200 2.9 Säure-Base-Reaktionen mit Benzoesäure
↑ Zum Vergrößern klicken
✕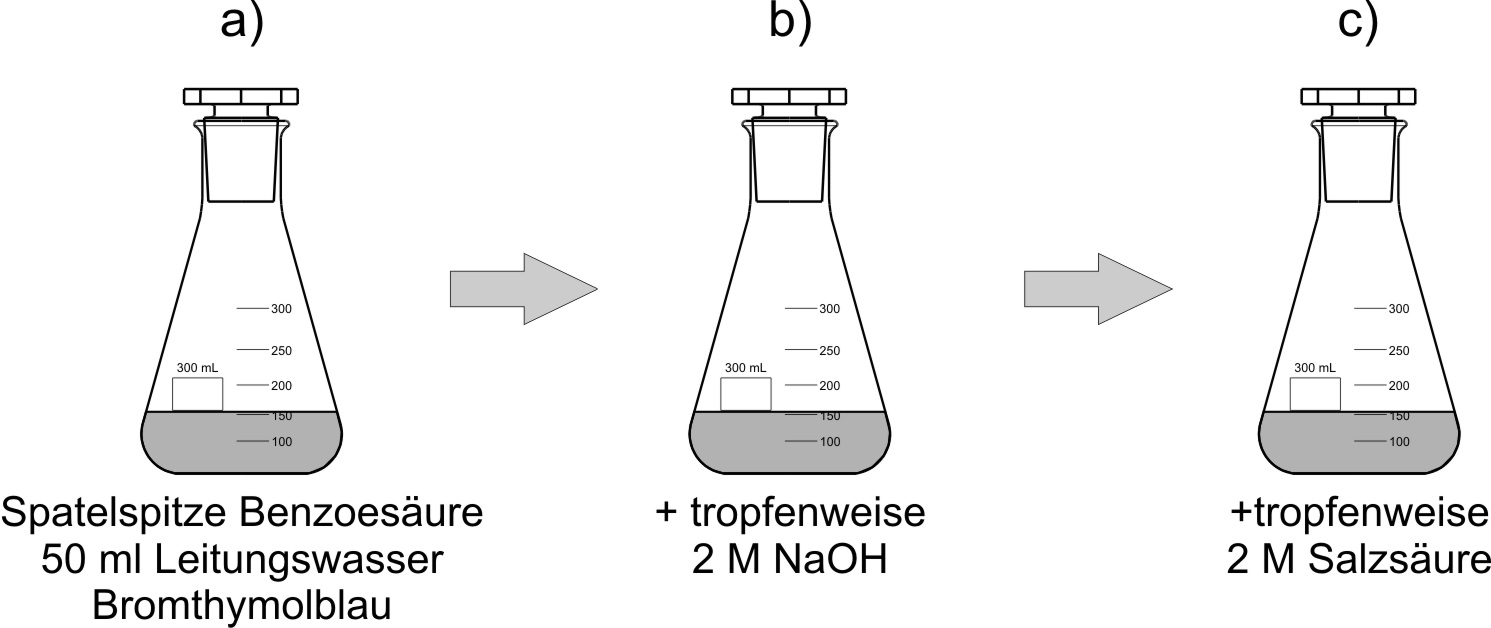
a) Benzoesäure + Wasser
Man gibt feste Benzoesäure in Wasser. Dabei beobachtet man, dass die Benzoesäure als weiße Substanz oben auf dem Wasser schwimmt. Auch mit Schütteln löst sie sich nicht auf.
Frage: Warum löst sich Benzoesäure nicht in Wasser? Dafür muss man sich einmal Benzoesäure anschauen (Hinweis: Benzoesäure ist noch vereinfacht „falsch" geschrieben, da wir die Aromaten erst später genauer betrachten).
↑ Zum Vergrößern klicken
✕Erklärt, warum Benzoesäure nur schlecht in Wasser löslich ist!
✕Lösung: Löslichkeit der Benzoesäure
Bei Benzoesäure ist ein großer Teil unpolar (der Benzolring). Der polare Teil (die –COOH-Gruppe) ist kleiner. Die Benzoesäure kann zwar mit Wasser H-Brücken ausbilden, aber der große unpolare Rest sorgt für eine schlechte Löslichkeit.
↑ Zum Vergrößern klicken
Hinweis: Ähnliches löst sich in Ähnlichem.
Zusammenfassung Beobachtung: wenig löslich in Wasser; die Lösung reagiert schwach sauer.
Formuliert die Reaktionsgleichung für die Reaktion von Benzoesäure mit Wasser mit bindenden und nichtbindenden Elektronenpaaren (Hinweis: Benzoesäure ist jetzt schon etwas vereinfacht geschrieben, indem die H-Atome am Ring weggelassen wurden).
✕Lösung: Reaktionsgleichung Benzoesäure + Wasser
↑ Zum Vergrößern klicken
Es findet nur eine schwache Reaktion mit H2O statt. Es reagieren nur wenige Benzoesäuremoleküle. Das Gleichgewicht liegt links.

b) Benzoesäure + Natronlauge (Neutralisation)
Man gibt vorsichtig Natronlauge zu und schüttelt die Lösung, bis die Benzoesäure vollständig aufgelöst ist.
Beobachtung: Es entsteht eine klare Lösung.Formuliert hierfür auch wieder eine Reaktionsgleichung mit bindenden und nichtbindenden Elektronenpaaren.
✕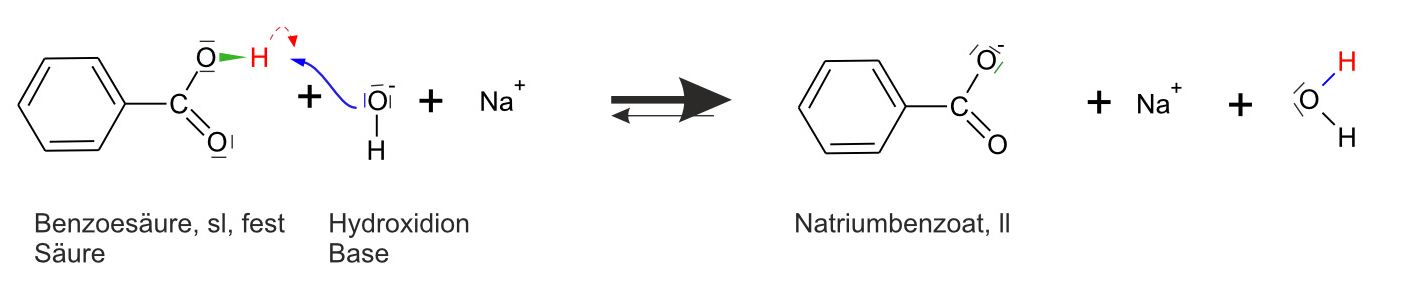
Die Benzoesäuremoleküle reagieren praktisch vollständig (das Gleichgewicht liegt weit auf der rechten Seite).
c) Gelöstes Natriumbenzoat + verd. Salzsäure
Die klare Natriumbenzoat-Lösung wird mit verdünnter Salzsäure versetzt.
✕
Beobachtung: Die klare Lösung wird trübe. Eine weiße, pulverartige Substanz schwimmt wieder auf der Oberfläche.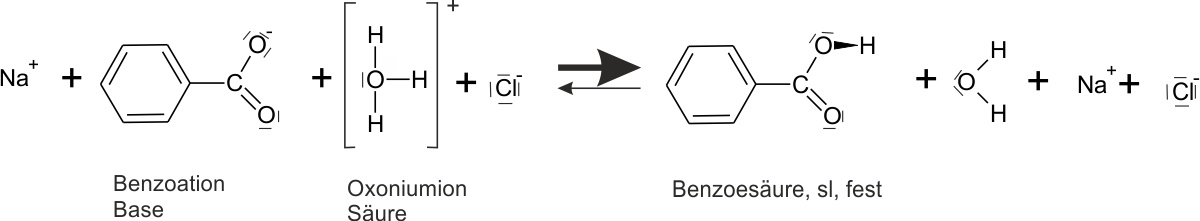
Feste Benzoesäure scheidet sich ab; die Benzoat-Anionen reagieren praktisch vollständig.
Auf einen Blick – die wichtigsten Aussagen
SCHWACHE SÄURE
Benzoesäure ist eine schwache Säure: das Gleichgewicht mit Wasser liegt links – es reagieren nur wenige Moleküle.
LÖSLICHKEIT
Der große unpolare Benzolring überwiegt die polare –COOH-Gruppe: Benzoesäure ist deshalb wenig wasserlöslich.
STARKE BASE
Natronlauge (starke Base) lässt Benzoesäure vollständig reagieren → klare Natriumbenzoat-Lösung entsteht.
STARKE SÄURE
Salzsäure (starke Säure) verdrängt Benzoesäure aus dem Benzoat-Salz → weißer Feststoff fällt wieder aus.
Häufige Fragen – Benzoesäure-Gleichgewicht
Warum löst sich Benzoesäure kaum in Wasser?
Benzoesäure besteht aus einem großen unpolaren Benzolring und einer kleineren polaren Carboxylgruppe (–COOH). Da „Ähnliches Ähnliches löst", ist der unpolare Anteil so dominant, dass die Wasserlöslichkeit sehr gering bleibt – obwohl die –COOH-Gruppe H-Brücken zu Wasser ausbilden kann. Mehr zur Struktur von Benzol und seinen Derivaten: → Aromaten (Kursstufe).
Warum liegt das Gleichgewicht von Benzoesäure + Wasser auf der linken Seite?
Benzoesäure ist eine schwache Säure: Sie gibt Protonen nur in geringem Umfang an Wasser ab. Im Gleichgewicht überwiegen daher die Edukte (undissoziierte Benzoesäure + Wasser) gegenüber den Produkten (Benzoat-Ion + Hydronium-Ion). Man sagt: das Gleichgewicht liegt links. Ein kleiner Kc-Wert (Ks ≈ 6,3 · 10−5) bestätigt das. Grundlagen zur Gleichgewichtslage: → Merkmale eines chemischen Gleichgewichts.
Was geschieht, wenn man Benzoesäure mit Natronlauge versetzt?
Natronlauge enthält OH−-Ionen (eine starke Base). Diese reagieren mit der Benzoesäure vollständig zu Natriumbenzoat (C6H5COO− Na+) und Wasser. Das Benzoat-Ion ist gut wasserlöslich → die zuvor trübe Suspension wird klar. Diese vollständige Reaktion ist möglich, weil NaOH eine viel stärkere Base ist als Wasser. Verwandte Grundlagen: → Neutralisation (Kl. 9).
Was passiert beim Ansäuern von Natriumbenzoat-Lösung mit Salzsäure?
Salzsäure (HCl) ist eine starke Säure und gibt bereitwillig Protonen an das Benzoat-Ion ab. Dabei wird Benzoesäure zurückgebildet, die sich wegen ihrer geringen Wasserlöslichkeit sofort als weißer Feststoff abscheidet (Lösung wird trüb). Stärkere Säuren verdrängen schwächere Säuren aus ihren Salzen – ein direktes Anwendungsbeispiel des Stärke-Prinzips von Säuren und Basen (Kl. 9).
Wie berechnet man Kc für das allgemeine Zahlenbeispiel A + B ⇌ C + D?
Im Zahlenbeispiel liegen im Gleichgewicht vor: A = 800, B = 800, C = 200, D = 200 (gleiche Einheit, z. B. mmol/L). Das Massenwirkungsgesetz ergibt:
Kc = [C] · [D] / ([A] · [B]) = 200 · 200 / (800 · 800) = 40.000 / 640.000 ≈ 0,0625
Ein Kc < 1 zeigt: die Edukte überwiegen im Gleichgewicht (Gleichgewicht liegt links). Mehr dazu: → Massenwirkungsgesetz (MWG).
Lernkarten – Benzoesäure-Gleichgewicht
Klicke auf eine Karte, um die Antwort zu sehen.
1Was versteht man unter einer schwachen Säure – und wo liegt ihr Gleichgewicht?
Eine schwache Säure gibt Protonen nur in geringem Umfang ab. Das Gleichgewicht liegt auf der Seite der Edukte (undissoziierte Säure überwiegt). Ks ist klein (≪ 1).
2Warum ist Benzoesäure nur wenig in Wasser löslich?
Der große unpolare Benzolring überwiegt die polare –COOH-Gruppe. Da ähnliches ähnliches löst, bleibt Benzoesäure in Wasser weitgehend unlöslich.
3Was beobachtet man beim Zugeben von Natronlauge zur Benzoesäure-Suspension?
Die trübe Suspension wird klar. Benzoesäure reagiert vollständig mit OH− zu gut löslichem Natriumbenzoat. Die starke Base verschiebt das Gleichgewicht vollständig nach rechts.
4Was passiert, wenn man Natriumbenzoat-Lösung mit verdünnter Salzsäure ansäuert?
Die klare Lösung wird trübe: Benzoesäure wird zurückgebildet und fällt als weißer Feststoff aus. HCl (starke Säure) verdrängt Benzoesäure (schwache Säure) aus ihrem Salz.
5Rechenaufgabe: A + B ⇌ C + D. Im GG: [A] = [B] = 0,80 mol/L, [C] = [D] = 0,20 mol/L. Berechne Kc und gib die Gleichgewichtslage an.
Kc = (0,20 · 0,20) / (0,80 · 0,80) = 0,04 / 0,64 ≈ 0,0625
Kc < 1 → Gleichgewicht liegt links (Edukte überwiegen).Weiter im Kapitel Gleichgewichtsreaktionen
← 2.6/2.7 Schreibweise und Kollisionsmodell → 2.10 Verschiebung des Gleichgewichts
← 2.5 Estergleichgewicht → 2.12 Massenwirkungsgesetz
🔁 Grundlagen: Brønsted-Definition (Kl. 9) · Stärke von Säuren und Basen (Kl. 9) · Neutralisation (Kl. 9)
🔗 Weiterführend: Aromaten – Benzol und Derivate (Kursstufe) · Autoprotolyse und pH-Wert (Kursstufe)
-
3 Protolyse-Reaktionen
Was du auf dieser Seite lernst
Chlorwasserstoff-Gas (HCl) reagiert mit Wasser zu Oxonium- und Chlorid-Ionen – das ist eine Protolyse-Reaktion nach Brønsted. Du lernst den Springbrunnenversuch zu erklären, Reaktionsgleichungen in Summenformel- und Lewis-Schreibweise aufzustellen und das Protolysen-Schema (Bergab-Reaktion) zu lesen und anzuwenden.
3 Protolyse-Reaktionen
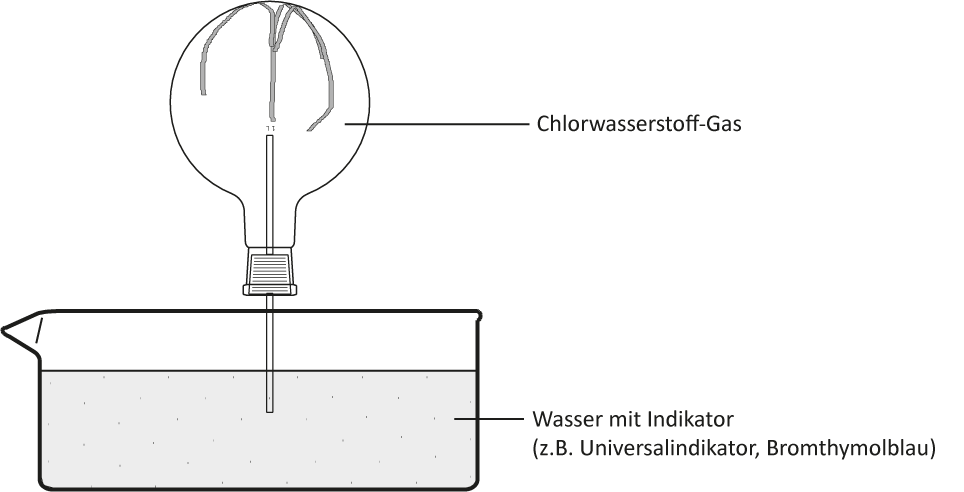
3.1 Chlorwasserstoff-Gas und Wasser (Springbrunnen)
Chlorwasserstoff: Summenformel HCl · polare Atombindung · Gas · stechender Geruch
Wasser: Summenformel H2O · polare Atombindung · Flüssigkeit · geruchslos✕Lewis-Formeln
H — Cl: Chlorwasserstoff H — O: Wasser | H 
a) Versuch:
↑ Zum Vergrößern klicken
✕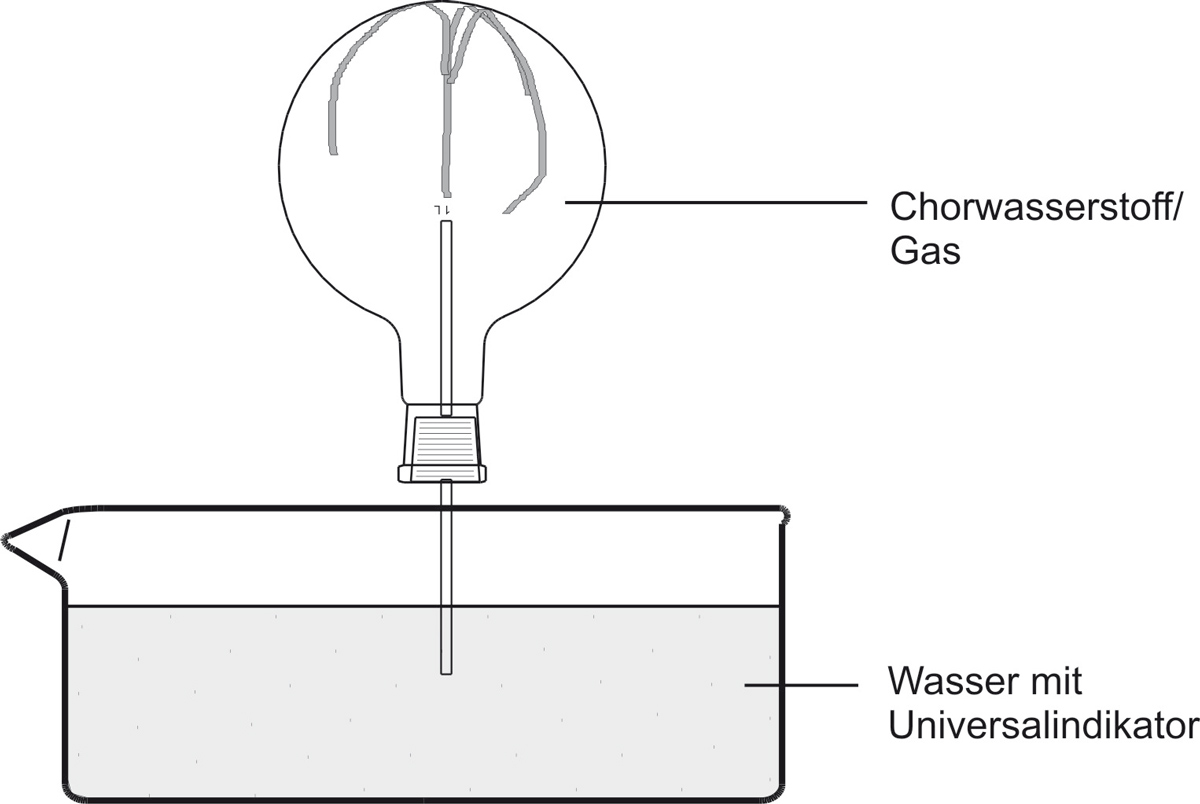
⚠️ Hinweis: Im Bild steht „Chorwasserstoff" – korrekte Schreibweise: Chlorwasserstoff.
b) Beobachtung:
Das Wasser „schießt" bergauf in den Rundkolben. Die Indikatorfarbe schlägt nach rot/gelb um. Die rote wässrige Lösung ist geruchlos.c) Reaktionsgleichung – Struktur/Lewisformel:
Es gibt zwei mögliche Reaktionsgleichungen (wenn man zunächst die Säurestärke vernachlässigt). Welche zwei Reaktionsgleichungen sind das?
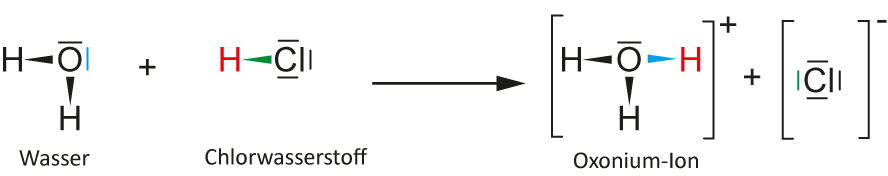
{slider title="Lösung" open="false" class="icon"}1. Möglichkeit – HCl als Säure, H2O als Base (korrekte Reaktion):
✕H2O(l) + HCl(g) ⟶ H3O+(aq) + Cl−(aq)
Wasser Chlorwasserstoff Oxonium-Ion Chlorid-Ion
⇒ bildet zusammen: „Salzsäure"

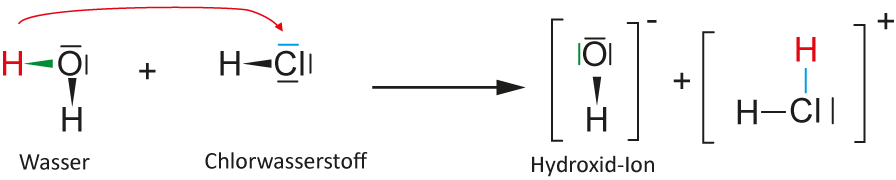
2. Möglichkeit – H2O als Säure, HCl als Base:
↑ Zum Vergrößern klicken
✕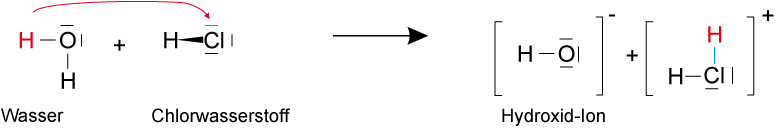
Chlorwasserstoff ist die stärkere Säure, Hydroxid-Ion (OH−) wäre eine sehr starke Base. Durch Elektrolyse wird die 1. Möglichkeit bestätigt: HCl wirkt als Säure.
{/sliders}Nachweis der gebildeten Ionen:
- Leitfähigkeitsmessung: Die Lösung leitet elektrischen Strom → Ionen sind vorhanden.
- Elektrolyse: An der Anode (Pluspol) entsteht Cl2-Gas → Chlorid-Ionen (Cl−) müssen vorliegen.
↑ Zum Vergrößern klicken
✕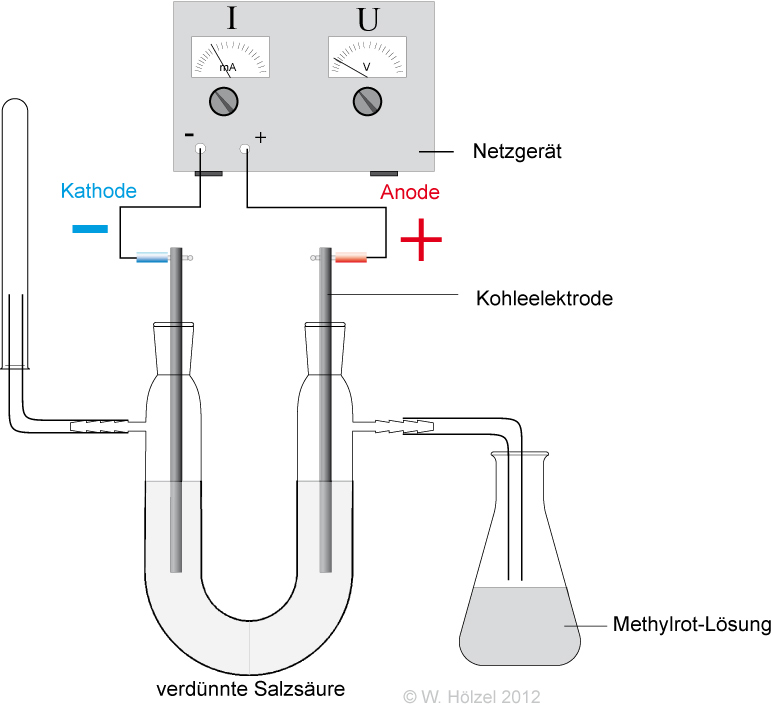
- Indikator: Bromthymolblau färbt gelb → Oxonium-Ionen (H3O+) sind vorhanden.
Komplette Lösung:
{slider title="Lösung" open="false" class="icon"}Reaktionsgleichung (Lewis-Formel):
↑ Zum Vergrößern klicken
✕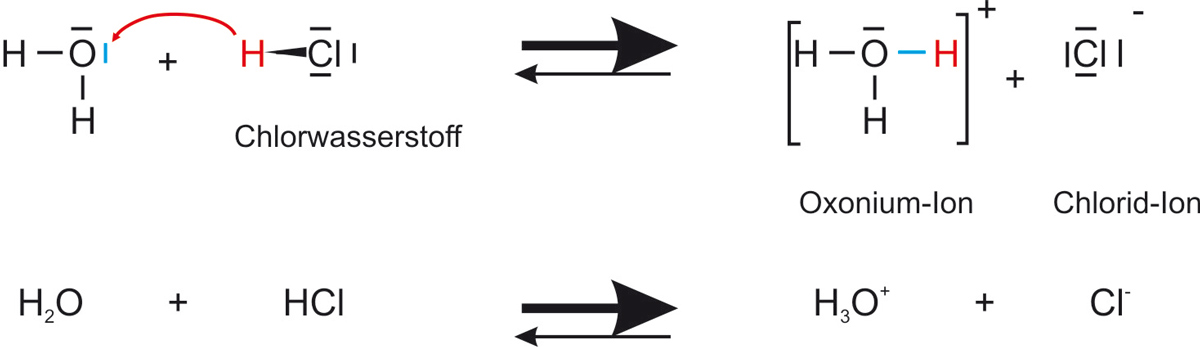
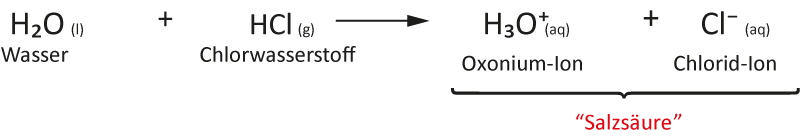
Reaktionsgleichung (Summenformel):
✕H2O(l) + HCl(g) ⇌ H3O+(aq) + Cl−(aq)
Wasser Chlorwasserstoff Oxonium-Ion Chlorid-Ion
„Salzsäure"

Verdünnte Salzsäure enthält hydratisierte Oxonium- und Chlorid-Ionen sowie Wassermolekule.
d) Protolysen-Schema:
↗ Originalbild des Protolysen-Schemas ansehen
✕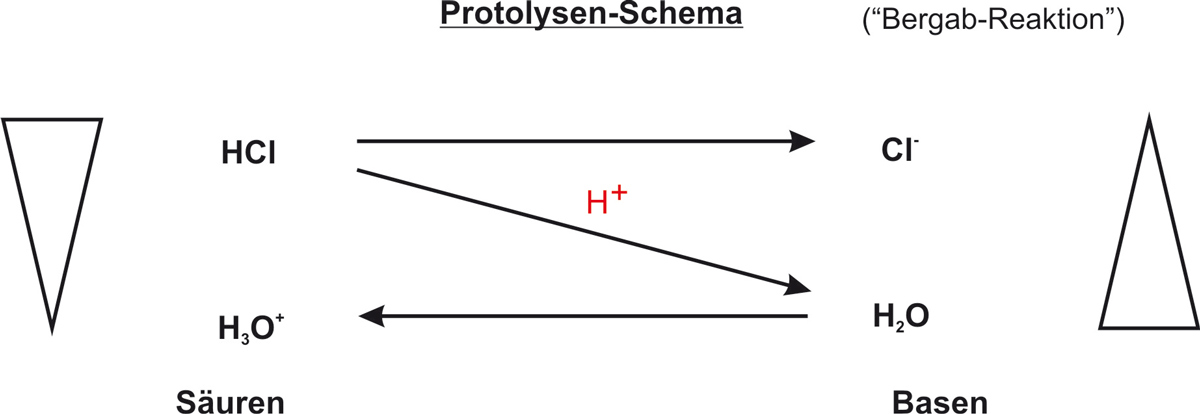 {/sliders}
{/sliders}
e) Erklärung:
Chlorwasserstoff-Gas reagiert mit Wasser zu Oxonium-Ionen (H3O+) und Chlorid-Ionen (Cl−). Im Kolben entsteht durch das vollständige Auflösen ein Unterdruck. Die H3O+-Ionen färben den Universalindikator bzw. Bromthymolblau rot/gelb.Salzsäure = wässrige Lösung des Gases Chlorwasserstoff
Leitet man sehr viel HCl-Gas in Wasser ein, reagieren nicht mehr alle HCl-Moleküle mit H2O. Diese HCl-Moleküle liegen „gelöst" vor – es entsteht rauchende bzw. konzentrierte Salzsäure.
Leitfähigkeit Geruch Indikatorpapier Teilchen Verdünnte Salzsäure + − rot H2O, H3O+, Cl− Rauchende Salzsäure + + rot H2O, H3O+, Cl−, HCl
Auf einen Blick – die wichtigsten Aussagen
Protolyse (Brønsted)
Eine Protolyse ist die Übertragung eines Protons (H+) vom Protonendonator (Säure) auf den Protonenakzeptor (Base).
Springbrunnen
HCl löst sich vollständig in H2O auf → Ionen bilden sich → Unterdruck entsteht → Atmosphärendruck drückt Wasser hoch.
Bergab-Reaktion
Das Proton wandert von der stärkeren Säure (HCl) zur stärkeren Base (H2O) – immer zur schwächeren Säure/Base hin.
Salzsäure
Salzsäure = wässrige Lösung von HCl. Enthält H3O+, Cl− und H2O; konzentriert zusätzlich gelöstes HCl.
Häufige Fragen – Protolyse-Reaktionen
Warum schießt das Wasser beim Springbrunnenversuch in den Kolben?
HCl-Gas reagiert sofort mit dem eingetretenen Wasser zu H3O+- und Cl−-Ionen. Dadurch sinkt der Gasdruck im Kolben stark. Der Atmosphärendruck drückt das Wasser durch das Glasrohr nach oben – der „Springbrunnen-Effekt". Die Indikatorfarbe zeigt: die Lösung ist sauer (H3O+-Ionen).
Was ist der Unterschied zwischen Chlorwasserstoff und Salzsäure?
Chlorwasserstoff (HCl) ist ein farbloses Gas mit stechendem Geruch. Salzsäure ist die wässrige Lösung dieses Gases: HCl löst sich in H2O und bildet dabei Oxonium-Ionen (H3O+) und Chlorid-Ionen (Cl−). Verdünnte Salzsäure ist geruchlos, da kein HCl mehr als Gas vorliegt.
Was versteht man unter einer Protolyse nach Brønsted?
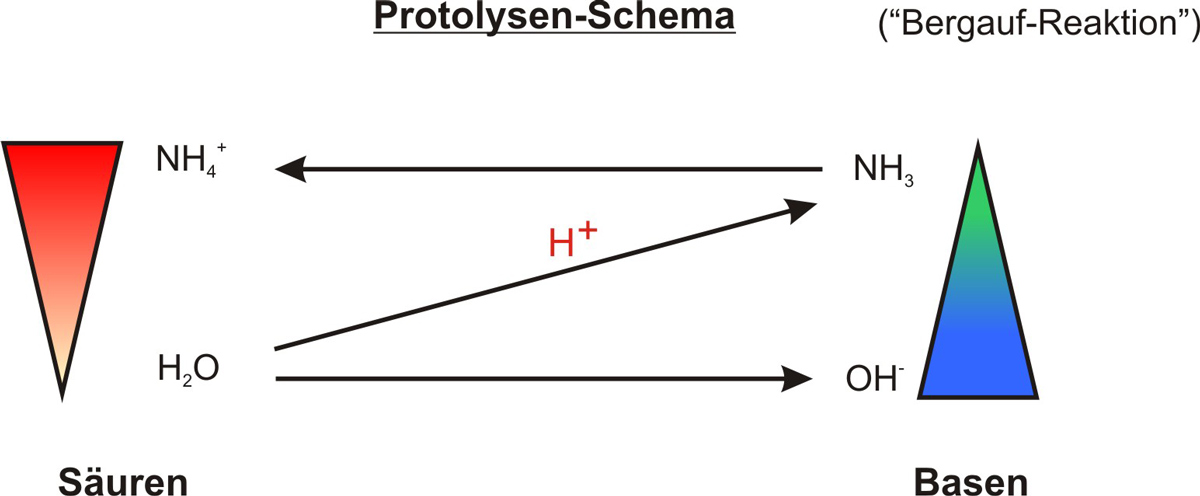
Nach Brønsted ist eine Säure ein Protonendonator (gibt H+ ab) und eine Base ein Protonenakzeptor (nimmt H+ auf). Eine Protolyse ist die Übertragung eines Protons. Das Protolysen-Schema zeigt: Die Reaktion läuft stets von der stärkeren Säure/Base zu den schwächeren Produkten – die sogenannte Bergab-Reaktion. Mehr dazu: Brønsted-Definition (Kl. 9).
Wie weist man Chlorid-Ionen in Salzsäure nach?
Durch Elektrolyse: An der Anode (Pluspol) entwickelt sich Chlorgas (Cl2), das durch Oxidation von Cl− entsteht – direkter Nachweis. Außerdem fällt bei Zugabe von Silbernitrat-Lösung (AgNO3) ein weißer Niederschlag aus Silberchlorid (AgCl) aus.
Was enthält rauchende Salzsäure im Vergleich zu verdünnter Salzsäure?
Verdünnte Salzsäure enthält nur H2O, H3O+ und Cl− – alles HCl hat mit Wasser reagiert. In konzentrierter (rauchender) Salzsäure ist so viel HCl gelöst, dass nicht mehr alle Moleküle mit H2O reagieren können. Sie liegen als undissoziiertes HCl vor → stechender Geruch, „Rauchen" an feuchter Luft. Mehr zur Konzentration: Konzentration von Lösungen (Kl. 9).
Lernkarten – Protolyse von Chlorwasserstoff
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist eine Protolyse-Reaktion nach Brønsted?
Übertragung eines Protons (H+) vom Protonendonator (Säure) auf den Protonenakzeptor (Base).
2Erkläre den Springbrunnenversuch mit HCl!
HCl löst sich schnell in H2O → Ionenbildung → Gasdruck sinkt → Atmosphärendruck drückt Wasser nach oben in den Kolben.
3Warum wirkt HCl als Säure und H2O als Base?
HCl ist die stärkere Säure. Im Protolysen-Schema reagiert immer die stärkere Säure mit der stärkeren Base (Bergab-Reaktion).
4Welche Teilchen enthält verdünnte vs. rauchende Salzsäure?
Verdünnt: H2O, H3O+, Cl−
Rauchend: zusätzlich gelöstes HCl → stechender Geruch5Berechne: Welche Masse HCl (M = 36,5 g/mol) steckt in 250 mL 0,2-mol/L-Salzsäure?
n = c · V = 0,2 mol/L · 0,25 L = 0,05 mol
m = n · M = 0,05 mol · 36,5 g/mol = 1,825 gWeiter im Kapitel Säure-Base-Reaktionen
→ 3.2 Chlorwasserstoff und Ammoniak → Brønsted-Definition → Stärke von Säuren und Basen
🔗 Verwandte Themen: pH-Wert und Oxonium-Ionen · Konzentration von Lösungen · Neutralisation
ⓘ Die verlinkten Seiten wurden nicht gegen die aktuelle Sitemap verifiziert – bitte vor dem Veröffentlichen prüfen.
-
3.2 Ammoniak-Gas + Wasser
Was du auf dieser Seite lernst
Ammoniak ist ein Gas, das sich außergewöhnlich gut in Wasser löst – das zeigt der Springbrunnenversuch eindrucksvoll. Du lernst, wie Ammoniak mit Wasser nach der Brønsted-Theorie reagiert (Protolyse), warum dabei eine basische Lösung entsteht, und verstehst im Exkurs, warum Sprudelwasser sauer ist und wie man daraus den pH-Wert berechnet.
Grundlagen aus der 9. Klasse
Die Grundlagen zur Brønsted-Theorie (Protonendonator / Protonenakzeptor) hast du bereits in der 9. Klasse kennengelernt: → Brønsted-Theorie (Kl. 9) · → Säure-Base-Reaktionen (Kl. 9)
3.2 Ammoniak-Gas + Wasser (Springbrunnen 2)
a) Versuch
↑ Zum Vergrößern klicken
✕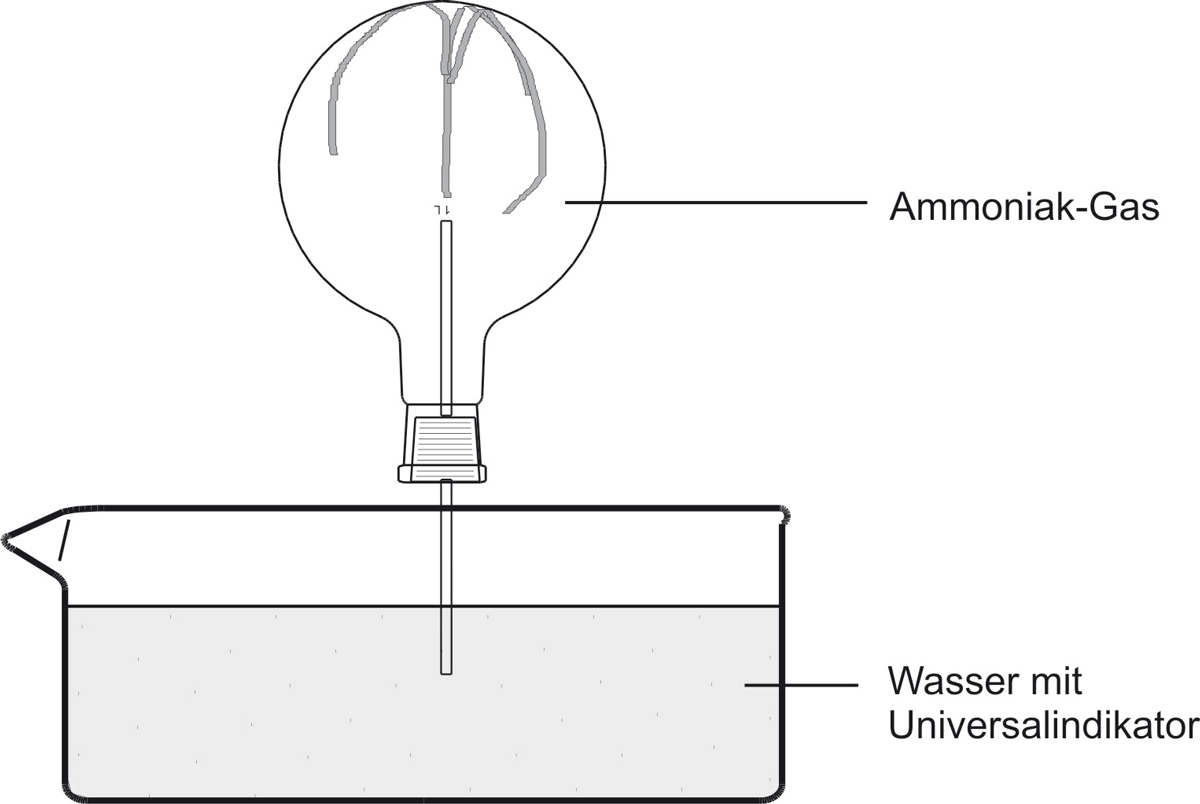
b) Beobachtung
Das Wasser „schießt" bergauf in den Rundkolben. Die Indikatorfarbe schlägt nach blau um. Die blaue wässrige Lösung riecht nach Ammoniak.
c) Erklärung
Ammoniak-Gas löst sich sehr gut in Wasser und reagiert teilweise mit Wasser. Im Kolben entsteht durch das Lösen des Gases ein starker Unterdruck. Die entstehenden Hydroxid-Ionen (OH⁻) färben den Universalindikator blau.
d) Reaktionsgleichung (mit Strukturformeln und Summenformeln)
Versuche die Gleichung erst selbst zu formulieren!
Formuliere nun das Protolyseschema:
Exkurs: Was macht den Sprudel sauer?
Kohlenstoffdioxid reagiert beim Lösen in Wasser im Gleichgewicht zu Kohlensäure:
CO₂ (g) + H₂O (l) ⇌ „H₂CO₃" (aq) – instabil (→ Erlenmeyer-Regel: zwei OH-Gruppen am selben C-Atom sind nicht beständig)
1. Protolysestufe: H₂CO₃ (aq) + H₂O (l) ⇌ HCO₃⁻ (aq) + H₃O⁺ (aq)
2. Protolysestufe: HCO₃⁻ (aq) + H₂O (l) ⇌ CO₃²⁻ (aq) + H₃O⁺ (aq)
Nachweis der H₃O⁺-Ionen durch:
- Geschmack (sauer)
- pH-Papier
- pH-Meter
Messwert: pH(Sprudel) = 5,1
Berechnung der Oxoniumionen-Konzentration:
pH = −lg c(H₃O⁺)
c(H₃O⁺) = 10−pH = 10−5,1 ≈ 7,9 · 10−6 mol/L
Auf einen Blick – die wichtigsten Aussagen
Springbrunneneffekt
NH₃ löst sich so gut in Wasser, dass im Kolben ein starker Unterdruck entsteht – das Wasser „schießt" nach oben in den Rundkolben.
Protolyse (Brønsted)
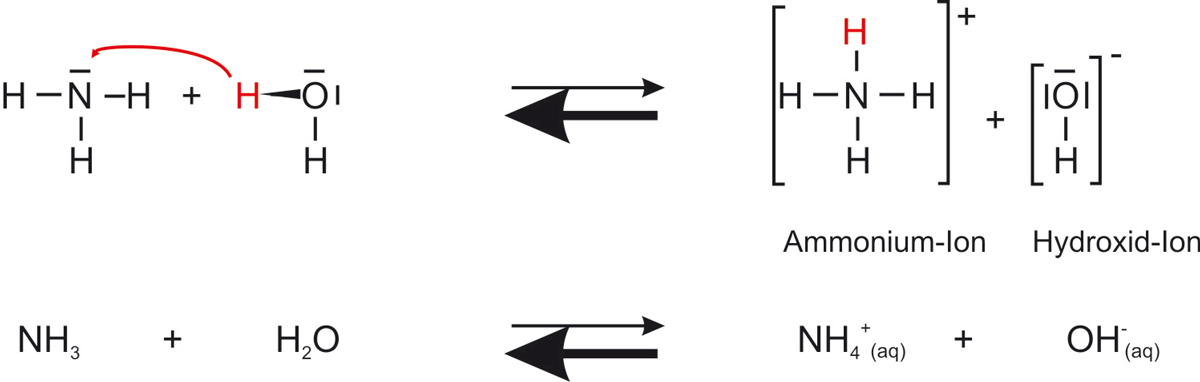
NH₃ + H₂O ⇌ NH₄⁺ + OH⁻. NH₃ ist Protonenakzeptor (Base), H₂O ist Protonendonator (Säure). Lösung basisch (pH > 7).
Erlenmeyer-Regel
H₂CO₃ ist instabil – zwei OH-Gruppen am selben C-Atom sind nicht beständig. H₂CO₃ zerfällt sofort in CO₂ und H₂O.
pH-Rechnung
pH = −lg c(H₃O⁺) · c(H₃O⁺) = 10−pH
Sprudel: pH 5,1 → c(H₃O⁺) ≈ 7,9 · 10−6 mol/LHäufige Fragen – Ammoniak und Wasser
Warum steigt beim Springbrunnenversuch das Wasser von selbst auf?
Ammoniak löst sich außergewöhnlich gut in Wasser (ca. 700 Liter NH₃ in 1 Liter Wasser bei Raumtemperatur). Sobald Wasser mit dem Ammoniak-Gas in Berührung kommt, löst sich das Gas nahezu vollständig. Der Gasdruck im Kolben fällt schlagartig ab – es entsteht ein starker Unterdruck. Der Atmosphärendruck drückt daraufhin das Wasser durch die Glasspitze nach oben in den Kolben.
Ist NH₃ in Wasser eine Säure oder eine Base?
Nach Brønsted ist NH₃ eine Base: Es nimmt ein Proton (H⁺) vom Wasser auf und bildet das Ammoniumion NH₄⁺. Gleichzeitig gibt Wasser ein Proton ab und wird zur konjugierten Base OH⁻. Die Reaktion verläuft als Gleichgewicht:
NH₃ (aq) + H₂O (l) ⇌ NH₄⁺ (aq) + OH⁻ (aq)
Da OH⁻-Ionen entstehen, ist die Lösung basisch (pH > 7), was der Universalindikator durch Blaufärbung anzeigt.Was bedeutet „konjugiertes Säure-Base-Paar"?
Ein konjugiertes Säure-Base-Paar unterscheidet sich nur um ein Proton H⁺. Bei der Ammoniak-Protolyse gibt es zwei solche Paare:
- NH₄⁺ / NH₃ – NH₄⁺ ist die Säure, NH₃ die konjugierte Base
- H₂O / OH⁻ – H₂O ist die Säure, OH⁻ die konjugierte Base
Das Protolyseschema stellt diese Paare mit Pfeilen dar und zeigt, in welche Richtung das Proton wandert. Mehr dazu auf der Seite → Brønsted-Theorie.
Was ist die Erlenmeyer-Regel und wozu braucht man sie?
Die Erlenmeyer-Regel besagt: Verbindungen, bei denen zwei Hydroxyl-Gruppen (OH) an demselben Kohlenstoffatom gebunden sind, sind instabil und wandeln sich spontan um. Kohlensäure H₂CO₃ hätte formal zwei OH-Gruppen am gleichen C-Atom – sie ist daher so instabil, dass sie sofort in CO₂ und H₂O zerfällt. Diese Regel erklärt, warum im Sprudelwasser kein stabiles H₂CO₃ vorliegt, sondern CO₂ im Gleichgewicht mit Wasser steht und dabei H₃O⁺-Ionen entstehen.
Wie berechnet man aus dem pH-Wert die Oxoniumionen-Konzentration?
Formel: pH = −lg c(H₃O⁺), umgestellt: c(H₃O⁺) = 10−pH
Beispiel Sprudel mit pH = 5,1:
c(H₃O⁺) = 10−5,1 ≈ 7,9 · 10−6 mol/LZum Vergleich: Reines Wasser hat c(H₃O⁺) = 10−7 mol/L (pH = 7). Weitere Berechnungen findest du auf der Seite → pH-Wert berechnen.
Lernkarten – Ammoniak und Wasser
Klicke auf eine Karte, um die Antwort zu sehen.
1Warum entsteht beim Springbrunnenversuch ein Unterdruck im Kolben?
NH₃ löst sich extrem gut in Wasser → Gas verschwindet aus der Gasphase → Druck sinkt → Unterdruck → Atmosphärendruck drückt Wasser nach oben.
2Formuliere die vollständige Protolysegleichung von NH₃ mit Wasser.
NH₃ (aq) + H₂O (l) ⇌ NH₄⁺ (aq) + OH⁻ (aq)
NH₃ = Base (Protonenakzeptor)
H₂O = Säure (Protonendonator)3Nenne die beiden konjugierten Säure-Base-Paare bei der Ammoniak-Protolyse.
Paar 1: NH₄⁺ (Säure) / NH₃ (Base)
Paar 2: H₂O (Säure) / OH⁻ (Base)4Warum ist Sprudelwasser sauer, obwohl H₂CO₃ instabil ist?
CO₂ reagiert im Gleichgewicht mit H₂O. Auch ohne stabiles H₂CO₃ entstehen durch Protolyse H₃O⁺-Ionen (Erlenmeyer-Regel) → saure Lösung (pH ≈ 5,1).
5Berechne: Ein Sprudel hat pH = 4,5. Wie groß ist c(H₃O⁺)?
c(H₃O⁺) = 10−pH = 10−4,5 ≈ 3,2 · 10−5 mol/L
Weiter im Kapitel Säure-Base-Reaktionen
← 3 Protolyse-Reaktionen (Übersicht) → 3.3 Neutralisation
🔁 Grundlagen (Kl. 9): Säure-Base-Reaktionen (Kl. 9) · Brønsted-Theorie (Kl. 9) · Neutralisation (Kl. 9)
📈 Vertiefung: pH-Wert berechnen · pKB-Wert (Basestärke) · Pufferlösung
-
4 Allgemeine Säure-Base-Definition nach Brønsted (1923)
4 Allgemeine Säure-Base-Definition nach Brønsted (1923)
a) Säuren...
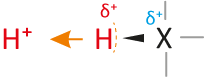
... sind Teilchen, die Protonen abgeben können (= Protonendonator, „Protonenspender“).
Die Teilchen enthalten positivierte H-Atome (Die Bindung zum H-Atom muss polar sein):Wasserstoffatome bestehen nur aus Protonen und Elektronen. Eine Säure besitzt ein Wasserstoffatom, wobei das Elektron von dem Wasserstoffatom „stark“ angezogen wird. Kommt es zu einer Säure-Base-Reaktion (Protolyse), dann wird vereinfacht ausgedrückt nur das Proton des Wasserstoffatoms abgegeben. Das Elektron der Wasserstoffatoms bleibt beim Teilchen zurück (vgl. dazu alle vorher genannten Beispiele).
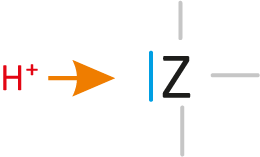
b) Basen...sind Teilchen, die Protonen aufnehmen können (= Protonenakzeptor, „Protonenräuber“). Die Teilchen enthalten mindestens ein freies Elektronenpaar.
Dieses freie Elektronenpaar „nimmt“ dann den positiven Wasserstoffkern (Proton) „auf“.
c) Übung
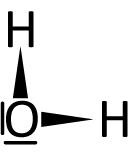
Im folgenden ist die Lewis-Formel (Strukturformel) von Wasser abgebildet. Gehört dieses Molekül zu einer Brønsted-Säure oder -Base? Schaut Euch dafür nochmals die Definitionen an.
{slider title="Lösung: Was ist Wasser? Eine Säure oder Base?" open="false" class="icon"}
Wasser kann (je nach Reaktionspartner) beides sein. Es kann ein Proton (H⁺) abgeben [es hat ja positivierte Wasserstoff-Atome], wie auch aufnehmen [es hat ja auch freie Elektronenpaare].
Dafür gibt es eine neue Bezeichnung: Wasser ist ein Ampholyt.
{/sliders}
c) Ampholyte
Ampholyte können sowohl als Säuren, wie auch als Basen reagieren. Sie müssen also freie Elektronenpaare (für die Funktion als Basen) wie auch positivierte Wasserstoff-Atome (Funktion als Säure) besitzen.
-
5 Stärke von Säuren und Basen
5 Stärke von Säuren und Basen - Säurestärke und Molekülstruktur
Hinweis 1: Das Kapitel stammt aus dem Oberstufenbereich. Ich halte es für das Verständnis für Säure-Base-Reaktionen wichtig, weil man sonst bei einer Reaktion mit zwei Ampholyten (z.B. Wasser und Ammoniak) gar nicht weiß, wer die Säure ist und wer als Base funktioniert.
Hinweis 2: Auch hier ist es von Vorteil, wenn man ein Periodensystem der Elemente zur Hand hat.
Brønsted-Theorie:
Säurestärke ist die Tendenz Protonen abzugeben.
Basenstärke Tendenz Protonen aufzunehmen.Bsp. HCl + H₂O → H₃O⁺ + Cl⁻
Säure 1 Base 2 Säure 2 Base 1Info: Supersäuren = Säuren die stärker als H₂SO₄ sind.
Je stärker die Säure desto schwächer die konjugierte (korrespondierende) Base.
5.1 Binäre Säuren.
Faktoren für Säurestärke von Bedeutung:
- Elektronegativität (innerhalb einer Periode)
- Atomgröße (innerhalb einer Gruppe)
a) innerhalb einer Periode (binäre H-Verbindungen)
Säurestärke nimmt mit der EN zu (Atomgrößenunterschiede sind „zu“ gering)
⇨ Elektronen werden stärker dem H-Atom entzogen ⇨ erleichterte Protonenabspaltung.Bsp.:
2. Periode:
Zunahme der EN: N < O < F
Zunahme der Säurestärke NH₃ < H₂O < HF
Gegenüber Wasser Base Säure
3. Periode
Zunahme der EN: P < S < Cl
Zunahme der Säurestärke PH₃ < H₂S < HCl
b) innerhalb einer Gruppe (binäre H-Verbindungen):
Säurestärke nimmt mit der Atomgröße zu (stärkere Auswirkung als Elektronegativität)
⇨ bei einem großen Atom ist die Valenzelektronenwolke auf einem größeren Raum verteilt ⇨ H⁺ ist weniger fest gebunden.H₂O < H₂S < H₂Se < H₂Te
HF < HCl < HBr < HI5.2 Oxosäuren
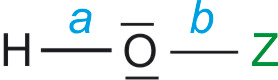
Sauerstoff hat in etwa die gleiche Größe
a) EN von Z ist entscheidend.
Je größer die EN von Z, desto stärker ist die Säure (-I-Effekt).HOI < HOBr < HOCl
hyopoiodige Säure hypobromige hypochlorige Säureb) An Z sind weitere O-Atome gebunden ⇨ stärkerer –I-Effekt (bzw. höhere Formalladung am Z. )

hypochlorige – chlorige – Chlor – Perchlorsäuren
⇨ Man kann Säurestärke abschätzen: Je mehr mehr O-Atome an das Z-Atom jedoch nicht an H-Atom gebunden sind, desto die Säure:
H-O-NO < H-O-NO₂
salpetrige Säure Salpetersäure
(H-O-)₂SO < (H-O-)₂SO₂
schweflige Säure Schwefelsäure -
5.1.5 Induktiver Effekt
5.1.5 Induktiver Effekt (I-Effekt)
Ausschlaggebend: Elektronegativität (EN) der Substituenten (Atomgruppen, Atome die dranhängen). Dabei werden Elektronen über mehrere Bindungen angezogen oder „abgestoßen“.
Reichweite: 3 benachbarte Bindungen.
(-I)-Effekt (sprich: „minus I Effekt“; „negativer I Effekt“).• Substituenten (Atomgruppen) mit höherer Elektronegativität (Bsp.: Halogene, Sauerstoff-Verbindungen,...)• „Elektronenziehend“:
Ziehen Bindungselektronen zu sich
Auswirkung: z.B. Erleichterte Abspaltung eines Protons; Alkohol kann als Säure reagieren.
(+I)-Effekt (sprich: „plus I Effekt“; positiver I Effekt)Elektropositiveren Substituenten (Bsp.: Alkylgruppen). Je mehr bzw. je länger die Alkylgruppe, umso stärker ist der +-I-Effekt.
„Elektronenschiebend“:
Auswirkung: z.B. geringere Säurestärke
Keinen I-Effekt haben Wasserstoffatome.Auswirkung für das Experiment und Vergleich: Ethanol + Natrium und Wasser + Natrium
Bei diesem Experiment (siehe Seite zuvor) kommt es zu einer heftigeren Reaktion, wenn das Proton (vom Wasser oder Alkohol) leicht abgespalten wird. Je leichter es abgespalten wird, umso stärker ist ja auch seine Säure-Wirkung. Da Wasser keinen positiven induktiven Effekt hat (hat ja auch keine Alkylgruppe), reagiert es heftiger als Ethanol (positiver induktiver Effekt durch Alkylgruppe).
-
5.1.6 Aminosäure sind Ampholyte
5.1.6 Aminosäure sind Ampholyte
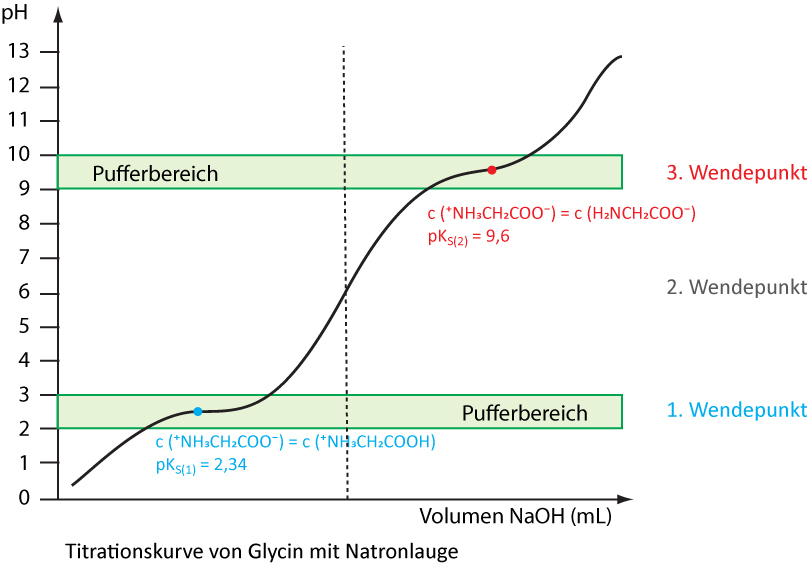
Aminosäuren können sowohl als Brønsted-Säuren als auch als Brønsted-Basen reagieren.
Die hinzugefügten Oxonium- und Hydroxid-Ionen werden abgefangen. Der pH-Wert verändert sich kaum. Aminosäuren besitzen Pufferwirkung.1. Wendepunkt
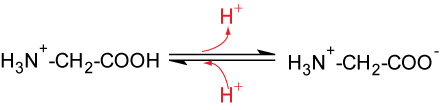
50 % 50 %
pKS1 = 2,34Für jede Aminosäure gibt es einen pH-Wert, bei dem sie im elektrischen Feld nicht wandert. Diesen pH-Wert bezeichnet man als isoelektrischen Punkt. Bei diesem Punkt liegen praktisch nur die Zwitterionen vor. Der isoelektrische Punkt bei Glycin liegt bei pH 6,0 (2. Wendepunkt).
3. Wendepunkt

50 % 50 %
pKS2 = 9,77 -
6 Chlorwasserstoff-Gas und Wasser
6 Chlorwasserstoff-Gas und Wasser (Springbrunnen)
Chlorwasserstoff: Summenformel HCl, polare Atombindung, Gas, stechender Geruch
Wasser: Summenformel H₂O, polare Atombindung, Flüssigkeit, geruchslos
a) Versuch:
b) Beobachtung:
Das Wasser „schießt“ bergauf in den Rundkolben. Die Indikatorfarbe schlägt nach rot/gelb um. Die rote wässrige Lösung ist geruchlos.c) Reaktionsgleichung – Struktur/Lewisformel:
Theoretisch gibt es zwei Möglichkeiten, wie Wasser und Chlorwasserstoff reagieren können.
- Formuliere einmal diese zwei Möglichkeiten als Reaktionsgleichung mit Strukturformeln.
- Entscheide, welche dieser beiden möglichen Reaktionen tatsächlich abläuft. Falls du nicht drauf kommst, gehe zurück zum Thema: Säure-Stärke
{slider title="Lösung" open="false" class="icon"}
1. Möglichkeit:
2. Möglichkeit:
Chlorwasserstoff ist die stärkere Säure, da Chlor ein größeres Atom ist, als Wasserstoff. Außerdem ist das Hydroxid-Ion ist eine sehr starke Base.
{/sliders}
Nachweis der gebildeten Ionen:
- Leitfähigkeitsmessung
- durch Elektrolyse: An der Anode (+-Pol) entsteht dabei Cl₂-Gas. Somit müssen in der verdünnten Salzsäure Chlorid-Ionen (Cl⁻-Ionen) vorliegen.
- durch Indikator: Die Gelbfärbung bei Bromthymolblau zeigt Oxonium-Ionen (H₃O⁺) an.
Reaktionsgleichung Zusammenfassung
{slider title="Lösung" open="false" class="icon"}
Begründung:
Chlor (vom Chlorwasserstoff) ist ein größeres Atom als Sauerstoff (vom Wasser). Deshalb ist Chlorwasserstoff eine stärkere Säure und gibt das Proton (H⁺) und Wasser nimmt das Proton auf.
verdünnte Salzsäure enthält hydratisierte Oxonium- und Chlorid-Ionen und Wassermoleküle.{/sliders}
Verdünnte Salzsäure enthält hydratisierte Oxonium- und Chlorid-Ionen und Wassermoleküle.
d) ProtolyseschemaFormuliere für diese Reaktion einmal das Protolyseschema:
{slider title="Lösung" open="false" class="icon"}
{/sliders}
e) Erklärung:
Chlorwasserstoff-Gas reagiert mit Wasser. Im Zylinder entsteht ein Unterdruck. Die Oxonium-Ionen färben den Universalindikator/Bromthymolblau rot/gelb.Salzsäure: = wässrige Lösung des Gases Chlorwasserstoff Wenn man sehr viel HCl-Gas in Wasser einleitet, reagieren nicht mehr alle HCl-Moleküle mit den H₂O-Molekülen. Diese HCl-Moleküle liegen „gelöst“ vor. Es ist so „rauchende“ bzw. konzentrierte Salzsäure entstanden.
Leitfähigkeit Geruch Indikatorpapier Teilchen verdünnte Salzsäure + - rot H₂O, H₃O⁺, Cl⁻ rauchende Salzsäure + + rot H₂O, H₃O⁺, Cl⁻, HCl -
9 Bildung von Calciumhydroxid
9 Bildung von Calciumhydroxid aus Calciumoxid und Wasser
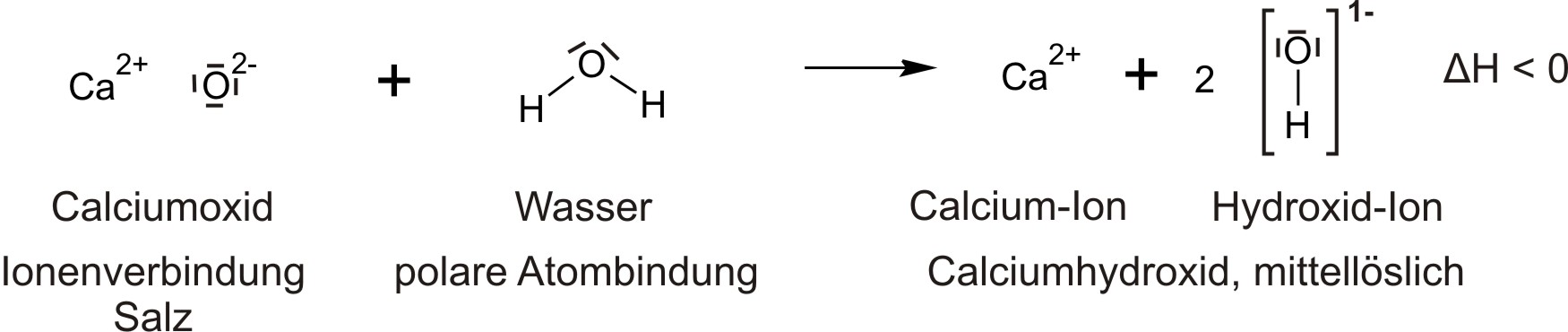
a) Bildung von Calciumhydroxid („Löschen von gebranntem Kalk“)
Hierfür wird in einem Experiment etwas Calcium(II)-Oxid in ein Reagenzglas gegeben und wenige Wasser zugetropft.
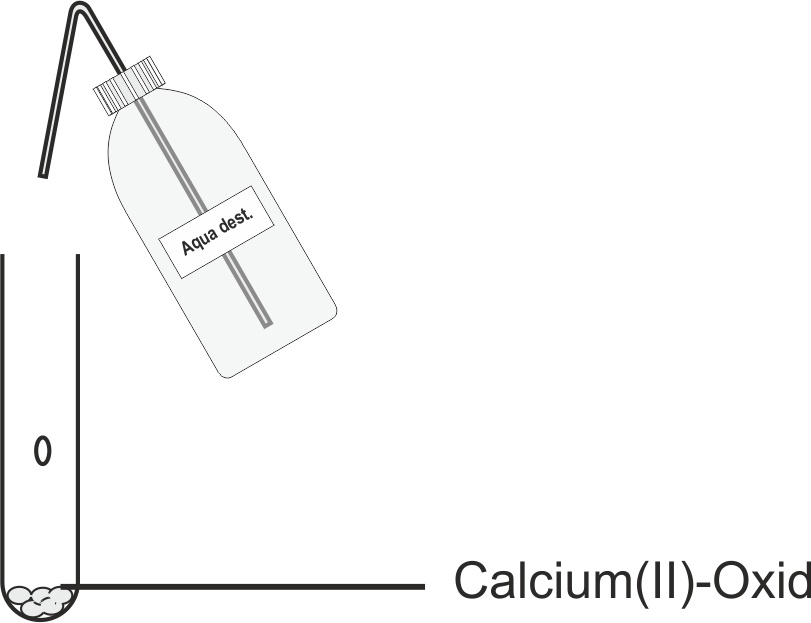
Beobachtung: Das Reagenzglas wird sehr heiß! Es ist also eine freiwillige, exotherme Reaktion.
Aufgabe: Formuliert die Reaktionsgleichung mit Hilfe von Strukturformeln (formuliert hierfür auch die Teilchen als Ionen). Zeichnet dann auch noch eine Protolyse-Schema für dies Reaktion mit den Teilchen, die bei dieser Reaktion beteiligt sind.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
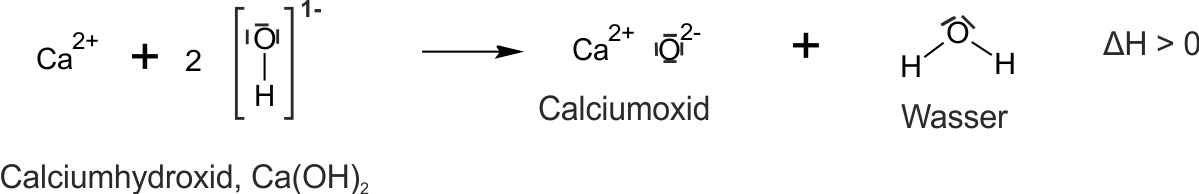
b) Erhitzen von Calciumhydroxid
Die oben genannte Reaktion kann man aber auch Umkehren. Da die Bildung von Calciumhydroxid freiwillige und exotherm verläuft muss die Umkehrung natürlich unter Zwang und endotherm (also Energie in Wärme muss in das System hingesteckt werden) verlaufen.
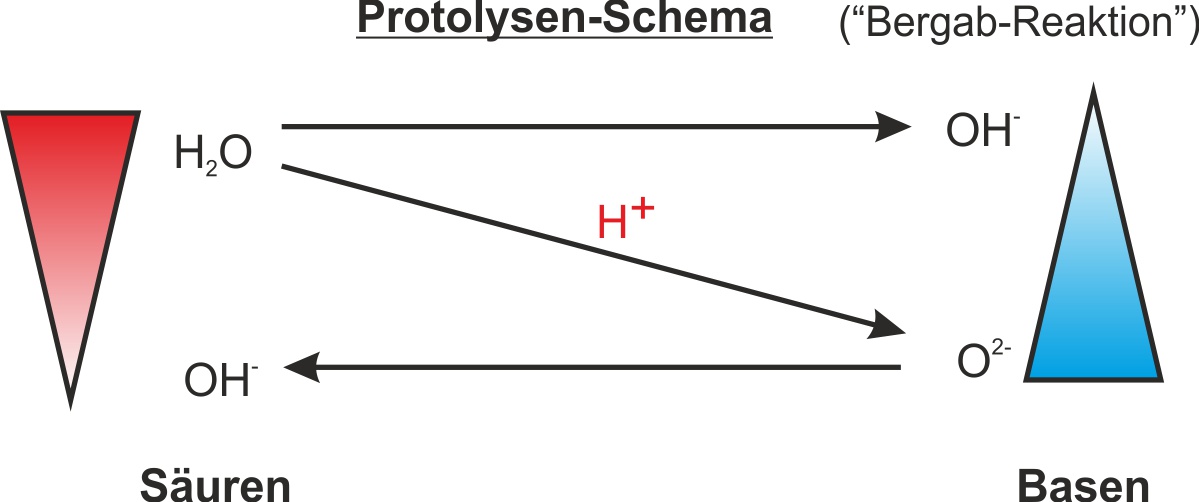
Aufgabe: Formuliert für die Umkehrung dieser Reaktion auch eine Reaktionsgleichung mit Hilfe von Strukturformeln und ein Protolyse-Schema. Wichtig für das Schema ist, dass die Säuren immer links stehen, die starke Säure oben links und die starke Base unten rechts. Außerdem zeigt der diagonale Pfeil an, ob eine Reaktion freiwillig ("bergab" = von oben nach unten) oder unfreiwillig ("bergauf" = von unten nach oben) verläuft.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
-
Säure-Base-Reaktionen
Säure-Base-Reaktionen (=Protolyse-Reaktionen)
1 Reaktion von Chlorwasserstoffgas mit festem Natriumhydroxid
2 Reaktion von Chlorwasserstoff-Gas mit Ammoniak-Gas
3 Reaktion von festem Ammoniumchlorid und festem Natriumhydroxid
4 Allgemeine Säure-Base-Definition nach Brønsted (1923)
5 Stärke von Säuren und Basen
6 Chlorwasserstoff-Gas und Wasser (Springbrunnen)
7 Konzentration
8 Neutralisationsreaktion
9 Reaktion von verdünnter Salzsäure mit verdünnter Natronlauge
10 Reaktion von Calciumoxid mit Wasser
(x) Ammoniak-Gas + Wasser (Springbrunnen 2)
11 Technisch wichtige Säuren
11.1 Schwefelsäure
11.2 Schweflige Säure