Gleichgewichtsreaktionen
-
02 Gleichgewichte
2 Gleichgewichte
2.1 Schwefelsäure – Wasserdampf – Gleichgewicht
a) konzentrierte Schwefelsäure (H2SO4)
- enthält Schwefelsäuremoleküle
- zeichnet einmal die Strukturformel(n) (unter Berücksichtigung, dass die Edelgas-Regel erfüllt sein muss):
{slider title="Lösung" open="false" class="icon"}
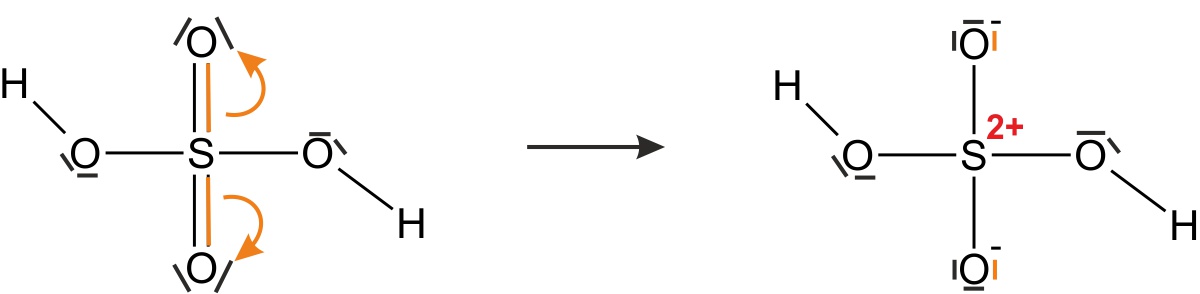
{/sliders}
- Konzentrierte Schwefelsäure ist geruchlos;
- Siedetemperatur beträgt 300°C;
- Konzentrierte Schwefelsäure reagiert heftig mit Wasser und Ionenbildung (Protolyse-Reaktion)
Formuliert für die Reaktion der Schwefelsäure mit Wasser in zwei Stufen die Reaktionsgleichung in Summenformeln
{slider title="Lösung" open="false" class="icon"}
H2SO4 + H2O → HSO4- + H3O+
HSO4- + H2O → SO42- + H3O+{/sliders}
b) Verdünnte Schwefelsäure
Verdünnte Schwefelsäure enthält folgende Ionen und Moleküle; nennt diese:{slider title="Lösung" open="false" class="icon"}
- H3O+ (Oxonium-Ion; früher Hydronium-Ion oder „Hydroxonium-Ion“)
- HSO4- (Hydrogensulft-Ion)
- SO42- (Sulfat-Ion; wenig)
- H2O Enthält viele Wassermoleküle
{/sliders}
2.2 Langzeitversuch: Konzentrierte SchwefelsäureVersuchsdurchführung: In einen Zylinder 1 werden 100 ml konzentrierte Schwefelsäure gegeben. In einen Zylinder 2 werden zunächst 900 ml Wasser und dann vorsichtig 100 ml konzentrierte Schwefelsäure gegeben. Beide Zylinder werden mehrere Jahre offen im gleichen Zimmer stehengelassen.
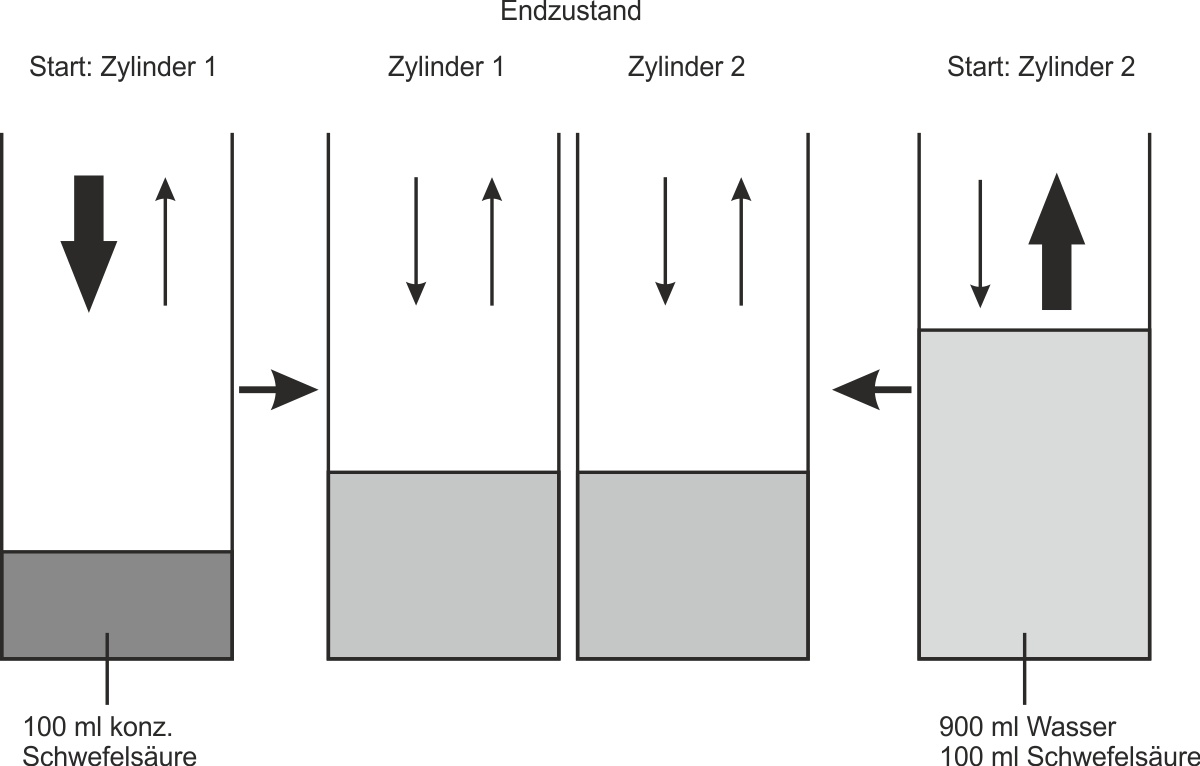
Versucht eine Deutung dieses Versuches:
{slider title="Lösung" open="false" class="icon"}
• Zylinder 1 nimmt mehr H2O -Moleküle aus der Umgebung auf als er abgibt.
• Zylinder 2 gibt mehr H2O -Moleküle an die Umgebung ab, als er aufnimmt.
• Nach einigen Jahren hat sich ein Gleichgewichtszustand eingestellt: Pro Zeiteinheit werden nun gleich viel H2O-Moleküle an die Umgebung abgegeben wie H2O-Moleküle in die Lösung hinzukommen.
{/sliders}
-
2.10 Verschiebung des Gleichgewichts
2.10 Verschiebung des Gleichgewichts
Die Lage des GG ergibt sich aus dem Zusammenwirken von Hinreaktion und Rückreaktion. Das GG verschiebt sich, wenn beide Reaktionen verschieden stark geändert werden.
Das ist häufig der Fall bei einer Änderung von
- Konzentration (Konzentration = Stoffmenge/Volumen)
- Temperatur
- Druck
2.10.1 Änderung der Konzentration und Temperatur
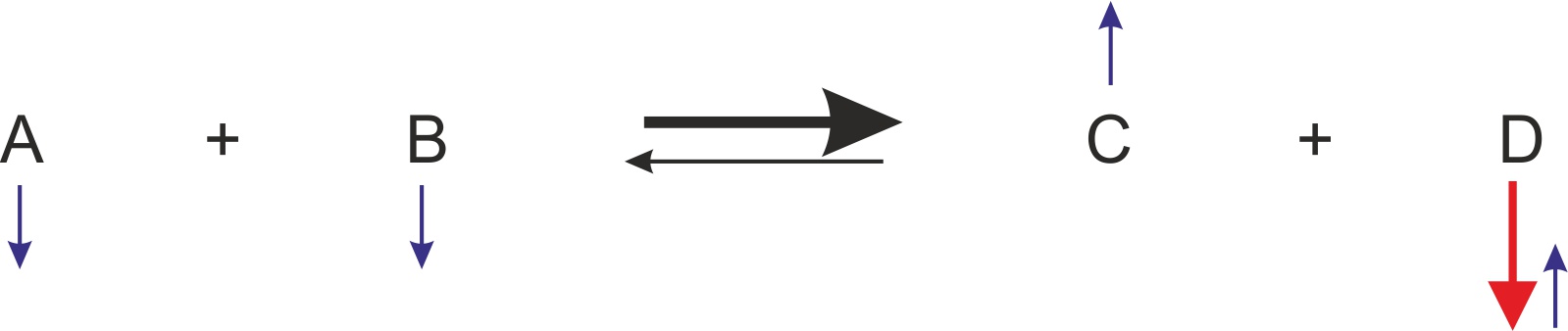
α) einmaliger Zusatz von Stoff D
Es erfolgen mehr Rückreaktionen (Wichtig, das über das Kollisionsmodell zu verstehen: durch mehr Teilchen wird häufiger ein Zusammenstoß zwischen C und D erfolgen); dadurch stellt sich ein neues Gleichgewicht ein. Man sagt: „Das GG wird nach links verschoben.“Roter Pfeil: Zugabe von dem Stoff D -> Stoff D kollidiert häufiger mit C und reagieren miteinander. Dadurch werden es etwas weniger Stoffe C und D (blaue Pfeile auf der Produktseite); gleichzeit entstehen etwas mehr Stoffe A und B. Bitte immer dran denken, bei einem Gleichgewicht gibt es immer alle Stoffe; hier also gibt es gleichzeitig A, B, C und D!. Man kann sich das relativ schnell veranschaulichen, wenn man bei einer Reaktionsgleichung die Pfeile reinschreibt.
β) einmalige Wegnahme von Stoff DJetzt seid ihr dran. Wie ändert sich das GG, wenn man einmalig den Stoff D wegnimmt. Macht eine analoge Reaktionsgleichung mit Pfeilen wie oben.
{slider title="Lösung" open="false" class="icon"}
Es erfolgen mehr Hinreaktionen; dadurch stellt sich ein neues Gleichgewicht ein. Man sagt: „Das GG wird nach rechts verschoben.“
{/sliders}
γ) dauernde Wegnahme von Stoff D (z.B. als Gas)
Wie ändert sich bei dauerhaften Wegnahme das GG, wenn der Stoff D, der entsteht, permanent aus dem System verdampft?
{slider title="Lösung" open="false" class="icon"}
In einem offenen System kann sich kein Gleichgewicht einstellen; Die Reaktion läuft vollständig ab.

{/sliders}
Eisenrhodanit-Gleichgewicht
Vergleich dazu Arbeitsblatt zum Experiment.
Vereinfachte Reaktionsgleichung:

a) Das 1. RG bleibt unverändert und dient zum Vergleich!
b) Ein Spatellöffel NH4Cl (Ammoniumchlorid) wird in das Reagenzglas 2 gegeben.
Beobachtung: Die Lösung wird heller.Wie kann man das mit Hilfe des Verschiebung des Gleichgewichts deuten?
{slider title="Lösung" open="false" class="icon"}
Deutung: Das GG wird nach links verschoben{/sliders}
c) Ein Spatelspitze FeCl3 (Eisenchlorid) wird in das Reagenzglas 3 gegeben.
Nenne die mögliche Beobachtung und Deutung:
{slider title="Lösung" open="false" class="icon"}
Beobachtung: Die Lösung wird dunkelrot.
Deutung: Das GG wird nach rechts verschoben.{/sliders}
d) Ein Spatellöffel NH4 SCN (Ammoniumrhodanid = Ammoniumthiocyanat) wird in das Reagenzglas 4 gegeben.
{slider title="Lösung" open="false" class="icon"}
Beobachtung: Die Lösung wird dunkelrot.
Deutung: Das GG wird nach rechts verschoben{/sliders}
Ergebnis: Konzentrationserhöhung eines Reaktionspartners begünstigt die Reaktion, die diesen Stoff verbraucht. e) Reagenzglas 5 wird in heißes Wasser gestellt.
Beobachtung: Die Lösung wird heller
{slider title="Lösung" open="false" class="icon"}
Deutung: Das GG wird nach links verschoben{/sliders}
f) Reagenzglas 6 wird in Eiswasser gestellt
Überlegt, was jetzt die Beobachtung sein könnte:
{slider title="Lösung" open="false" class="icon"}
Beobachtung: Die Lösung wird dunkler.
Deutung: Das GG wird nach rechts verschoben{/sliders}
Ergebnis:
• Temperaturerhöhung begünstigt die endotherme Reaktion;
• Temperaturerniedrigung begünstigt die exotherme Reaktion.FeCl3 + 3 NH4SCN ⇌ Fe(SCN)3 + 3 NH4Cl ΔH<0
b) weitere BeispieleH2O (l) ⇌ H2O (g) ΔH=+41 kJ
flüssig gasförmigTemperaturerhöhung --> mehr Wasser verdampft.
2.10.2 Änderung des Drucks
a) Chlorethandampf - Chlorethanflüssigkeit (Kältespray); genau: Monochlorethan
C2H5Cl (g) ⇌ C2H5Cl (l)
α) Bei Druckerhöhung bilden sich im Kolbenprober Chlorethantröpfchen:
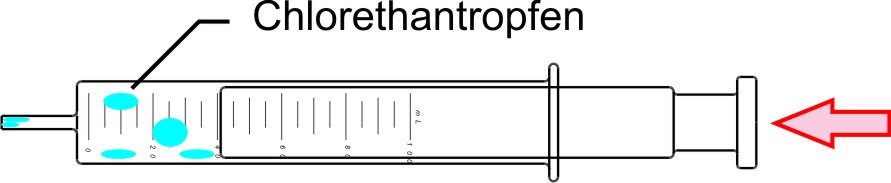
β) Bei Druckerniedrigung verschwinden diese Chlorethantröpfchen wieder.
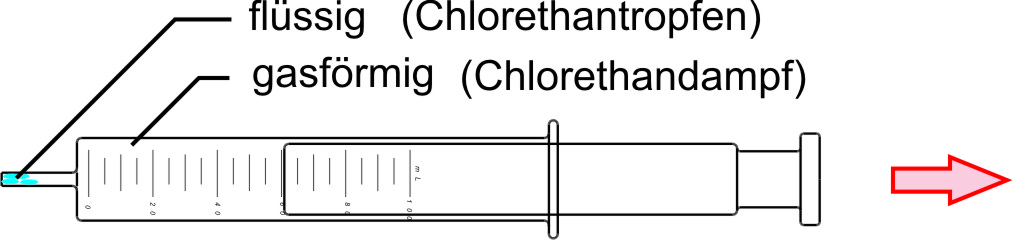
γ) Ergebnis:
• Druckerhöhung begünstigt die Reaktion mit Volumenabnahme.b) weitere Beispiele
H₂O (s) ⇌ H₂O (l)
Fest (solid) flüssig (liquid)Druckerhöhung verschiebt das Gleichgewicht nach rechts, Wasser wird flüssig.
Grund: flüssiges Wasser hat eine größere Dichte (kleineres Volumen) als Eis (Eis schwimmt).
-
2.3 Modellexperiment - Stechheberversuch
2.3 Modellexperiment - Stechheberversuch
Vergleiche dazu auch das ausgeteilte Arbeitsblatt zum Experiment.
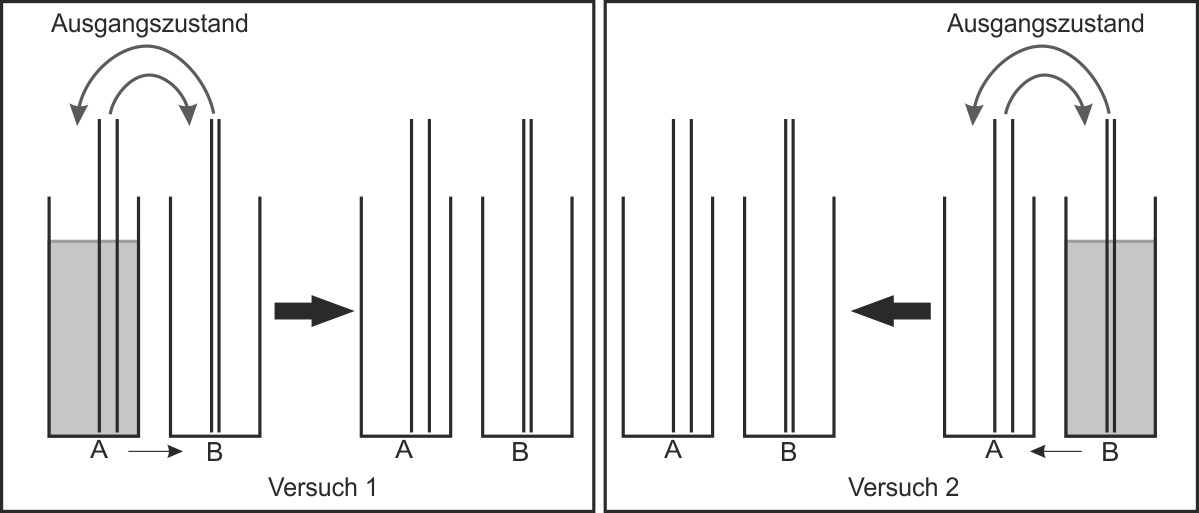
Versuch 1: Flüssigkeit gelangt von A nach B. Die reversible Reaktion setzt mit der „Hinreaktion“ ein.
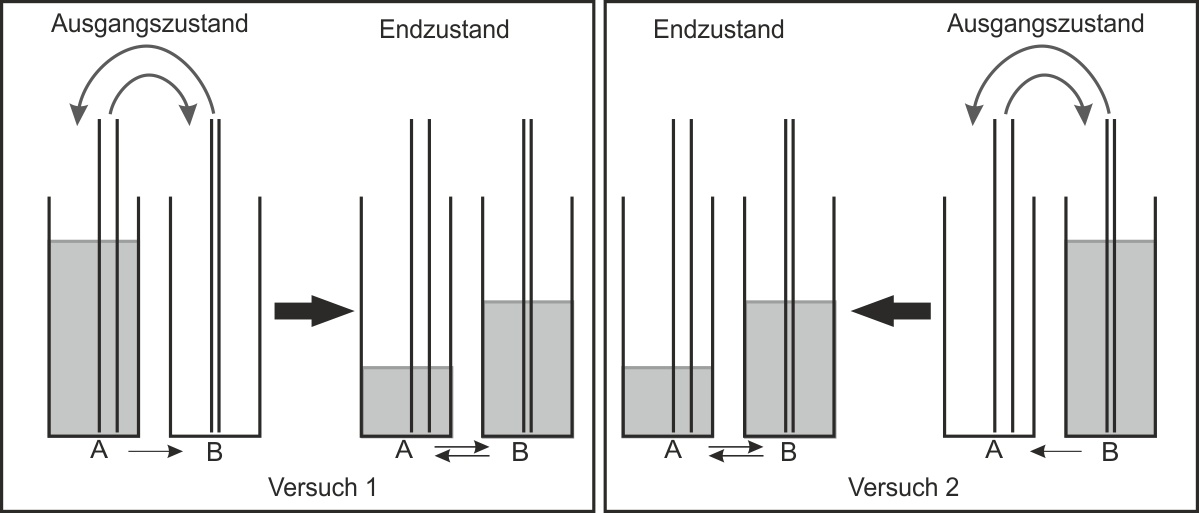
Anschließend gelangt auch Flüssigkeit von B zurück nach A. Es findet also auch eine „Rückreaktion“ statt. Nach einiger Zeit sind die in den Rohren im gleichen Takt beförderten Flüssigkeitsportionen gleich groß geworden.Wie könnten die Endzustände bei den Experimenten 1 und 2 ausschauen?
{slider title="Lösung" open="false" class="icon"}
Versuch 1 und 2 führen zum gleichen Ergebnis („Gleichgewichtszustand“)
{/sliders}
Was für ein Diagramm bekommt man, wenn man das Volumen in den Standzylindern gegen die Zeit aufträgt? Und wie sieht das Diagramm aus, wenn man das Volumen innerhalb der Pipetten/Glasrohre gegen die Zeit aufträgt?
{slider title="Lösung" open="false" class="icon"}
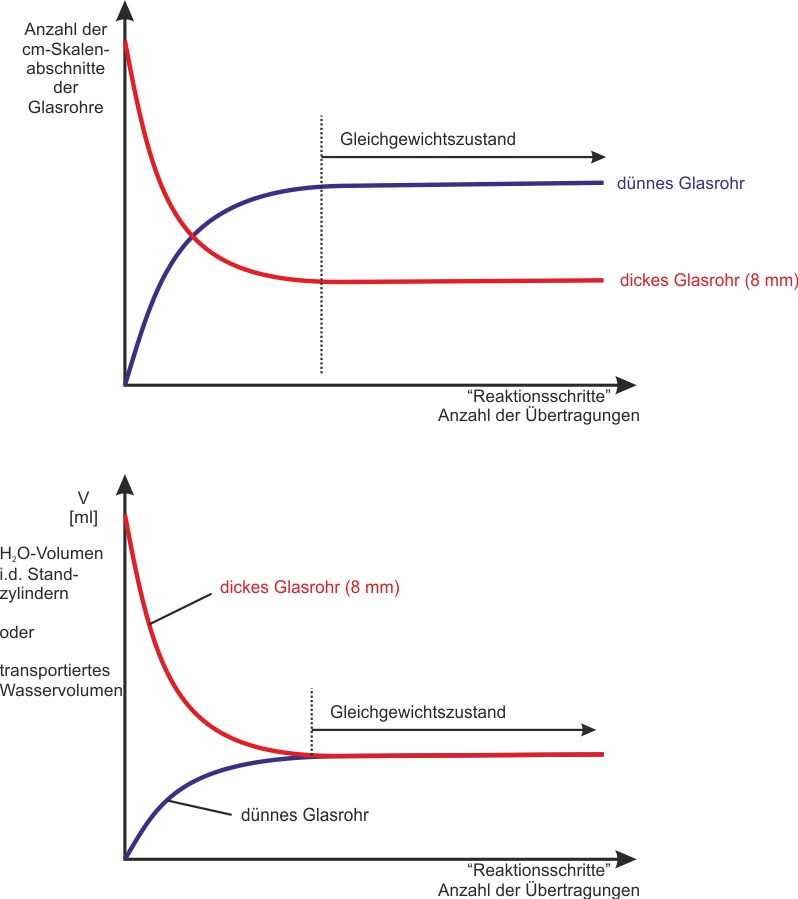
{/sliders}
-
2.4 Merkmale eines chemischen Gleichgewichts
2.4 Merkmale eines chemischen Gleichgewichts
Wichtig:
- Im abgeschlossenen System stellt sich ein Gleichgewicht von beiden Seiten her ein.
- Im Gleichgewicht (Endzustand) erfolgen gleich viel Hin- wie Rückreaktionen pro Zeiteinheit.
- Im Gleichgewicht liegen meist nicht gleich viel Anfangs- wie Endstoffe vor.
Wiederholung: System-Begriff
Offenes System Geschlossenes System Abgeschlossenes System
(= isoliertes SystemAustausch von.... + Energie
+ Teilchen+ Energie -- Kein Austausch von.... - Teilchen - Energie
- Teilchen- Gesamtenergie ist konstant
- i.d.R. idealisiertes System
idealisierte Beispiele "Kochtopf"
Mensch"Dampfkochtopf"
Reagenzglas mit Stopfen"Thermoskanne"
Universum -
2.5 Estergleichgewicht
Was du auf dieser Seite lernst
Du lernst, wie Carbonsäuren und Alkohole in einer Kondensationsreaktion zu Estern und Wasser reagieren. Am Beispiel des Estergleichgewichts (Essigsäure + Ethanol) wird deutlich, dass sowohl Hin- als auch Rückreaktion zum gleichen Endzustand führen – ein klassisches Beispiel für ein chemisches Gleichgewicht.
Grundlagen aus der 10. Klasse
Die Grundlagen zu Carbonsäuren und Alkoholen hast du bereits in der 10. Klasse kennengelernt:
→ Essigsäure / Ethansäure (Kl. 10) · → Alkohole / Alkanole (Kl. 10)2.5 Estergleichgewicht
Allgemeine Reaktion
Carbonsäure + Alkohol ⇌ Ester + Wasser
Wer sich an die 10. Klasse erinnern kann, kann ja mal versuchen, die Reaktionsgleichung für Ethansäure und Ethanol zu formulieren.
Tipp 1: Es handelt sich um eine Kondensationsreaktion – zwei Moleküle verbinden sich unter Abspaltung eines kleinen Moleküls (hier: Wasser).
Tipp 2: Es reagieren meist die funktionellen Gruppen miteinander und selten die Alkylgruppen.
Allgemeine Reaktionsgleichung (Summenformeln)
R–COOH + R'–OH ⇌ R–COO–R' + H2O
Carbonsäure + Alkohol ⇌ Ester + Wasser | Katalysator: H+ (z. B. konz. H2SO4)
✕Lösung: Reaktionsgleichung Ethansäure + Ethanol

Mechanismus der Veresterung (säurekatalysiert)
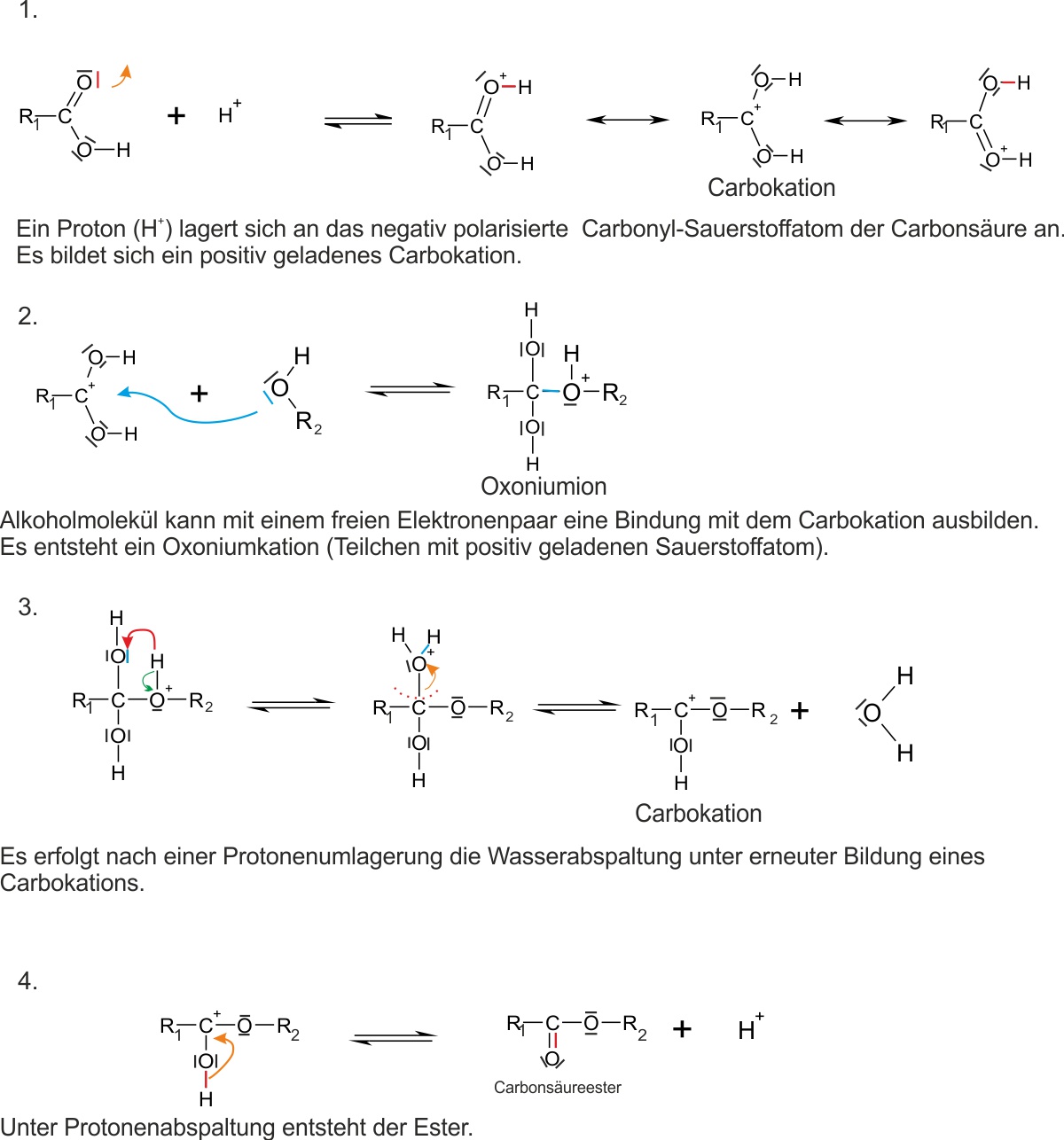
Der Mechanismus der säurekatalysierten Veresterung verläuft in vier reversiblen Teilschritten. Der Katalysator (H+) wird am Ende wieder freigesetzt:
↑ Zum Vergrößern klicken
✕Die 4 Teilschritte in Kurzform
1. Protonierung der Carbonylfunktion der Carbonsäure → Carbokation
2. Nukleophiler Angriff des Alkohols (freies Elektronenpaar) → Oxoniumion
3. Protonenumlagerung → Wasserabspaltung → erneutes Carbokation
4. Protonenabspaltung (H+ wird regeneriert) → CarbonsäureesterAlle Teilschritte sind reversibel (⇌). Der H+-Katalysator beschleunigt die Reaktion, verschiebt aber das Gleichgewicht nicht.
Das Estergleichgewicht – Nachweis durch zwei Versuchsansätze
Versuchsansatz 1 (Hinreaktion): Man gibt 1 mol Carbonsäure und 1 mol Alkohol zusammen.
Versuchsansatz 2 (Rückreaktion): Man gibt 1 mol Ester und 1 mol Wasser zusammen.Tipp: Was erwartest du?
Schau dir nochmals die Merkmale eines chemischen Gleichgewichts an. Ein echtes Gleichgewicht wird vom gleichen Endzustand aus erreicht – egal von welcher Seite man startet.
✕Lösung: Ergebnis des Experiments
Ergebnis: Man erhält in beiden Fällen denselben Endzustand.
↑ Zum Vergrößern klicken
Reaktionsgleichung und Mengenverhältnisse im Gleichgewicht
CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O
Zeitpunkt n(CH3COOH) n(C2H5OH) n(Ester) n(H2O) Anfang 1 (Hinreaktion) 1 mol 1 mol 0 mol 0 mol Gleichgewicht ⅓ mol ⅓ mol ⅔ mol ⅔ mol Anfang 2 (Rückreaktion) 0 mol 0 mol 1 mol 1 mol 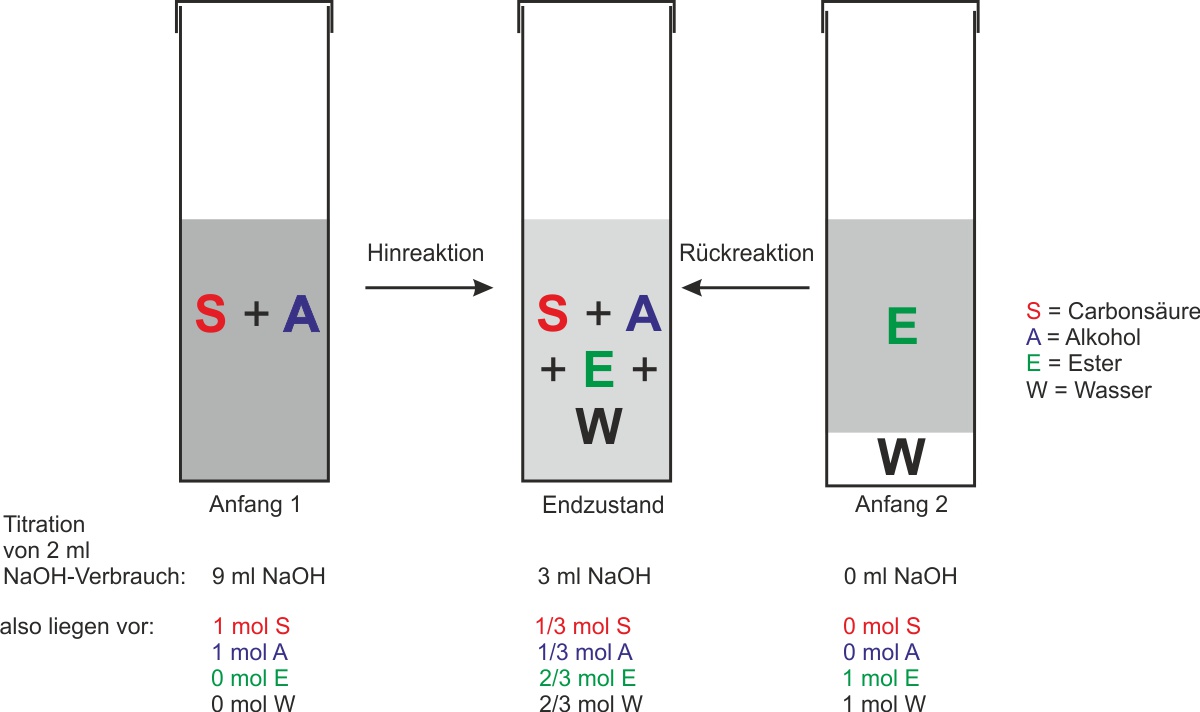
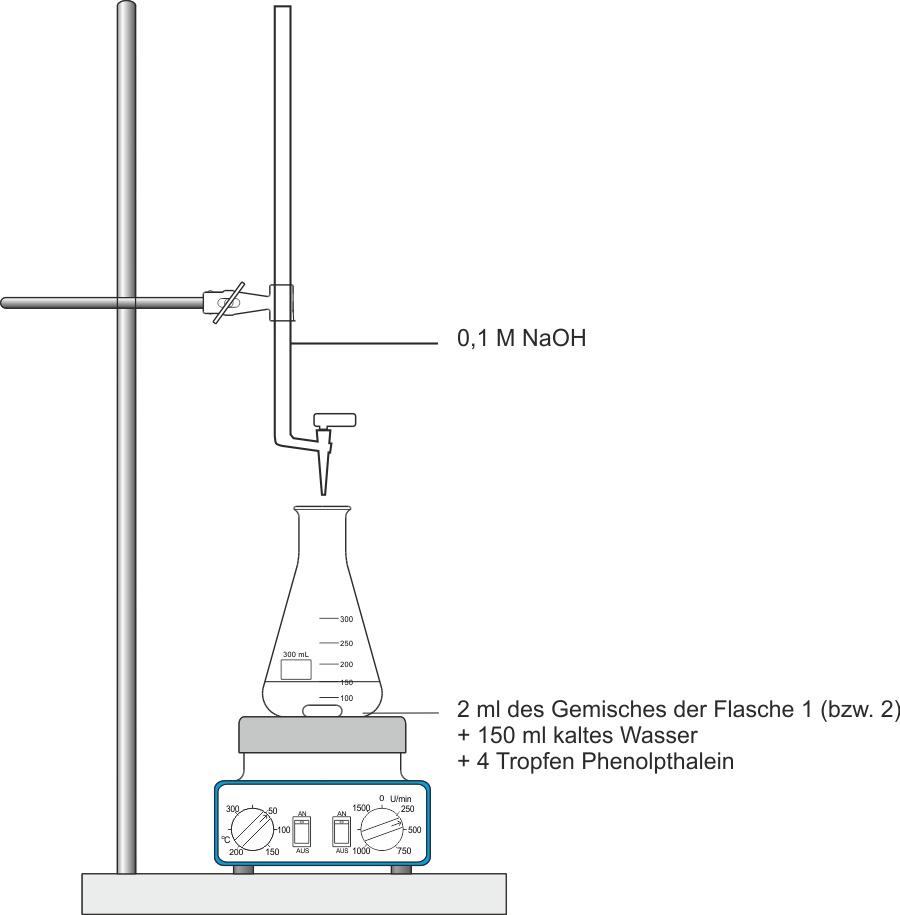
Quantitativer Nachweis: Titration der Carbonsäure
Man kann in beiden Versuchsansätzen die vorhandene Carbonsäuremenge durch quantitative Reaktion mit Natronlauge (Titration) messen.
Reaktionsgleichung der Titration (Summenformeln)
CH3COOH + NaOH → CH3COONa + H2O
Essigsäure reagiert vollständig und quantitativ mit NaOH. Mit 0,1 M NaOH und dem Verbrauch kann die Säuremenge berechnet werden: n(CH3COOH) = c(NaOH) · V(NaOH)
↑ Zum Vergrößern klicken
✕
Auf einen Blick – die wichtigsten Aussagen
KONDENSATIONSREAKTION
Bei der Veresterung verbinden sich Carbonsäure und Alkohol unter Abspaltung von Wasser – typische Kondensationsreaktion.
MECHANISMUS
4 reversible Schritte: Protonierung → Carbokation → Oxoniumion → Wasserabspaltung → Ester. H+ ist Katalysator.
GLEICHGEWICHT
Hin- und Rückreaktion erreichen denselben Endzustand: ⅔ mol Ester + ⅔ mol Wasser (aus je 1 mol Edukt).
TITRATION
Der Gleichgewichtszustand lässt sich quantitativ nachweisen: Die Carbonsäuremenge wird durch Titration mit NaOH bestimmt.
Häufige Fragen – Estergleichgewicht
Was ist eine Kondensationsreaktion und warum ist die Veresterung eine solche?
Bei einer Kondensationsreaktion verbinden sich zwei Moleküle unter Abspaltung eines kleinen Moleküls – hier Wasser. Bei der Veresterung reagiert die Carboxylgruppe (–COOH) der Carbonsäure mit der Hydroxylgruppe (–OH) des Alkohols: Beide funktionellen Gruppen treten miteinander in Wechselwirkung, und als Nebenprodukt entsteht ein Wassermolekül. Mehr zur Carboxylgruppe findest du auf der Seite Funktionelle Gruppe der Monocarbonsäuren (Kl. 10).
Wie läuft der Mechanismus der säurekatalysierten Veresterung ab?
Der Mechanismus verläuft in vier reversiblen Schritten: (1) Ein Proton (H+) lagert sich an das Carbonyl-Sauerstoffatom der Carbonsäure – es entsteht ein Carbokation. (2) Ein freies Elektronenpaar des Alkohols greift das Carbokation an – es bildet sich ein Oxoniumkation. (3) Nach einer Protonenumlagerung wird Wasser abgespalten und erneut ein Carbokation gebildet. (4) Durch Protonenabspaltung entsteht der fertige Ester, und H+ wird regeneriert.
Warum führen Hin- und Rückreaktion zum gleichen Endzustand?
Weil es sich um ein echtes chemisches Gleichgewicht handelt. Das Gleichgewicht wird dynamisch erreicht: Hin- und Rückreaktion laufen gleichzeitig ab, bis ihre Geschwindigkeiten gleich groß sind. Egal ob man mit 1 mol Carbonsäure + 1 mol Alkohol (Hinreaktion) oder mit 1 mol Ester + 1 mol Wasser (Rückreaktion) startet – der Endzustand ist identisch: ca. ⅔ mol Ester und ⅔ mol Wasser liegen neben ⅓ mol Carbonsäure und ⅓ mol Alkohol vor. Mehr zu den Merkmalen eines Gleichgewichts: Merkmale eines chemischen Gleichgewichts.
Wie kann man das Estergleichgewicht zugunsten des Esters verschieben?
Nach dem Prinzip von Le Chatelier kann das Gleichgewicht verschoben werden, indem man:
• einen der Reaktionspartner im Überschuss einsetzt (z. B. mehr Alkohol),
• ein Produkt laufend entzieht (z. B. Wasser durch Destillation oder mit einem Trockenmittel entfernt).
Hinweis: Ein Katalysator (konz. H2SO4) beschleunigt lediglich die Gleichgewichtseinstellung – er verschiebt das Gleichgewicht nicht.
Mehr dazu: Prinzip von Le Chatelier.Wie wird das Estergleichgewicht experimentell nachgewiesen?
Man misst quantitativ die verbliebene Carbonsäuremenge durch Titration mit Natronlauge (NaOH) und dem Indikator Phenolphthalein. Aus dem NaOH-Verbrauch lässt sich n(Carbonsäure) berechnen: n = c(NaOH) · V(NaOH). Beim Gleichgewichtsansatz verbraucht man nur noch ⅓ des ursprünglichen NaOH-Verbrauchs, was zeigt, dass ⅔ der Essigsäure abreagiert haben. Mehr zur Säure-Base-Titration: Säure-Base-Titration (Kursstufe).
Lernkarten – Estergleichgewicht
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist eine Kondensationsreaktion? Nenne ein Beispiel.
Zwei Moleküle verbinden sich unter Abspaltung eines kleinen Moleküls (z. B. H2O). Beispiel: Veresterung – Carbonsäure + Alkohol → Ester + Wasser.
2Welche Zwischenstufen entstehen im Mechanismus der säurekatalysierten Veresterung?
1. Carbokation (nach Protonierung der Carbonsäure)
2. Oxoniumkation (nach Angriff des Alkohols)
3. erneutes Carbokation (nach Wasserabspaltung)
→ Ester + H+ (regeneriert)3Was beweist das Estergleichgewicht-Experiment mit zwei Ansätzen?
Beide Ansätze (1 mol S + 1 mol A bzw. 1 mol E + 1 mol W) führen zum gleichen Endzustand – Beweis für ein echtes dynamisches Gleichgewicht.
4Nenne zwei Maßnahmen, um das Estergleichgewicht auf die Esterseite zu verschieben.
1. Überschuss eines Reaktionspartners (z. B. mehr Alkohol)
2. Entzug eines Produkts (z. B. Wasser abdestillieren oder binden)
→ Prinzip von Le Chatelier
Nicht geeignet: Katalysator – beschleunigt nur, verschiebt nicht.5Beim GG-Ansatz (1 mol CH3COOH + 1 mol C2H5OH) verbraucht die Titration von 2 ml Probe 3 ml NaOH (0,1 M). Wie viel mol Essigsäure sind noch vorhanden, wenn der Gesamtansatz 50 ml beträgt?
n(NaOH) pro 2 ml Probe = 0,003 l · 0,1 mol/l = 3·10−4 mol
→ Hochrechnung auf 50 ml: n(CH3COOH) = 3·10−4 · 25 = 7,5·10−3 mol ≈ ⅓ der Ausgangsmenge (erwartet: ⅓ mol)Weiter im Kapitel Gleichgewichtsreaktionen
← Merkmale eines chemischen Gleichgewichts → Schreibweise und Kollisionsmodell
🔁 Grundlagen aus Klasse 10: Essigsäure / Ethansäure (Kl. 10) · Alkohole / Alkanole (Kl. 10) · Funktionelle Gruppe der Monocarbonsäuren (Kl. 10)
⬇️ Weiter im Kapitel: Prinzip von Le Chatelier · Massenwirkungsgesetz · Ammoniaksynthese
-
2.6 Schreibweise und 2.7 Kollisionsmodell
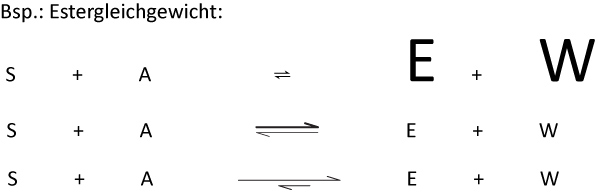
2.6 Schreib- und Sprechweise bei Gleichgewichtsreaktionen
Man sagt: „Das GG liegt rechts“
Um zu zeigen, dass das Gleichgewicht rechts liegt, gibt es mehrere Möglichkeiten:
- Man kann die Produkte "größer" Schreiben (wird so gut wie nie benutzt);
- Man kann den Pfeil nach rechts dicker machen;
- Man kann den Pfeil nach rechts länger zeichen.
2.7 Estergleichgewicht und Kollisionsmodell
Problem: Wie ist ein Gleichgewicht zwischen wenigen Säure- und Alkoholmolekülen und vielen Ester- und Wasserteilchen möglich?
2.7.1 WH: Kollisionsmodell
{slider title="Wiederholung" open="false" class="icon"}
Damit Teilchen miteinander reagieren können, müssen sie zusammenstoßen.
a) Erklärung: Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit: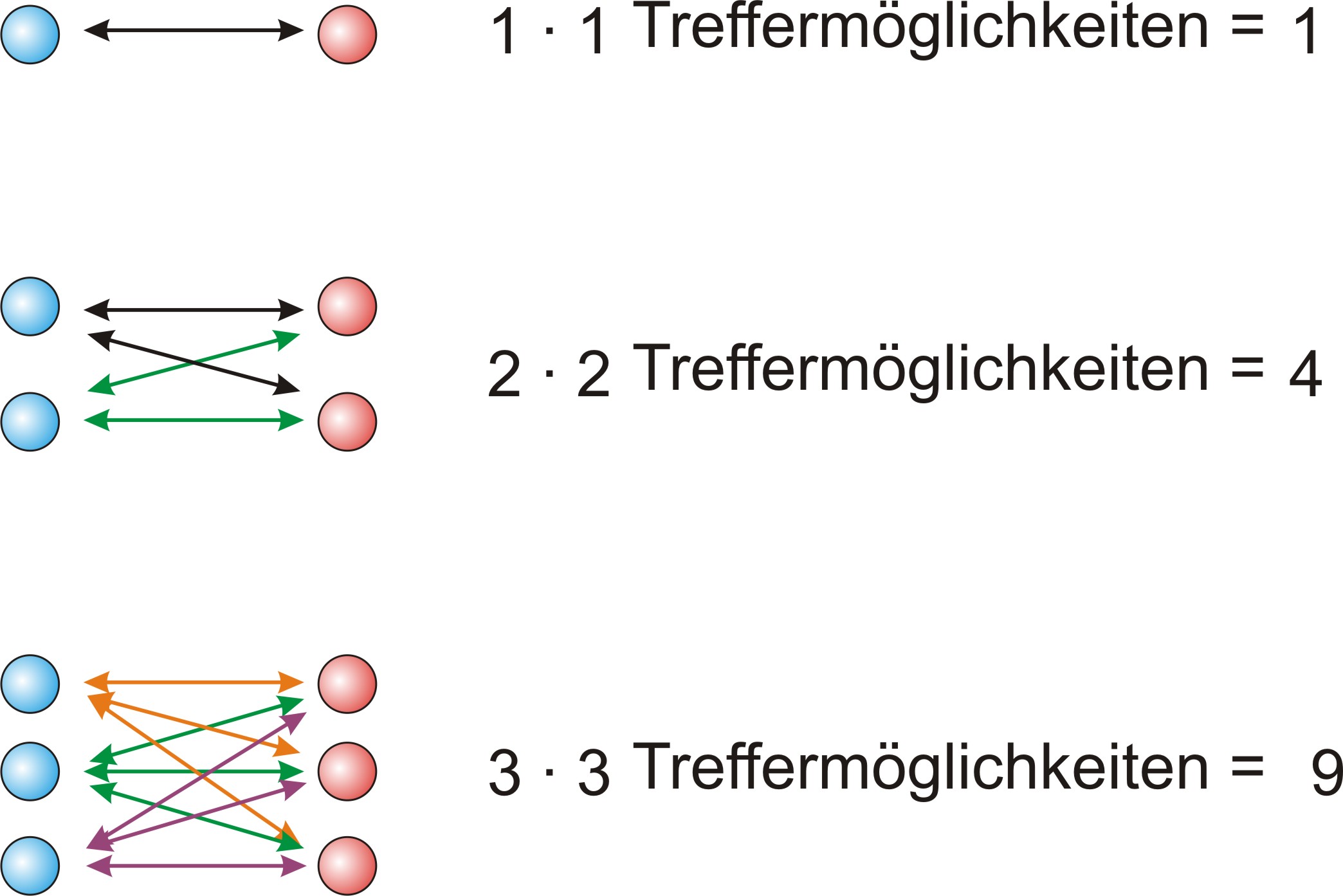
Reaktionsgeschwindigkeit bei Stoffen zweier Phasen (Aggregatzustände):
- Können nur an der Phasengrenze miteinander reagieren
- Je größer die Oberfläche (je stärker der Zerteilungsgrad), desto höher die Reaktionsgeschwindigkeit ⇨ Anzünden eines Feuers
⇨ Biologie: Oberflächenvergrößerung/-verkleinerung
b) Mindestgeschwindigkeit der Teilchen = Temperaturabhängigkeit
- nicht jeder Zusammenstoß führt zur Reaktion
- Reaktion setzt eine Mindestenergie und die richtige Orientierung der Teilchen zueinander voraus.
höhere Temperatur => höhere mittlere Geschwindigkeit der Teilchen
Mindestgeschwindigkeit vA ist nötigMaxwell-Boltzmann-Verteilung bei 3 Temperaturen:
vgl. Heftaufschrieb.
Je höher die Temp, desto mehr Teilchen überschreiten eine gegebene Temp. vA.
RGT-Regel (Reaktions-Geschwindigkeit-Temperaturregel):
Bei vielen Reaktionen bewirkt eine Temperaturerhöhung um 10°C eine 2-4 fache Beschleunigung der Reaktionsgeschwindigkeit.Zusammenfassung: 3 Faktoren die die Reaktionsgeschwindigkeit beeinflussen:
- Konzentration
- Temperatur
- Sterische Faktoren (v.a. bei großen Molekülen)
Info: Arrhenius-Gleichung beschreibt die quantitative Abhängigkeit der Reaktionsgeschwindigkeitskonstante k von der Temperatur
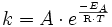
k = Geschwindigkeitskonstante
A = sterischer Faktor (Produkt aus der Stoßzahl Z und dem Orientierungsfaktor P)
EA = Aktivierungsenergie
R = 8,314 J/(K mol); Avogadro-Konstante (NA) und Boltzmann-Konstante (kB) R = NA ∙ kB
T = absolute (thermodynamische) Temperatur (Einheit: K).
e = Konstante = eulersche Zahl = 2,72
⇨T groß ⇨ k groß ⇨ v groß
⇨EA klein ⇨k groß ⇨v groß{/sliders}
Zurück zum Problem: Wie ist ein Gleichgewicht zwischen wenigen Säure- und Alkoholmolekülen und vielen Ester- und Wasserteilchen möglich?
Wie ist ein Gleichgewicht zwischen wenigen Säure- und Alkoholmolekülen und vielen Ester- und Wasserteilchen möglich?
S + A ⇌ E + W
Weniger Stöße, jedoch größere Erfolgchancen: Teilchen sind reaktionsfreudig VieleStöße, jedoch geringere Erfolgschancen Teilchen sind reaktionsträge Merke: Wenige reaktionsfreudige Teilchen können vielen reaktionsträgen Teilchen das Gleichgewicht halten.
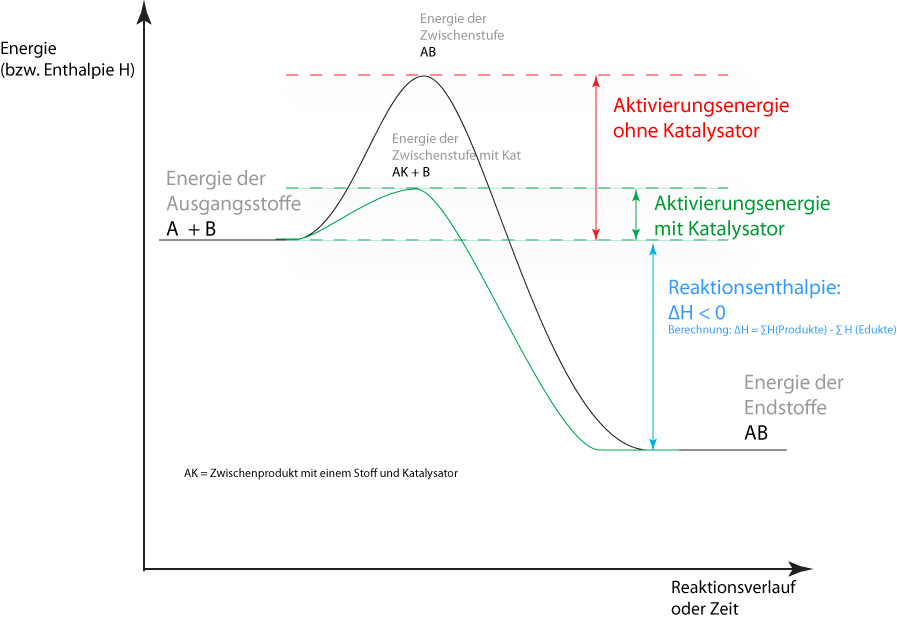
2.7.2 Reaktionsgeschwindigkeit und Katalysatoren
a) homogene Katalyse: Edukte und Kat. sind in der gleichen Phase (z.B. Lsg)
- Bildung von Zwischenstufen ⇨ EA ↓ ⇨ vmin ↓
b) heterogene Katalyse: Edukte u. Kat bilden 2 verschiedene Phasen
Edukte werden an Kat.-Oberfläche adsorbiert
⇨ Schwächung der Bdg.
⇨ günstige Räumliche Orientierung
⇨ Erhöhung der Konzentration
(Bsp. H₂ an Pt-Oberfläche)
Vermutung: Elektronenüberschuss oder –mangel an Oberfläche.c) Autokatalyse: Katalysator entsteht erst durch den Reaktionsablauf ⇨ Reaktion erst langsam ⇨ dann immer schneller (vgl. Abb. S. 80)
d) Biokatalyse: Enzyme (Proteine, Eiweiße) beschleunigen sehr selektiv Reaktionen ⇨ Bilden Enzym-Substrat-Komplex ⇨ Rkt findet bei Körpertemperatur statt. Substratspezifisch und Wirkungsspezifisch;
-
2.9 Säure-Base-Reaktion mit Benzoesäure
2.8 Allgemeines Zahlenbeispiel
A + B ⇌ C + D Vorher 1000 1000 0 0 Nachher 1000 - X 1000 - X X X z.B. in GG 800 800 200 200 2.9 Säure-Basereaktionen mit Benzoesäure
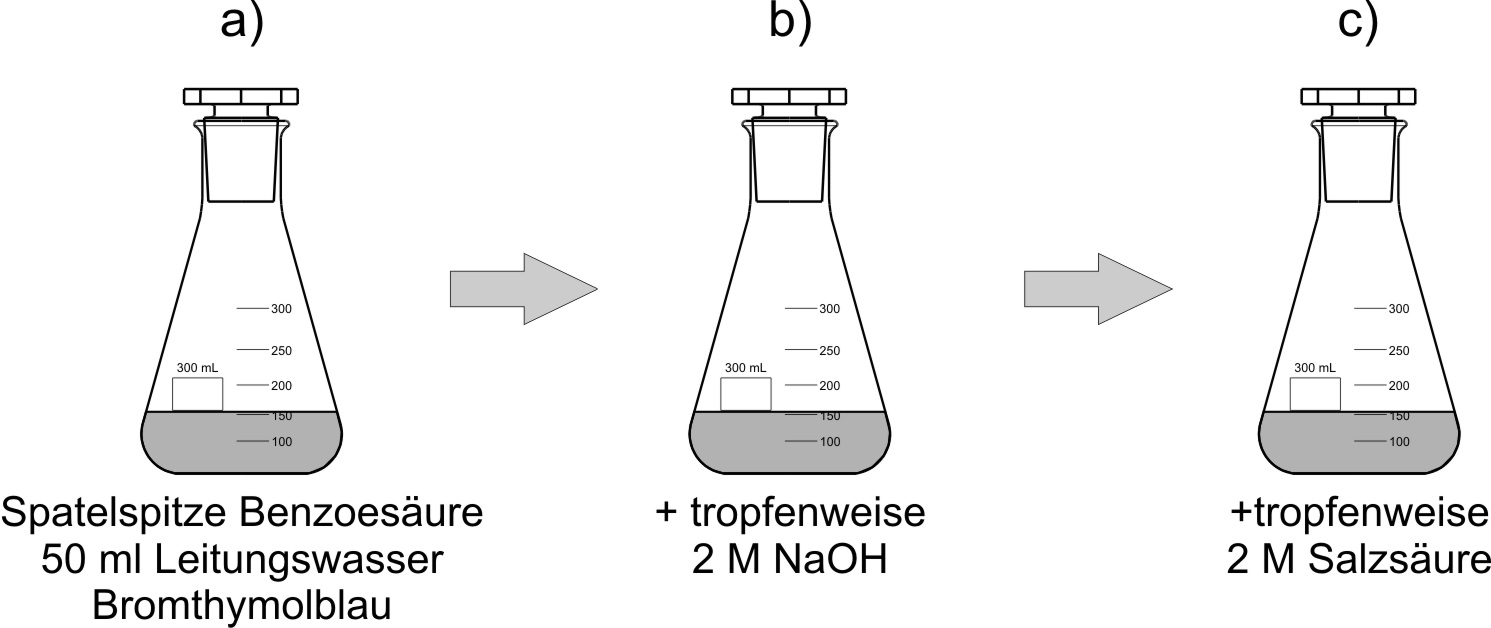
a) Benzoesäure + Wasser
Man gibt festes Benzoesäure in Wasser. Dabei beobachtet man, dass die Benzoesäure als weiße Substanz oben auf dem Wasser schwimmt. Auch mit Schütteln löst sie sich nichtauf.
Frage: Warum löst sich Benzoesäure nicht in Wasser? Dafür muss man sich einmal Benzoesäure anschauen (Hinweis: Benzoesäure ist noch vereinfacht "falsch" geschrieben, da wir die Aromaten erst später genauer betrachten).
Erklärt, warum Benzoesäure nur schlecht in Wasser löslich ist!
{slider title="Lösung" open="false" class="icon"}
Bei Benzoesäure ist ein großer Teil unpolar. Der polare Teil ist kleiner. Es kann zwar mit Wasser H-Brücken ausbilden, aber der große Rest sorgt bisher für eine schlechte Löslichkeit.
Hinweis: Ähnliches löst sich in ähnlichem.
{/sliders}
Zusammenfassung Beobachtung: wenig löslich in Wasser; die Lösung reagiert schwach sauer.
Formuliert die Reaktionsgleichung für die Reaktion von Benozesäure mit Wasser mit binden und nichtbindenen Elektronenpaaren (Hinweis; Benzoesäure ist jetzt schon etwas vereinfacht geschrieben indem die H-Atome am Ring weggelassen wurden.
{slider title="Lösung" open="false" class="icon"}
Es findet nur eine schwache Reaktion mit H2O statt. Es reagieren nur wenige Benzoesäuremoleküle. Das Gleichgewicht liegt rechts.
{/sliders}
b) Benzoesäure + Natronlauge (Neutralisation)
Man gibt vorsichtig Natronlauge zu und schüttelt die Lösung bis
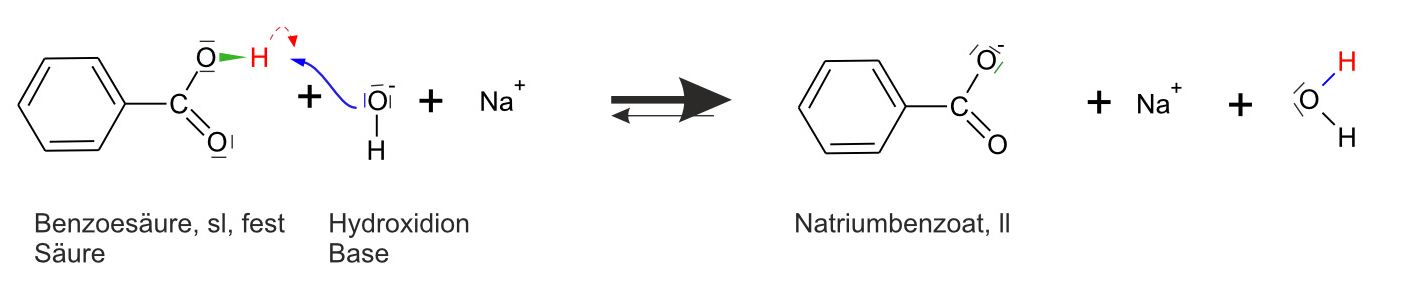
Beobachtung: Es entsteht eine klare Lösung.Formuliert hierfür auch wieder eine Reaktionsgleichung mit bindenden und nichtbindenden Elektronenpaaren.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
Die Benzoesäuremoleküle reagieren praktisch vollständig.c) gelöstes Natriumbenzoat + verd. Salzsäure
Die klare Lösung wird trübe. Weißes, pulverartige Substanz schwimmt wieder auf der Oberfläche.{slider title="Lösung" open="false" class="icon"}
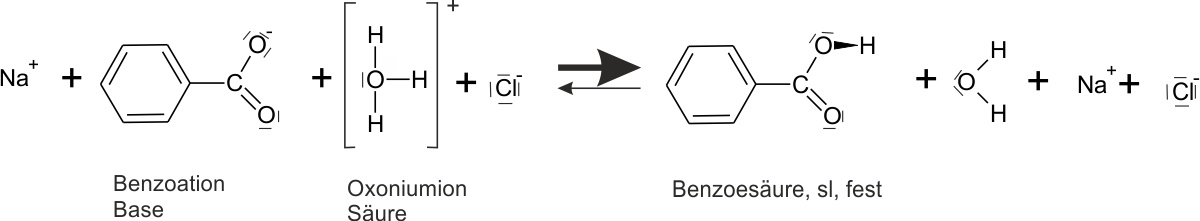
{/sliders}
Feste Benzoesäure scheidet sich ab; die Benzoanionen reagieren praktisch vollständig.