Isomerie
-
01 Isomerie
Naturstoffe
1 Isomerie:
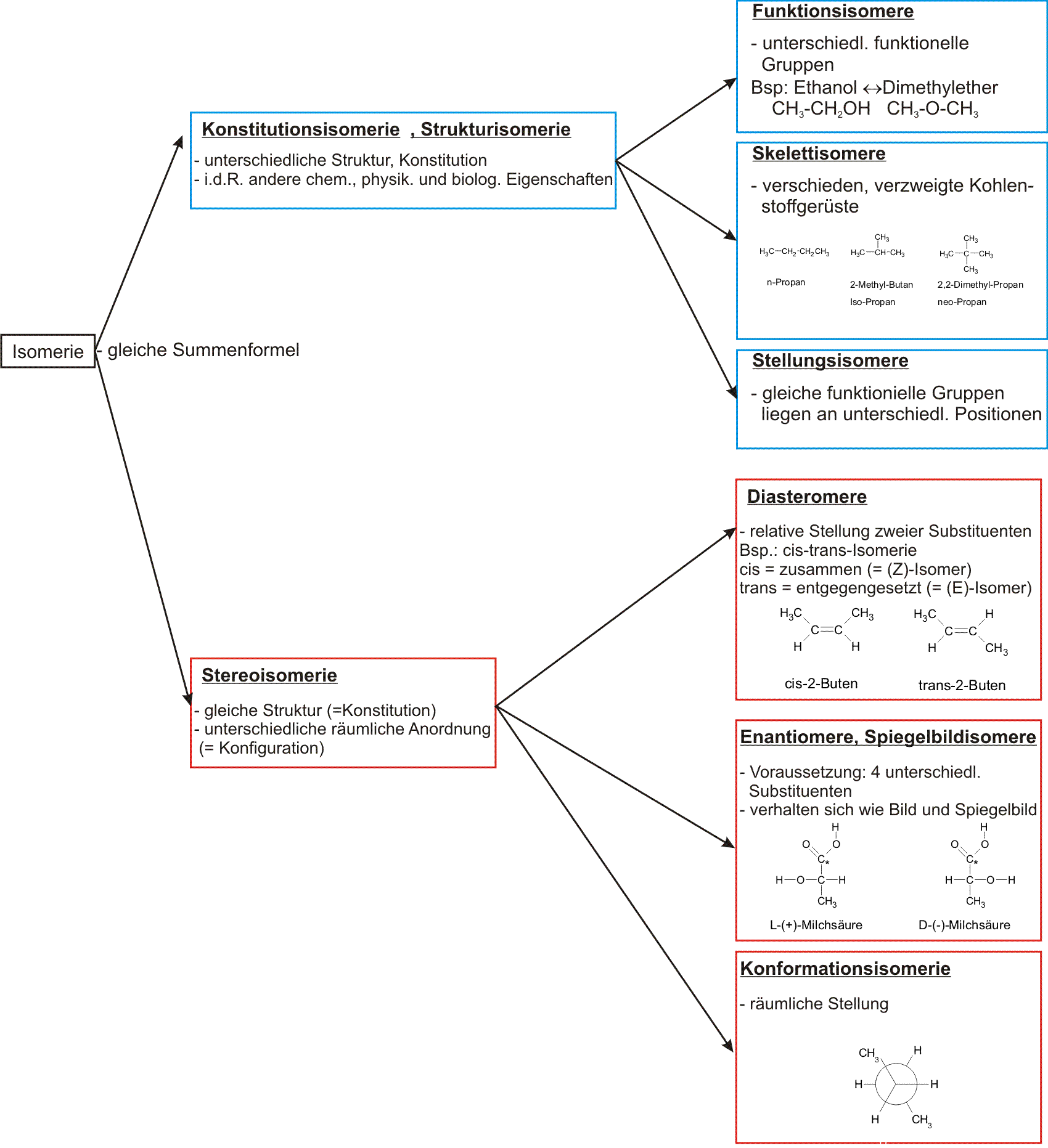
Isomere[1]: Zwei Verbindungen mit gleicher Summenformel, aber unterschiedlicher chemischer Struktur. Isomere unterscheiden sich teilweise in ihren physikalischen, biologischen und chemischen Eigenschaften.
Chiral[2]: Objekte, deren Spiegelbild nicht durch Drehung mit dem Original in Deckung gebracht werden können.
Achiral: Objekte, deren Spiegelbild durch Drehung in Deckung gebracht werden können.
-
01.4 Butan
Was du auf dieser Seite lernst
Butan (C₄H₁₀) ist das erste Alkan, das in zwei verschiedenen Strukturen vorkommt. Du lernst den zentralen Begriff der Konstitutionsisomerie kennen, verstehst warum n-Butan und Isobutan verschiedene Siedepunkte haben, und übst die Halbstrukturformel als platzsparende Schreibweise.
Grundlagen aus 1.1 Methan
Summenformel, Strukturformel und Lewis-Formel hast du am Beispiel Methan kennengelernt: → 1.1 Methan · → Lewis-Formeln (Kl. 9)
Hinweis: 1.2 Ethan und 1.3 Propan werden nur bei ausreichend Zeit besprochen. Da sie ähnlich aufgebaut sind, wird auf einen eigenen Heftaufschrieb verzichtet (vgl. 1.5 Homologe Reihe).
1.4.1 Vorkommen
Im Erdgas; fällt an bei der Benzingewinnung.
1.4.2 Eigenschaften
Farbloses Gas · größere Dichte als Luft · brennbar (Verbrennungsprodukte bei vollständiger Verbrennung: CO2 und H2O) · unter Druck leicht verflüssigbar.
1.4.3 Ermittlung der Summenformel und Strukturformel
a) Qualitative Analyse (Elementaranalyse)
↑ Zum Vergrößern klicken
✕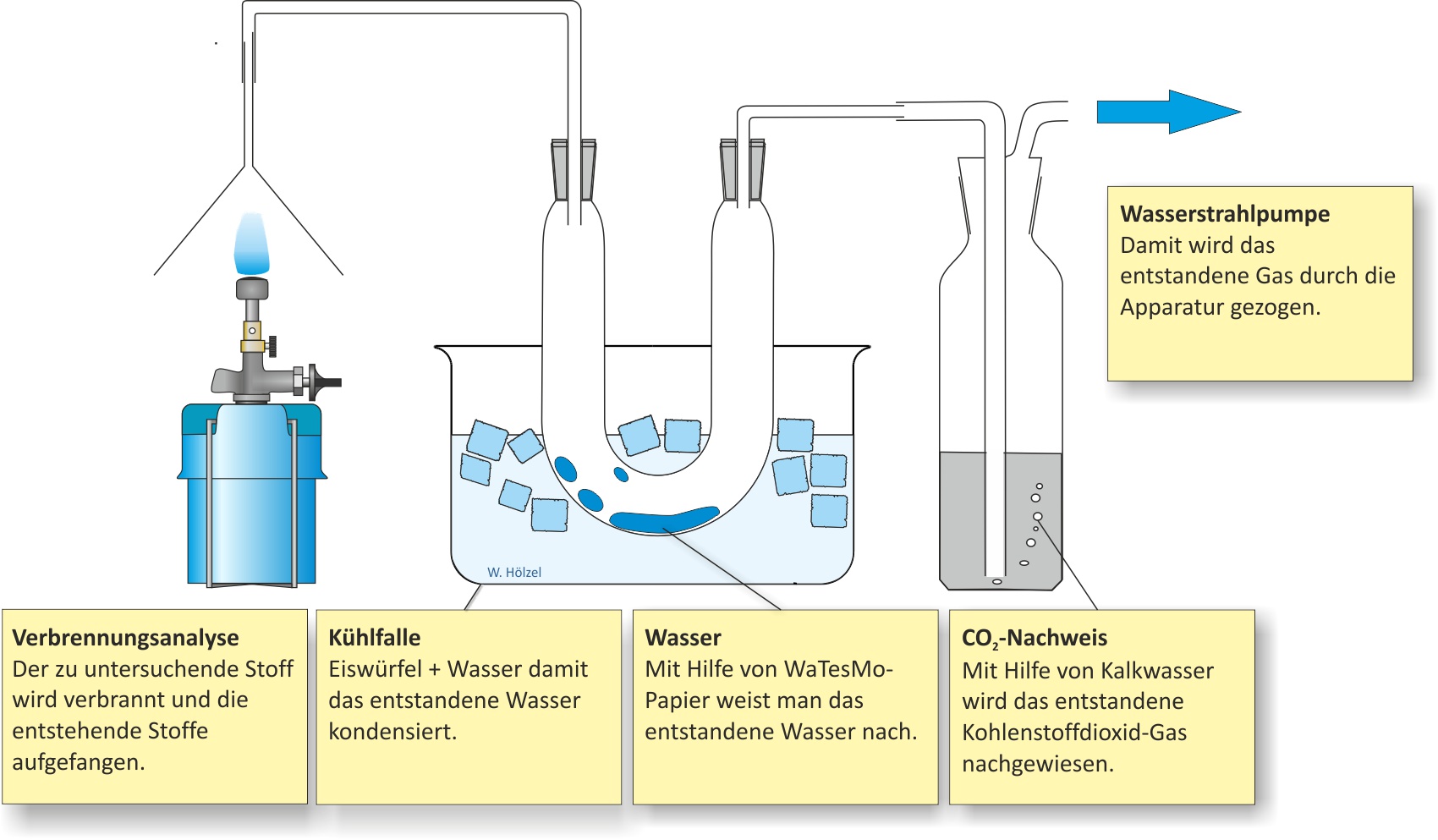
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) zeigen, dass Butan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält.
b) Bau und Formeln
1. Molare Masse = 58,12 g/mol · Molekülmasse = 58,12 u
2. Summenformel: C4H103. Strukturformel – zwei Möglichkeiten:
✕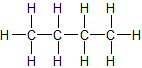 ✕
✕
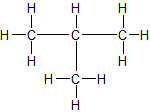
ZMK: nur Van-der-Waals-Kräfte. Bei n-Butan können sich die Moleküle dichter zusammenlagern → stärkere ZMK → etwas höhere Siedetemperatur als Isobutan.
Räumliche Strukturen im Kugelstabmodell (versuche, die Abbildungen n-Butan oder Isobutan zuzuordnen):
✕ ✕
✕
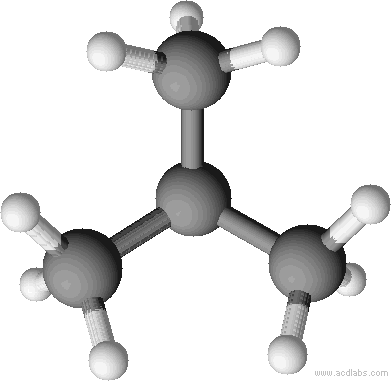
Renderbild n-Butan als Kugelstabmodell:
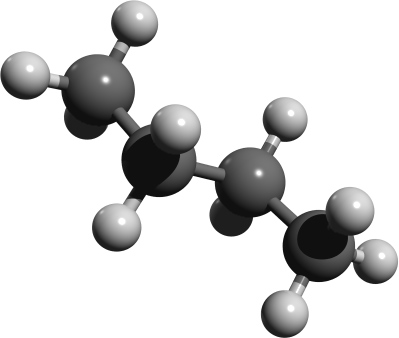
Kalottenmodell von 2-Methylpropan (= Isobutan) – bei Kalottenmodellen wird die Raumfüllung der Atome sichtbar:

Da Strukturformeln bei größeren Molekülen zu aufwendig sind, nutzt man die Halbstrukturformel: Die Wasserstoffatome werden als Summe direkt hinter das jeweilige C-Atom geschrieben. Man ermittelt zunächst, wie viele Bindungen ein C-Atom bereits hat, und ergänzt H-Atome bis zur Vierbindigkeit. Hier am Beispiel Isobutan:
↑ Zum Vergrößern klicken
✕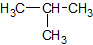
1.4.4 Verwendung
Heizgas („blaue Gaskartuschen") · Kältemittel (Ersatz für FCKW) · Treibgas in Sprays · Feuerzeuggas (häufig zusammen mit Propan).
1.4.5 Isomerie
(isos (griech.) = gleich; meros (griech.) = Teil)
Definition – Konstitutionsisomerie
Verbindungen, deren Moleküle bei gleicher Summenformel unterschiedliche Strukturformeln besitzen, bezeichnet man als Isomere. Isomere unterscheiden sich vor allem in ihren physikalischen Eigenschaften (Schmelz- und Siedepunkt) und wenig in ihren chemischen Reaktionen.
1.4.6 Vollständige Verbrennung (Oxidation)
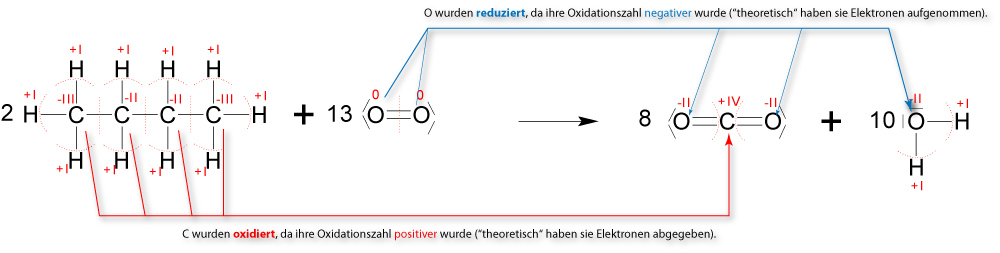
Wenn Butan vollständig verbrannt wird, entstehen ausschließlich Kohlenstoffdioxid und Wasser:
↑ Zum Vergrößern klicken
✕
Auf einen Blick – Butan
Summenformel
C4H10 · molare Masse 58,12 g/mol · stimmt mit der allg. Formel CₙH₂ₙ₊₂ überein (n = 4 → 4·2+2 = 10 H).
Konstitutionsisomerie
n-Butan (Sdp. −0,5 °C) und Isobutan = 2-Methylpropan (Sdp. −12 °C) haben die gleiche Summenformel C₄H₁₀, aber verschiedene Strukturformeln.
ZMK und Siedepunkt
Nur Van-der-Waals-Kräfte. n-Butan lagert sich dichter zusammen → stärkere ZMK → höherer Siedepunkt als das verzweigte Isobutan.
Halbstrukturformel
H-Atome als Summe hinter das C schreiben. n-Butan: CH₃–CH₂–CH₂–CH₃ · Isobutan: CH₃–CH(CH₃)–CH₃ · Vierbindigkeit von C muss stets erfüllt sein.
Häufige Fragen – Butan
Was versteht man unter Konstitutionsisomerie?
Konstitutionsisomere sind Verbindungen mit gleicher Summenformel, aber unterschiedlicher Verknüpfung der Atome. Bei C₄H₁₀ gibt es zwei Isomere: n-Butan (unverzweigte Kette) und 2-Methylpropan (Isobutan) (verzweigte Kette). Sie unterscheiden sich in physikalischen Eigenschaften wie dem Siedepunkt, kaum aber in chemischen Reaktionen. Mit steigender C-Zahl nimmt die Zahl möglicher Isomere stark zu (C₅: 3, C₁₀: 75).
Warum hat n-Butan einen höheren Siedepunkt als Isobutan?
Beide Isomere sind unpolar und besitzen nur Van-der-Waals-Kräfte als Wechselwirkung zwischen den Molekülen. Die gestreckte Kette von n-Butan ermöglicht eine größere Kontaktfläche zwischen benachbarten Molekülen als die kompaktere, kugelförmigere Gestalt von Isobutan. Größere Kontaktfläche → stärkere Van-der-Waals-Kräfte → höherer Siedepunkt (n-Butan: −0,5 °C; Isobutan: −12 °C).
Was ist der Unterschied zwischen Strukturformel, Halbstrukturformel und Summenformel?
Die Summenformel gibt nur die Anzahl der Atome an (C₄H₁₀), nicht deren Anordnung. Die Strukturformel zeigt alle Bindungsstriche explizit – anschaulich, aber bei großen Molekülen aufwendig. Die Halbstrukturformel ist ein Kompromiss: Das C-Gerüst wird ausgeschrieben, H-Atome werden als Anzahl hinter das jeweilige C-Atom gesetzt. Isobutan: CH₃–CH(CH₃)–CH₃ · n-Butan: CH₃–CH₂–CH₂–CH₃.
Wofür wird Butan im Alltag verwendet?
Butan wird wegen seiner leichten Verflüssigbarkeit unter Druck vielfältig eingesetzt: als Heizgas in Gaskartuschen beim Camping, als Kältemittel (FCKW-Ersatz in Kühlschränken), als Treibgas in Sprühdosen und als Feuerzeuggas (oft zusammen mit Propan).
Wie lautet die ausgeglichene Verbrennungsgleichung für n-Butan?
Vollständige Verbrennung:
2 C₄H₁₀ + 13 O₂ → 8 CO₂ + 10 H₂O
Kontrolle: C: 8 = 8 ✓ · H: 20 = 20 ✓ · O: 26 = 26 ✓
Die Reaktion ist stark exotherm – deshalb wird Butan als Brennstoff genutzt.Lernkarten – Butan
Klicke auf eine Karte, um die Antwort zu sehen.
1Gib Summenformel und molare Masse von Butan an. Prüfe die allg. Alkan-Formel.
Summenformel: C₄H₁₀
Molare Masse: 58,12 g/mol
Formel CₙH₂ₙ₊₂ mit n=4: 2·4+2 = 10 H ✓2Was sind Konstitutionsisomere? Nenne die beiden C₄H₁₀-Isomere mit Siedepunkten.
Gleiche Summenformel, verschiedene Struktur:
n-Butan: unverzweigt · Sdp. −0,5 °C
2-Methylpropan (Isobutan): verzweigt · Sdp. −12 °C3Schreibe n-Butan und Isobutan als Halbstrukturformel.
n-Butan:
CH₃–CH₂–CH₂–CH₃
Isobutan (2-Methylpropan):
CH₃–CH(CH₃)–CH₃4Warum hat n-Butan einen höheren Siedepunkt als Isobutan, obwohl beide C₄H₁₀ sind?
Nur Van-der-Waals-Kräfte vorhanden.
n-Butan: gestreckte Kette → größere Kontaktfläche
→ stärkere VdW-Kräfte → höherer Siedepunkt
Isobutan: kompaktere Form → weniger Kontakt5Stelle die ausgeglichene Verbrennungsgleichung für n-Butan auf.
2 C₄H₁₀ + 13 O₂ → 8 CO₂ + 10 H₂O
Kontrolle:
C: 2·4 = 8 | 8·1 = 8 ✓
H: 2·10 = 20 | 10·2 = 20 ✓
O: 13·2 = 26 | 8·2+10 = 26 ✓Weiter im Kapitel Alkane
← 1.1 Methan → 1.5 Homologe Reihe → 1.6 Nomenklatur
🔁 Grundlagen: 1.1 Methan · Lewis-Formeln (Kl. 9)
📚 Vertiefung: Isomerie bei Alkenen · Isomerie (Kursstufe) -
01.6 Nomenklatur der Alkane
Was du auf dieser Seite lernst
Mit der Genfer Nomenklatur (IUPAC-System) kannst du verzweigte Alkane eindeutig benennen und aus einem Namen die Strukturformel ableiten. Du lernst die sieben Nomenklaturregeln Schritt für Schritt kennen und wendest sie an konkreten Beispielmolekülen an.
Grundlagen aus dem Alkane-Kapitel
Die homologe Reihe der Alkane und den Begriff des Alkylrests hast du bereits im vorherigen Abschnitt kennengelernt: → 1.5 Homologe Reihe der Alkane
1.6 Nomenklatur (Benennung) der Alkane
1.6.1 Homologe Reihe der Alkane mit Alkylrest
Ein Alkylrest enthält jeweils ein Wasserstoff-Atom weniger als das entsprechende Alkanmolekül. Alkyle finden sich oft als „Seitengruppe" verzweigter Alkane.
Name Summenformel Name des Alkyls Summenformel Methan CH4 Methylrest –CH3 Ethan C2H6 Ethylrest –C2H5 Propan C3H8 Propylrest –C3H7 allg. Alkane CnH2n+2 Alkylrest –CnH2n+1 1.6.2 Nomenklaturregel für Alkane (Genfer Nomenklatur)
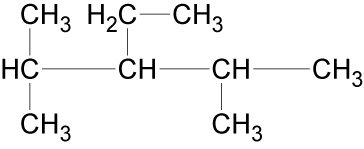
Als Beispiel soll folgendes Molekül systematisch benannt werden:
↑ Zum Vergrößern klicken
✕
-
Alkane haben die Endung -an.
-
Der Name des Alkans, das die Hauptkette bildet, liefert den Stammnamen des Stoffs.
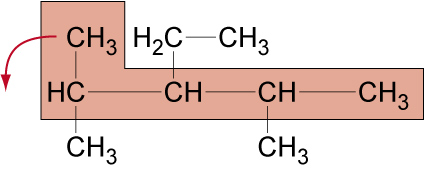
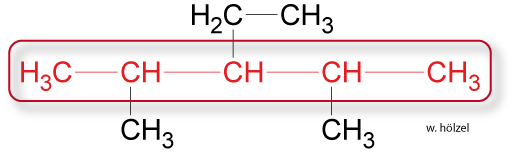
Längste Kette der Kohlenstoffkette suchen und „Glattbügeln".↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕
-
Alle Alkane mit 5 Kohlenstoff-Atomen in der längsten Kette heißen Pentan.
-
Die Namen der Seitenketten werden dem Stammnamen vorangestellt.
↑ Zum Vergrößern klicken
✕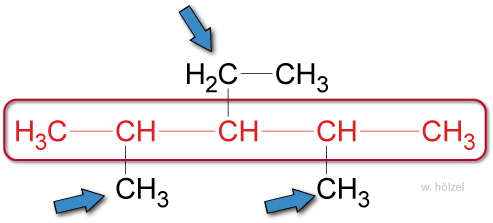
Beispiel: Methyl-Ethyl-Pentan.
-
Um anzuzeigen, an welchem Kohlenstoff-Atom die Seitenkette sitzt, wird die Hauptkette nummeriert. Die Verzweigungsstellen sollen dabei möglichst kleine Zahlen erhalten. Die Zahlen werden den Namen der Seitenketten vorangestellt.
↑ Zum Vergrößern klicken
✕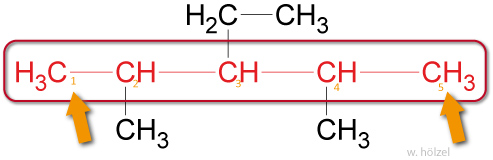
Beispiel: 2,4-Methyl-3-Ethyl-Pentan.
-
Treten gleiche Seitenketten mehrfach in einem Molekül auf, so wird das entsprechende Zahlwort (Di-, Tri-, Tetra-, Penta-) als Vorsilbe verwendet.
↑ Zum Vergrößern klicken
✕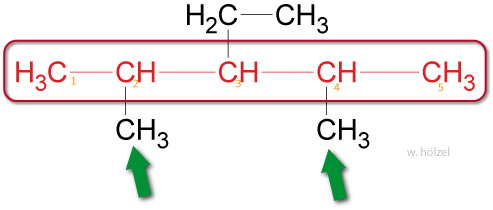
Beispiel: 2,4-Dimethyl-3-Ethyl-Pentan.
-
Unterschiedliche Seitenketten werden alphabetisch nach dem Namen der Alkylgruppe geordnet.
↑ Zum Vergrößern klicken
✕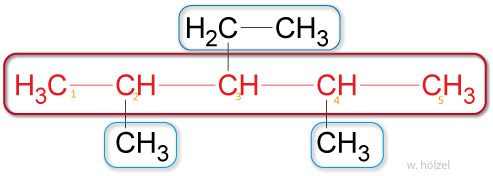
Beispiel: 3-Ethyl-2,4-Dimethylpentan.
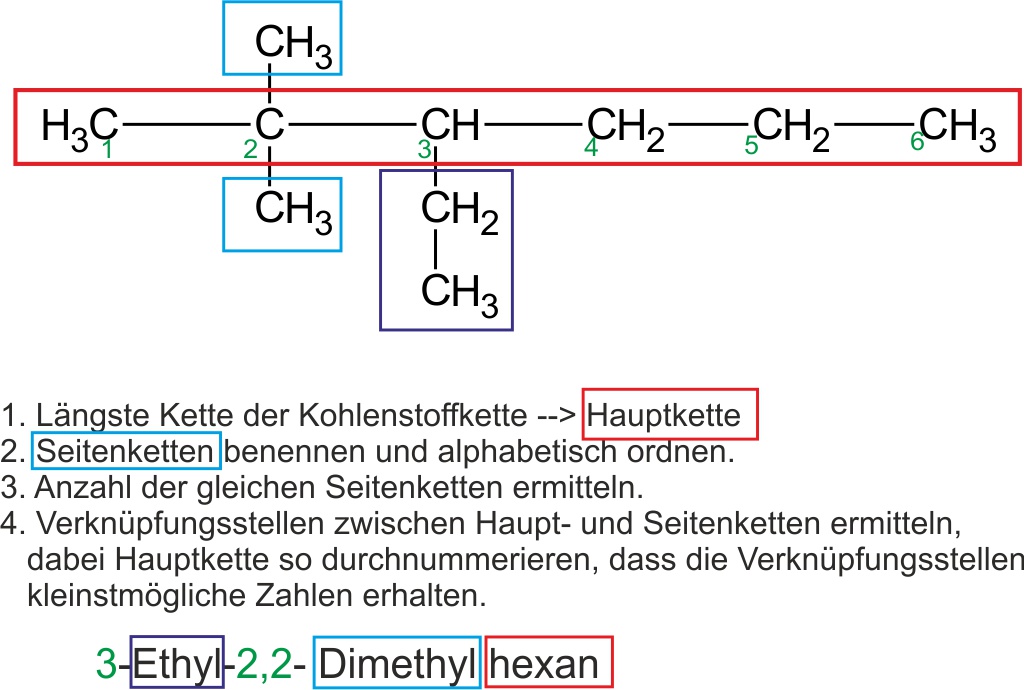
Folgende Abbildung zeigt ein weiteres Beispiel für die vollständige Anwendung aller Nomenklaturregeln:
↑ Zum Vergrößern klicken
✕
Auf einen Blick – die wichtigsten Aussagen
HAUPTKETTE
Die längste zusammenhängende C-Kette bestimmt den Stammnamen (z. B. Pentan für 5 C-Atome).
LOKANTEN
Die Hauptkette wird so nummeriert, dass die Verzweigungsstellen möglichst kleine Zahlen erhalten.
VORSILBEN
Gleiche Seitenketten werden gezählt: Di- (2×), Tri- (3×), Tetra- (4×). Diese Vorsilben zählen nicht bei der alphabetischen Sortierung.
ALPHABETISCH
Verschiedene Seitenketten stehen im Namen in alphabetischer Reihenfolge – Ethyl (E) vor Methyl (M).
Häufige Fragen – Genfer Nomenklatur der Alkane
Was ist der Unterschied zwischen einem Alkan und einem Alkylrest?
Ein Alkan ist ein gesättigter Kohlenwasserstoff mit der allgemeinen Formel CnH2n+2. Ein Alkylrest entsteht, wenn man einem Alkan-Molekül ein Wasserstoff-Atom „entfernt"; seine allgemeine Formel lautet –CnH2n+1. Alkylreste treten als Seitenketten in verzweigten Alkanen auf – zum Beispiel der Methylrest (–CH3) oder der Ethylrest (–C2H5).
Wie bestimmt man die Hauptkette bei einem verzweigten Alkan?
Man sucht die längste zusammenhängende Kohlenstoffkette im Molekül. Es hilft, die Kette gedanklich „glatt zu bügeln". Der Name des entsprechenden unverzweigten Alkans (Methan, Ethan, Propan, Butan, Pentan, Hexan …) bildet den Stammnamen. Bei gleich langen Ketten wählt man diejenige, die die meisten Seitenketten trägt.
Warum sollen die Lokanten (Positionszahlen) möglichst klein sein?
Die Regel der niedrigsten Lokanten sorgt dafür, dass es für jede Verbindung nur einen eindeutigen IUPAC-Namen gibt. Die Hauptkette wird von dem Ende aus nummeriert, das dem ersten Verzweigungspunkt am nächsten liegt. So ergibt sich beispielsweise „2-Methylbutan" statt „3-Methylbutan" für dieselbe Verbindung.
Was bedeuten die Vorsilben Di-, Tri- und Tetra-?
Treten gleiche Seitenketten mehrfach auf, wird die Anzahl als Zahlwort vor den Seitenkettenname gesetzt: Di- (2×), Tri- (3×), Tetra- (4×), Penta- (5×). Alle zugehörigen Lokanten werden aufgelistet, z. B. „2,4-Dimethyl" für zwei Methylgruppen an C-Atom 2 und 4. Wichtig: Diese Zahlvorsilben werden bei der alphabetischen Sortierung der Seitenketten nicht berücksichtigt.
In welcher Reihenfolge werden unterschiedliche Seitenketten im Namen angegeben?
Verschiedene Seitenketten werden alphabetisch nach dem Namen der Alkylgruppe geordnet – dabei bleiben Zahlvorsilben wie Di- oder Tri- außer Acht. Ethyl (E) kommt daher vor Methyl (M), also z. B.: „3-Ethyl-2,4-dimethylpentan". Mehr zur Nomenklatur der nächsten Stoffklasse findest du auf der Seite → Nomenklatur der Alkene (Kl. 10).
Lernkarten – Genfer Nomenklatur
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist ein Alkylrest und wie lautet seine allgemeine Formel?
Ein Alkylrest ist ein Alkan, dem ein H-Atom fehlt. Formel: –CnH2n+1 (z. B. Methylrest –CH3, Ethylrest –C2H5).
2Was bestimmt den Stammnamen eines verzweigten Alkans?
Die längste zusammenhängende Kohlenstoffkette (Hauptkette). 5 C-Atome → Pentan; 6 C-Atome → Hexan usw.
3Wie wird die Hauptkette nummeriert?
Von dem Ende aus, das dem ersten Verzweigungspunkt am nächsten liegt → niedrigste Lokanten für alle Seitenketten.
4Welche Reihenfolge gilt für verschiedene Seitenketten im IUPAC-Namen?
Alphabetisch nach dem Alkylgruppennamen (ohne Vorsilben Di-, Tri-). Ethyl (E) vor Methyl (M).
5Wie heißt: 6 C-Kette, Ethylgruppe an C-3, zwei Methylgruppen an C-2 und C-2?
3-Ethyl-2,2-dimethylhexan
(Hexan = 6 C; 2,2-Dimethyl = zwei Methyl an C-2; 3-Ethyl an C-3; E vor M).Weiter im Kapitel Alkane
← 1.5 Homologe Reihe der Alkane → 1.6 Übungen zur Nomenklatur
🔁 Weiter in der Organik: Nomenklatur der Alkene (Kl. 10)
-
-
01.6 Übung zur Nomenklatur
Was du auf dieser Seite übst
Hier übst du die Genfer Nomenklatur an allen 9 Konstitutionsisomeren der Summenformel C7H16. Schau dir die Halbstrukturformel an, überlege den systematischen Namen – und klappe dann die Lösung auf.
Grundlagen – Genfer Nomenklatur
Die 7 Nomenklaturregeln hast du auf der vorherigen Seite kennengelernt: → 1.6 Genfer Nomenklatur der Alkane
1.6.3 Isomere der Summenformel C7H16
Entwickle zur Übung die Halbstrukturformeln der Isomeren der Summenformel C7H16 und benenne die Verbindungen mit ihrem systematischen Namen. Beachte: Es gibt 9 verschiedene Konstitutionsisomere.
Schau dir jede Halbstrukturformel an, überlege den Namen – und klappe dann die Lösung auf.
Isomer 1 von 9

Lösung anzeigen
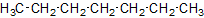
Name: n-Heptan
Isomer 2 von 9

Lösung anzeigen
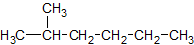
Name: 2-Methylhexan
Isomer 3 von 9

Lösung anzeigen
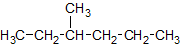
Name: 3-Methylhexan
Isomer 4 von 9

Lösung anzeigen
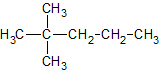
Name: 2,2-Dimethylpentan
Isomer 5 von 9

Lösung anzeigen
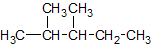
Name: 2,3-Dimethylpentan
Isomer 6 von 9

Lösung anzeigen
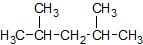
Name: 2,4-Dimethylpentan
Isomer 7 von 9

Lösung anzeigen
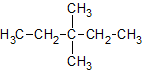
Name: 3,3-Dimethylpentan
Isomer 8 von 9

Lösung anzeigen
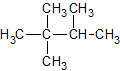
Name: 2,2,3-Trimethylbutan
Isomer 9 von 9

Lösung anzeigen
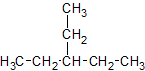
Name: 3-Ethylpentan
Lösung: Alle 9 Isomere im Überblick
1 unverzweigtes Isomer: n-Heptan
2 einfach verzweigte: 2-Methylhexan · 3-Methylhexan
5 zweifach verzweigte: 2,2- · 2,3- · 2,4- · 3,3-Dimethylpentan · 3-Ethylpentan
1 dreifach verzweigtes: 2,2,3-Trimethylbutan
Auf einen Blick – die wichtigsten Aussagen
KONSTITUTIONSISOMERE
Isomere haben die gleiche Summenformel, aber eine verschiedene Verknüpfung der Atome (→ verschiedene Strukturformeln).
ANZAHL
C7H16 hat 9 Konstitutionsisomere. Mit steigender Kettenlänge wächst die Isomerenzahl stark an.
SYSTEMATISCH VORGEHEN
Erst die längste Kette (unverzweigt), dann schrittweise kürzer mit mehr Verzweigungen – so findet man alle Isomere.
EIGENSCHAFTEN
Stärker verzweigte Isomere haben niedrigere Siedepunkte, weil die van-der-Waals-Kräfte bei kompakterer Gestalt schwächer sind.
Häufige Fragen – Isomere und Nomenklaturübungen
Was sind Konstitutionsisomere?
Konstitutionsisomere (auch Strukturisomere) sind Verbindungen mit gleicher Summenformel, aber verschiedener Verknüpfung der Atome. Sie sind vollständig verschiedene chemische Verbindungen mit eigenen Eigenschaften (Siedepunkt, Schmelzpunkt, Dichte). Alle 9 Isomere von C7H16 gehören zur Gruppe der Konstitutionsisomere.
Wie findet man systematisch alle Isomere einer Summenformel?
Man geht nach folgendem Schema vor: (1) Längste unverzweigte Kette (hier: n-Heptan, 7 C). (2) Hauptkette um 1 kürzen und eine Methylgruppe anbringen – dabei alle unterschiedlichen Positionen prüfen (→ 2-Methylhexan, 3-Methylhexan). (3) Hauptkette nochmals kürzen, zwei Seitenketten anbringen usw. Wichtig: Immer prüfen, ob ein neues Gebilde wirklich verschieden von bereits gefundenen ist.
Was unterscheidet 2-Methylhexan von 3-Methylhexan?
Beide haben eine 6 C-Atome lange Hauptkette (Hexan) und eine Methylgruppe als Seitenkette – aber an verschiedenen Positionen: Bei 2-Methylhexan sitzt die Methylgruppe an C-2, bei 3-Methylhexan an C-3. Gleiche Summenformel, verschiedene Struktur → verschiedene Eigenschaften.
Warum hat 2,2,3-Trimethylbutan einen niedrigeren Siedepunkt als n-Heptan?
Je stärker verzweigt ein Alkan ist, desto kugelförmiger (kompakter) ist das Molekül – die Oberfläche ist kleiner. Damit werden die van-der-Waals-Kräfte zwischen den Molekülen schwächer. Weniger Anziehungskräfte bedeuten: Das Molekül lässt sich leichter aus dem flüssigen Zustand herauslösen → niedrigerer Siedepunkt. Mehr dazu auf der nächsten Seite: → Eigenschaften der Alkane.
Wie viele Isomere hat C₅H₁₂?
C5H12 (Pentan) hat 3 Konstitutionsisomere: n-Pentan (5 C unverzweigt), 2-Methylbutan (4 C-Kette + 1 Methylgruppe an C-2) und 2,2-Dimethylpropan (3 C-Kette + 2 Methylgruppen an C-2, auch „Neopentan" genannt). Zum Vergleich: C4H10 hat 2 Isomere, C6H14 hat 5 Isomere.
Lernkarten – Isomere und Nomenklatur
Klicke auf eine Karte, um die Antwort zu sehen.
1Was sind Konstitutionsisomere? Nenne ein Kriterium.
Gleiche Summenformel, aber verschiedene Verknüpfung der Atome (→ verschiedene Strukturformel und verschiedene Eigenschaften).
2Wie viele Konstitutionsisomere hat C7H16?
9 Isomere: n-Heptan · 2- und 3-Methylhexan · 2,2- / 2,3- / 2,4- / 3,3-Dimethylpentan · 3-Ethylpentan · 2,2,3-Trimethylbutan.
3Wie viele Isomere hat C5H12? Nenne alle Namen.
3 Isomere: n-Pentan · 2-Methylbutan · 2,2-Dimethylpropan (Neopentan).
4Warum sinkt der Siedepunkt mit steigendem Verzweigungsgrad?
Stärkere Verzweigung → kompakteres Molekül → kleinere Oberfläche → schwächere van-der-Waals-Kräfte → niedrigerer Siedepunkt.
5Benenne: C-Kette mit 4 Atomen, je eine Methylgruppe an C-2 und C-3.
2,3-Dimethylbutan
(Butan = 4 C; zwei Methylgruppen an C-2 und C-3 → 2,3-Dimethyl; Summenformel: C6H14).Weiter im Kapitel Alkane
← 1.6 Genfer Nomenklatur → 1.7 Eigenschaften der Alkane
🔁 Weiter in der Organik: Isomerien der Alkene (Kl. 10)
-
02 Alkene
Was du in diesem Kapitel lernst
Alkene sind Kohlenwasserstoffe mit mindestens einer C=C-Doppelbindung – der charakteristischen funktionellen Gruppe dieser Verbindungsklasse. Am Beispiel des Ethens (C2H4) lernst du Aufbau, Eigenschaften und typische Reaktionen der Alkene kennen: von der Bromwasserprobe über die cis-trans-Isomerie bis zur katalytischen Hydrierung.
Grundlagen aus der 10. Klasse
Alkene bauen direkt auf dem Wissen über die gesättigten Kohlenwasserstoffe auf – wiederhole bei Bedarf: → 1. Alkane – Homologe Reihe, Genfer Nomenklatur, radikalische Substitution
Kapitelübersicht – 2. Alkene
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
H₂C=CH₂2.1
Ethen
Eigenschaften · Summenformel · Strukturformel · Vorkommen & Verwendung
Br₂2.1.5
Nachweis von Alkenen
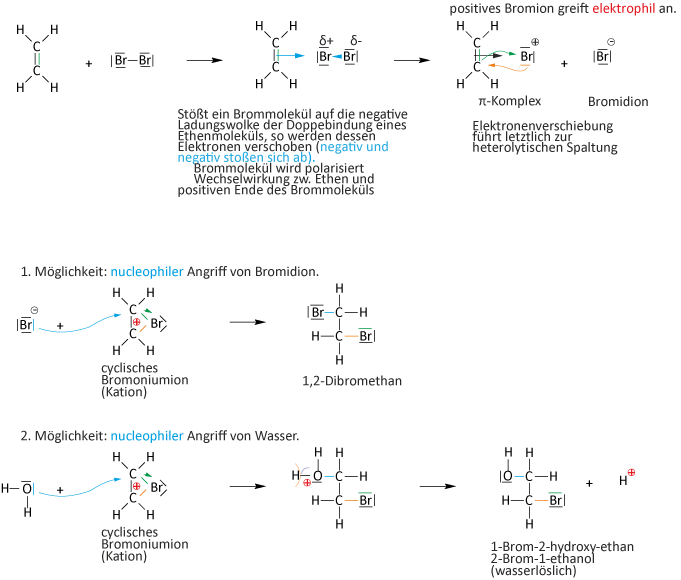
Bromwasserprobe · Elektrophile Addition · Reaktionsgleichung
cis
trans2.1.6 / 2.1.7
Isomerien von Alkenen
Konstitutions-Isomerie · cis-trans-Isomerie · (E/Z)-Nomenklatur
But-2-en2.2
Nomenklatur der Alkene
IUPAC-Benennung · Lokanten · Übungsaufgaben
+H₂/Ni2.3
Katalytische Hydrierung
Hydrierung ⇔ Eliminierung · Gleichgewicht · Katalysator Ni / Pt
sp²
sp³2.4
Vergleich Ethen – Ethan
Reaktivität · sp²- vs. sp³-Hybridisierung · π-Elektronensystem
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkene sind ungesättigte Kohlenwasserstoffe. Ihre charakteristische funktionelle Gruppe ist die C=C-Doppelbindung (σ- + π-Bindung). Allgemeine Formel: CnH2n.
Nachweis
Die Bromwasserprobe weist C=C-Doppelbindungen nach: Braunes Bromwasser wird durch Additionsreaktion entfärbt – eindeutiger Nachweis auf Mehrfachbindungen.
cis-trans-Isomerie
Die Doppelbindung blockiert die freie Rotation um die C=C-Achse. Dadurch entstehen räumlich verschiedene cis- und trans-Isomere mit unterschiedlichen Eigenschaften.
Reaktionstyp
Typisch für Alkene ist die elektrophile Addition: Die Doppelbindung wird geöffnet, Atome oder Gruppen lagern sich an (z. B. H2, Br2, HBr).
Häufige Fragen – Alkene
Was sind Alkene und wie unterscheiden sie sich von Alkanen?
Alkene sind Kohlenwasserstoffe mit mindestens einer C=C-Doppelbindung. Im Gegensatz zu den gesättigten Alkanen (nur Einfachbindungen) sind Alkene ungesättigt: Die Doppelbindung besteht aus einer σ-Bindung und einer π-Bindung. Die allgemeine Summenformel lautet CnH2n. Das einfachste Alken ist Ethen (C2H4). Alkene sind durch ihre Doppelbindung reaktiver als Alkane; ihr typischer Reaktionstyp ist die elektrophile Addition, nicht die radikalische Substitution der Alkane.
Wie weist man eine C=C-Doppelbindung nach?
Den klassischen Nachweis liefert die Bromwasserprobe: Braunes Bromwasser (Br2 in Wasser) wird durch Additionsreaktion entfärbt, weil das Brom an die Doppelbindung addiert wird. Gleichung am Beispiel Ethen: C2H4 + Br2 → C2H4Br2 (1,2-Dibromethan). Der Test ist eindeutig für alle Verbindungen mit Mehrfachbindungen. → 2.1.5 Nachweis von Alkenen
Was ist cis-trans-Isomerie, und wann tritt sie auf?
Die C=C-Doppelbindung blockiert die freie Drehbarkeit um die Bindungsachse. Wenn an beiden Doppelbindungskohlenstoffen je zwei verschiedene Substituenten sitzen, entstehen zwei räumlich unterschiedliche Isomere: Im cis-Isomer (= Z-Form: zusammen) stehen die gleichartigen Gruppen auf derselben Seite der Doppelbindung; im trans-Isomer (= E-Form: entgegen) auf gegenüberliegenden Seiten. Beispiel: cis-But-2-en und trans-But-2-en haben dieselbe Summenformel (C4H8), aber verschiedene Siedepunkte. → 2.1.6/2.1.7 Isomerien von Alkenen
Wie werden Alkene nach IUPAC benannt?
Die Nomenklatur der Alkene folgt denselben Grundregeln wie bei den Alkanen, mit Besonderheiten: (1) Die längste Kette, die die Doppelbindung enthält, ist die Hauptkette. (2) Sie wird so nummeriert, dass die Doppelbindung die niedrigstmögliche Lokante erhält. (3) Die Endung lautet „-en" (mehrere Doppelbindungen: -dien, -trien). (4) Die Position der Doppelbindung steht als Lokant vor der Endung: z. B. But-1-en, nicht 1-Buten (moderne IUPAC-Schreibweise). Bei cis-trans-Isomeren wird das Konfigurationspräfix vorangestellt: cis-But-2-en oder (Z)-But-2-en. → 2.2 Nomenklatur der Alkene
Was ist katalytische Hydrierung, und wie verhält sie sich zur Eliminierung?
Katalytische Hydrierung und Eliminierung sind Umkehrreaktionen: Bei der Hydrierung wird H2 mithilfe eines Nickel- oder Platin-Katalysators an die C=C-Doppelbindung addiert → Alken wird zu Alkan (z. B. C2H4 + H2 → C2H6). Bei der Eliminierung wird H2 unter hoher Temperatur abgespalten → Alkan wird zu Alken. Die Gesamtreaktion ist umkehrbar: Ethen ⇔ Ethan. Wichtig: Der Katalysator beeinflusst nur die Reaktionsgeschwindigkeit, verschiebt aber die Gleichgewichtslage nicht. → 2.3 Katalytische Hydrierung
Lernkarten – Alkene
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die funktionelle Gruppe der Alkene, und woraus besteht sie?
Die C=C-Doppelbindung. Sie besteht aus einer σ-Bindung (Überlappung entlang der Achse) und einer π-Bindung (seitliche Überlappung). Alkene sind deshalb ungesättigt und reaktiver als Alkane.
2Wie lautet die allgemeine Formel der Alkene? Nenne die ersten vier mit Formel.
CnH2n (n ≥ 2)
Ethen C2H4 · Propen C3H6
Buten C4H8 · Penten C5H103Wie funktioniert der Bromwassertest? Was beobachtet man?
Braunes Bromwasser wird mit dem Alken gemischt. Das Bromwasser entfärbt sich, weil Br2 durch elektrophile Addition an die C=C-Doppelbindung gebunden wird. → Nachweis auf Mehrfachbindung.
4Wann tritt cis-trans-Isomerie auf? Was unterscheidet cis von trans?
Wenn an beiden C-Atomen der C=C-Bindung je zwei verschiedene Substituenten sitzen. cis: gleichartige Gruppen auf einer Seite; trans: auf gegenüberliegenden Seiten. Freie Rotation um die Doppelbindung ist nicht möglich.
5Berechne: Wie viel g H2 werden benötigt, um 28 g Ethen vollständig zu hydrieren?
C2H4 + H2 → C2H6
M(C2H4) = 28 g/mol → n = 1 mol
Stöchiometrie 1:1 → n(H2) = 1 mol
m(H2) = 1 mol · 2 g/mol = 2 g H2
Weiter im Fach Chemie / 10. Klasse
← 1. Alkane → 3. Alkine ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Aromaten – Benzol und seine Derivate · Cycloalkane
-
02 Fischer-Projektion
2 Fischer-Projektion
Regeln und Reihenfolge:
- C-Gerüst senkrecht
- höchstes oxidiertes C-Atom oben (Oxidationszahl)
- beide C-C-Bindungen am mittleren C-Atom zeigen nach hinten (hinter die Papier-Ebene)
- beide horizontale Bindungen am mittleren, asymmetrischen C-Atom (H-C-; H-O-C-Bindung) zeigen nach vorne.
- Das Isomer, bei dem die Substituentengruppe mit dem elektronegativsten Atom in der Fischer-Projektion rechts steht, wird mit D[1] bezeichnet; steht der Substituent links, dann wird er mit L[2] bezeichnet.
Beispiel
a) Milchsäure: 2 Hydroxypropansäure
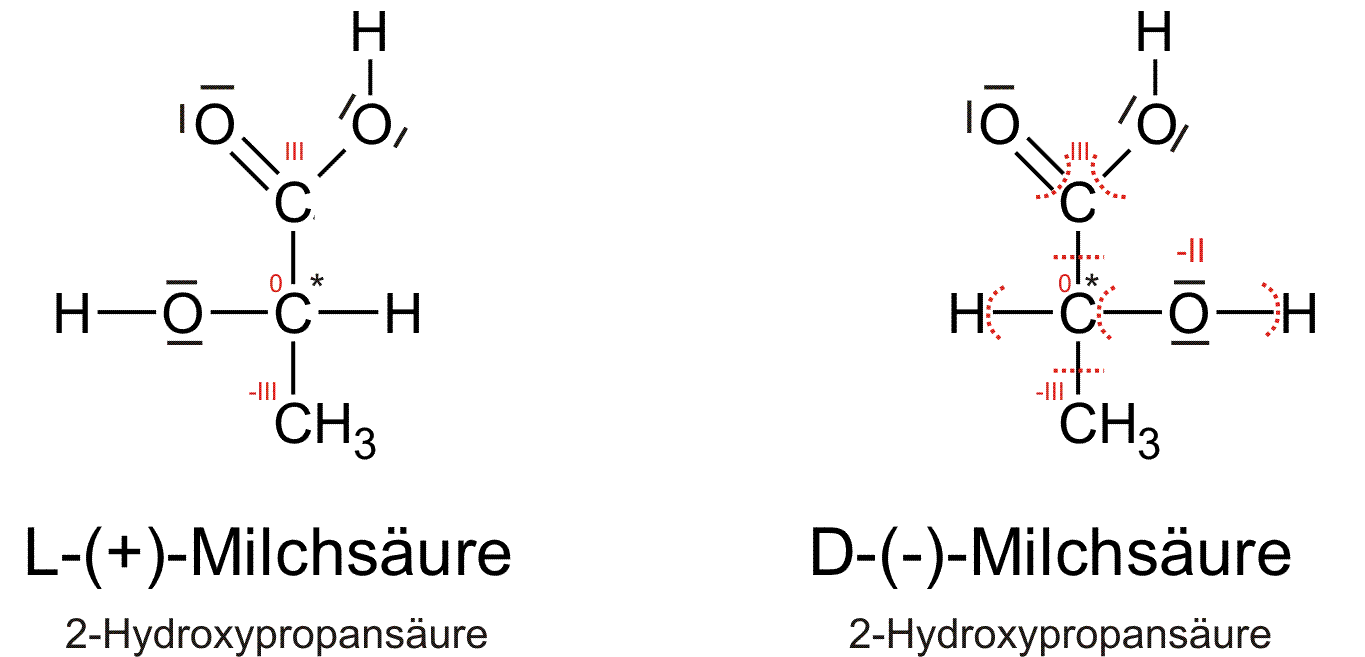
Im folgenden die D-Milchsäure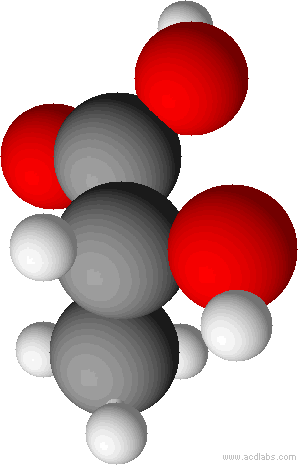
c) Weinsäure (2,3-Dihydroxybutan-1,4-Dicarbonsäure):
Wichtiger Hinweis: die zweite Weinsäure ist die D-(-)-Weinsäure. Der Name innerhalb der Abbildung ist falsch! Danke für die Korrektkur.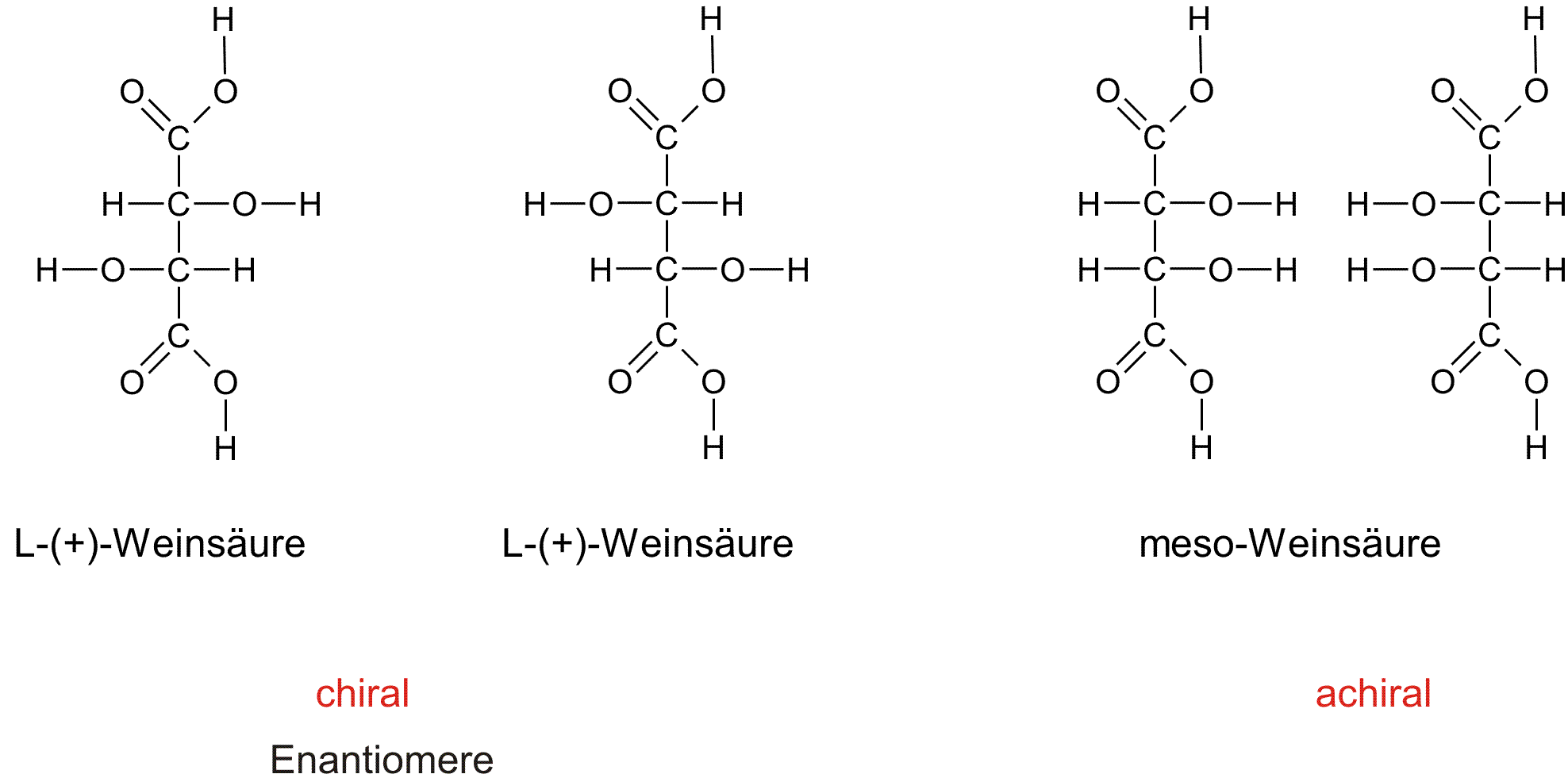
Hat eine Verbindung n asymmetrische C-Atome, so gibt es meist 2n Stereoisomere. Stereoisomere, die keine Enantiomere sind, heißen Diastereomere und haben verschiedene physikalische Eigenschaften.
Substanzen, deren Moleküle mit ihren Spiegelbildern übereinstimmen, obwohl sie Chiralitätszentranen besitzen, heißen meso-Verbindungen ("Das Spiegelbild des Originals kann durch Drehung wieder genau so aussehen, wie das Original). Sie besitzen eine Spiegelebene im Molekül.
-----------------[1] D = dexter (lat) = rechts
[2] L = laevus (lat) = links -
02.1.5 Nachweis von Alkenen (Mehrfachbindungen)
2.1.5 Nachweis von Alkenen (Doppelbindung)
Versuch: Ein Erlenmeyerkolben wird unter Wasser mit 250 ml Ethen gefüllt, anschließend werden 0,5 ml Brom dazugegeben und mit dem Stopfen verschlossen.
Alternativ: Hexen + Bromwasser (VORSICHT FALLS MAN BROM NIMMT ⇨ heftige Reaktion)
Beobachtung:
Die Bromfarbe verschwindet; Volumenabnahme; der Erlenmeyerkolben wird warm; es entsteht ein flüssiges Produkt, die Dichte ist größer als 1 g/cm³.Auswertung:
Zwei Hypothesen:I) Substitution:
II) Addition:
ErgebnisBei der Reaktion Ethen + Brom entsteht (fast) nur ein Reaktionsprodukt. „Bromwasserstoffnebel“ waren kaum zu sehen. Es fand somit eine Addition statt.
Additionsreaktionen: Reaktionen bei denen sich zwei Moleküle zu einem Molekül vereinigen! Es kommt dabei zur Anlagerung von Atomen oder Atomgruppen an Doppelbindungen (Mehrfachbindun-gen).
Reaktionsmechanismus: AE-Reaktionen (elektrophile Addition)
= typische Reaktion von Alkenen
-
03 Optische Aktivität und Polarimeter
3. Optische Aktivität und Polarimeter
Beim Durchgang von polarisiertem Licht durch die Lösung eines Enantiomeren erfährt die Polarisationsebene eine Drehung um einen bestimmten Betrag nach rechts oder links. Das andere Enantiomere dreht die Polarisationsebene des Lichtes um den gleichen Betrag in die entgegengesetzte Richtung.
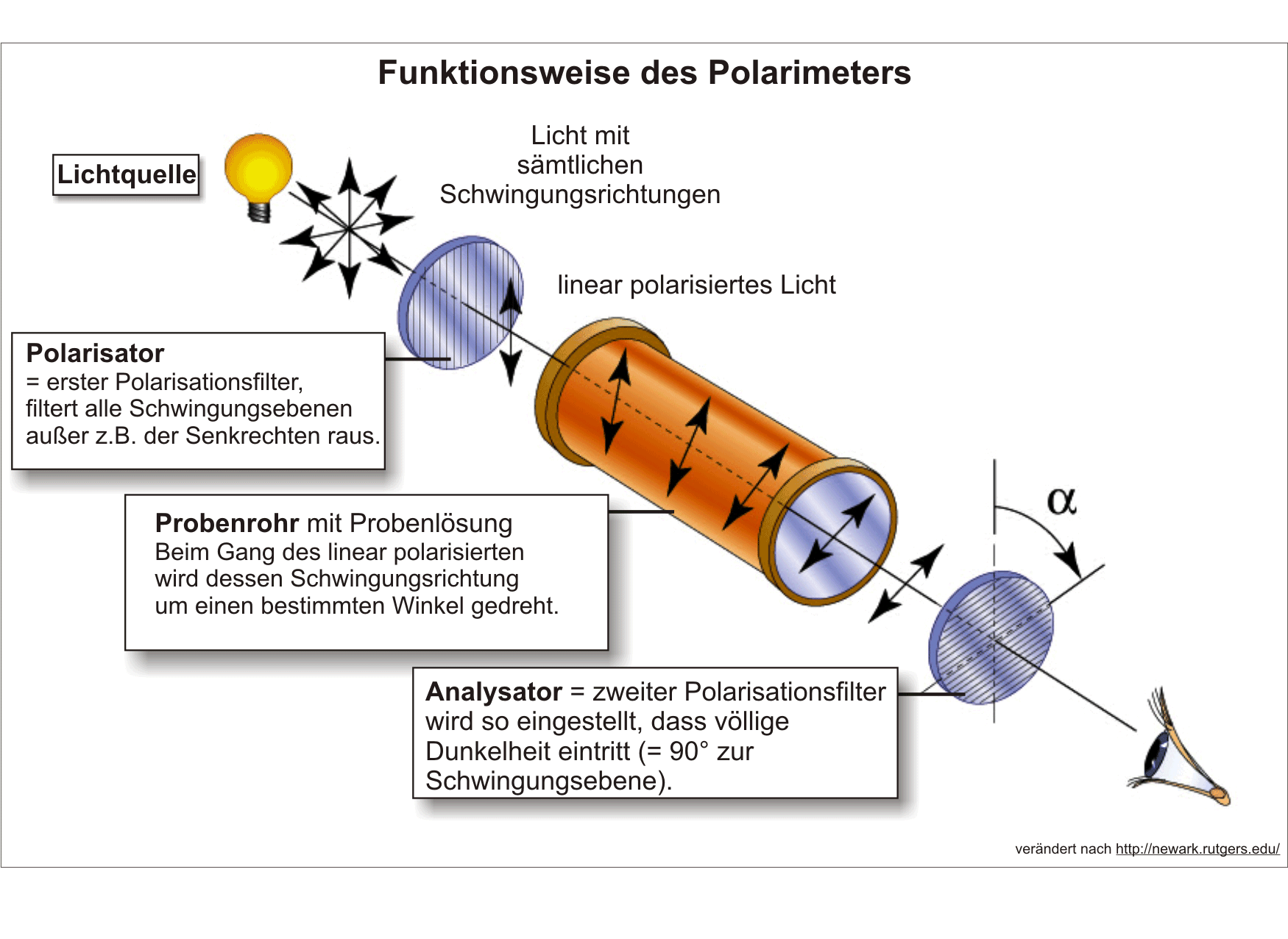
Der Drehwinkel α ist direkt proportional der:
- Massenkonzentration β
- Länge l des Probenrohrs
Der Proportionalitätsfaktor αsp hat einen für die optisch aktive Verbindung charakteristischen Wert. Er wird spezifische Drehung genannt. Sie wird bei 20 °C mit dem Licht einer Natrium-dampflampe bestimmt, das heißt mit Licht der Wellenlänge λ = 589,3 nm.
Schreibweise:
(+): rechtsdrehende Verbindungen
(-): linksdrehende Verbindung
Racemat (racemische Mischung, Raceform): äquimolares Gemisch der Enantiomere; dreht das polarisierte Licht nicht. -
04.1.3 Ringstruktur der Monosaccharide
4.1.3 Ringstruktur der Monosaccharide
Widersprüche:
- Schiffsche Reagenz (typ. Nachweis für Aldehyde) zeigt keine Farbreaktion.
- Drehwinkel in wässriger Lsg. 52,7° statt 112,2°.
- Tollens (1883) schloss daraus, dass Glucose nicht in der offenen Aldehydform vorliegt.
- Die Ursache hierfür ist in der intramolekularen Verknüpfung der Carbonylgruppe mit einer Hydroxylgruppe des gleichen Zuckermoleküls zu suchen. Es kommt also zu einer innermolekularen Halbacetalbildung.
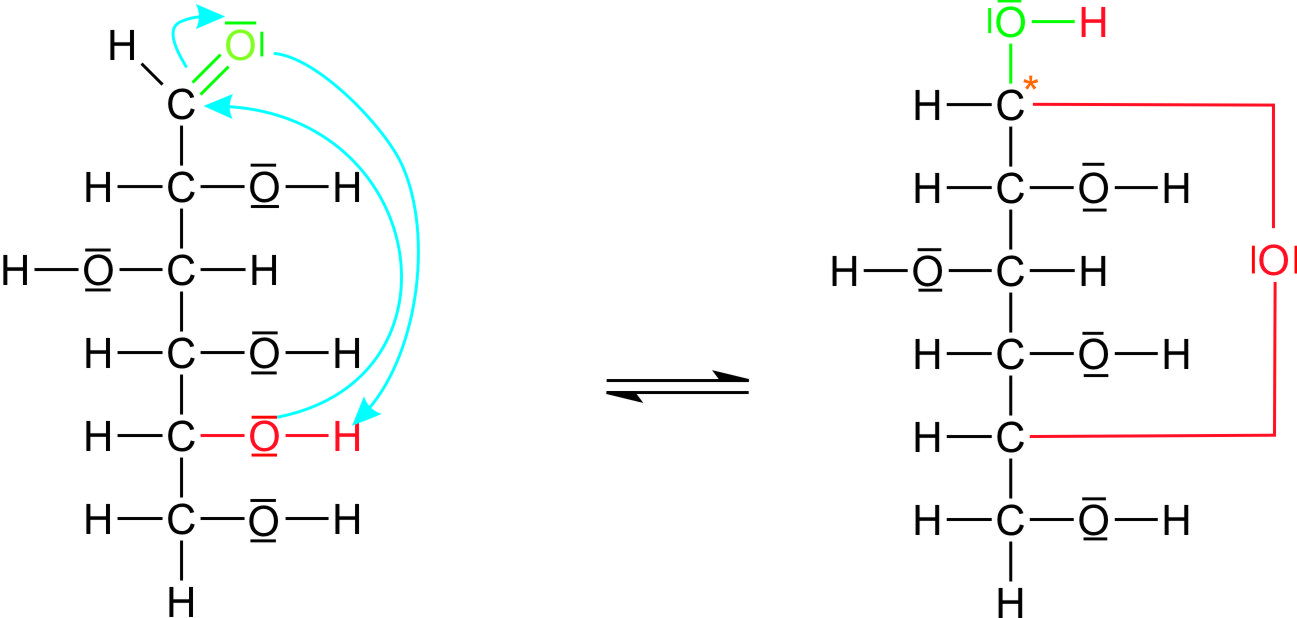
Haworth-Schreibweise- zyklisches Glucose Molekül wird als liegendes Sechseck [Pyranosen] oder Fünfeck [Furanosen] gezeichnet;
- Ringsauerstoffatom findet sich in der rechten hinteren Ecke [Pyranosen] bzw. im hinteren Eck [Furanosen];
- Substituenten, die in der FISCHERprojektion nach links weisen, stehen in der HAWORTH-Projektion oben ["Kommunistenregel"]
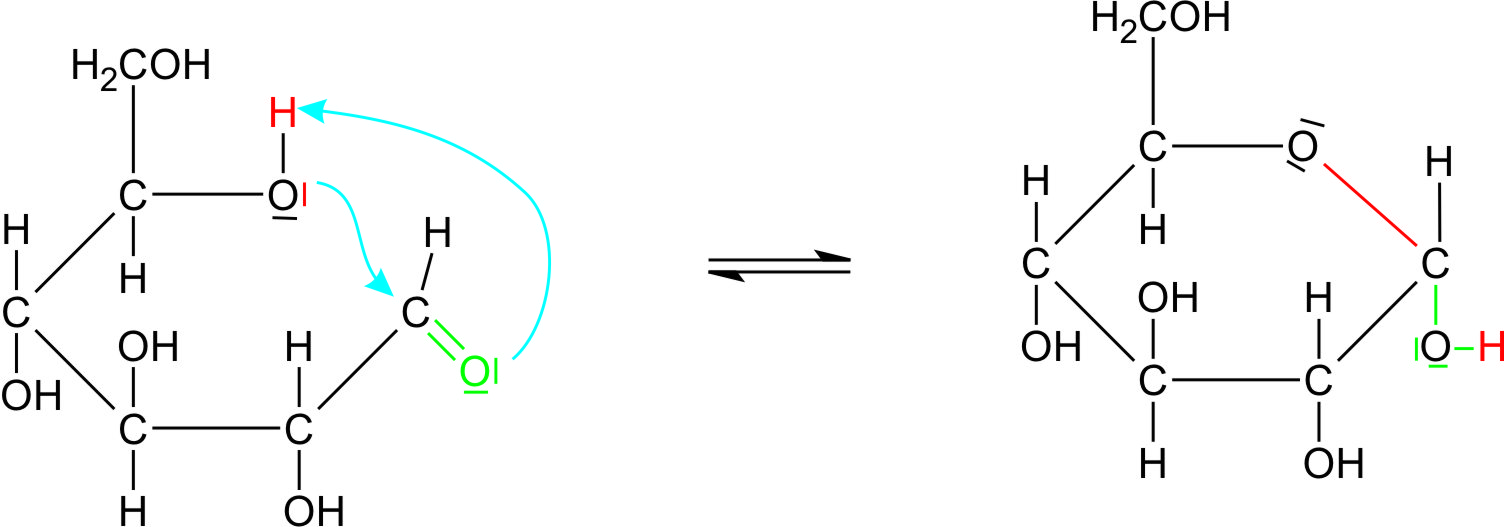
Erklärung der negativen Reaktion der Glucose mit der Schiffschen Reagenz: Es liegt ein Gleichgewicht zwischen der offenen Kette und dem Ring vor, wobei der Anteil der offenen Kette, bei der wirklich ein Aldehyd vorliegt verschwindend gering ist (< 1%):
Aldehydform (offenkettig) ⇌ Halbacetalform (Ring)- Fuchsinschweflige Säure (Schiffsches Reagenz) bildet mit dem Aldehyd eine reversible (umkehrbare) Reaktion, daher findet kein Entzug des Aldehyds statt. Das heißt, es gibt keine GG-Verschiebung und damit keinen wirklichen Aldehydnachweis (der Anteil an offener aldehydhaltigen Glucose ist zu gering).
- Bei der Fehling-Probe und der Tollens-Probe (Silberspiegel) findet eine GG-Verschiebung statt! Die offene Form wird laufend entzogen, neue Ringe gehen auf und es findet langsam der Aldehydnachweis statt.
Durch Ringbildung entstehen 2 Strukturisomere der D-(+)-Glucose (keine Spiegelbildisomere).
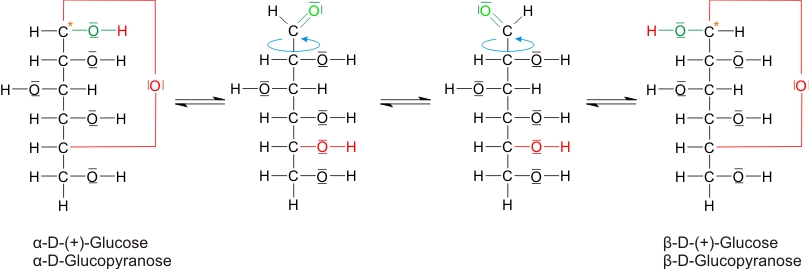
In wässriger Lösung liegen vor:36% 0,26% 64%
Drehwinkel: 112,2° 18,7°
Es entsteht ein neues asymmetrisches C-Atom (= anomeres Kohlenstoffatom) und damit 2 Diasteromere. Anomere = Isomere, die sich nur durch die Stellung der Hydroxylgruppen am anomeren Kohlenstoffatom unterscheiden.
α-Form: OH-Gruppe am neuen asymmetrischen C-Atom liegt auf derselben Seite wie die am untersten asymmetrischen C-Atom.
Muta1rotation: Drehwinkel einer Lösung einer optisch aktiven Substanz ändert sich vom Zeitpunkt des Ansetzens der Lösung kontinuierlich bis zum Erreichen eines festen Wertes. Grund dafür ist, dass man z.B. α-Glucose in eine wässrige Lösung gibt. Sobald sich das Molekül in Wasser löst, öffnen sich einige wenige Moleküle. Bei der erneuten Ringbildung, bildet sich auch β-Glucose. Erst wenn sich der Anteil wie oben angegeben einstellt, ändert sich der Drehwinkel nicht mehr.Glucose α-Form ⇌ offene Form ⇌ β-Form
Bei Glucose ist der Endwert: 0,36 * 112,2° + 0,64 * 18,7° = 52,36°
Haworth-Schreibweise
Achtet auf die Durchnummerierung der C-Atome. Am C1 war ursprünglich die Aldehydgruppe.
α-D-Glucose β-D-Glucose
Nachweis von Glucose: GOD-Test (Glucose-Oxidase-Stäbchen); Achtung beim schriftlichen Abitur: Fehling oder Tollens ist kein Nachweis für Glucose, sondern nur für Aldehydgruppen!- Glucose-Oxidase = Enzym: Oxidiert Glucose am C1-Atom zu Gluconsäure und Wasserstoffperoxid (H2O2).
- Durch das Enzym Peroxidase (z.B. aus Meerettich) wird das Wasserstoffperoxid zu Wasser reduziert.
- je mehr Glucose, umso intensiver die Farbe.
Im Handel als Teststreifen für Diabeteserkrankung.
-----
-
04.1.5 Fructose und Keto-Enol-Tautomerie
4.1.5 Fructose = Fruchtzucker
Vorkommen: in Früchten, Nektar, Honig; vor allem industriell hergestellte Fructose
Eigenschaften: kristallisiert schlecht aus wässriger Lösung → sirupartige Flüssigkeit.
Summenformel: C6H12O6
Fructose ist somit ein Strukturisomer der Glucose.
a) Seliwanow-Probe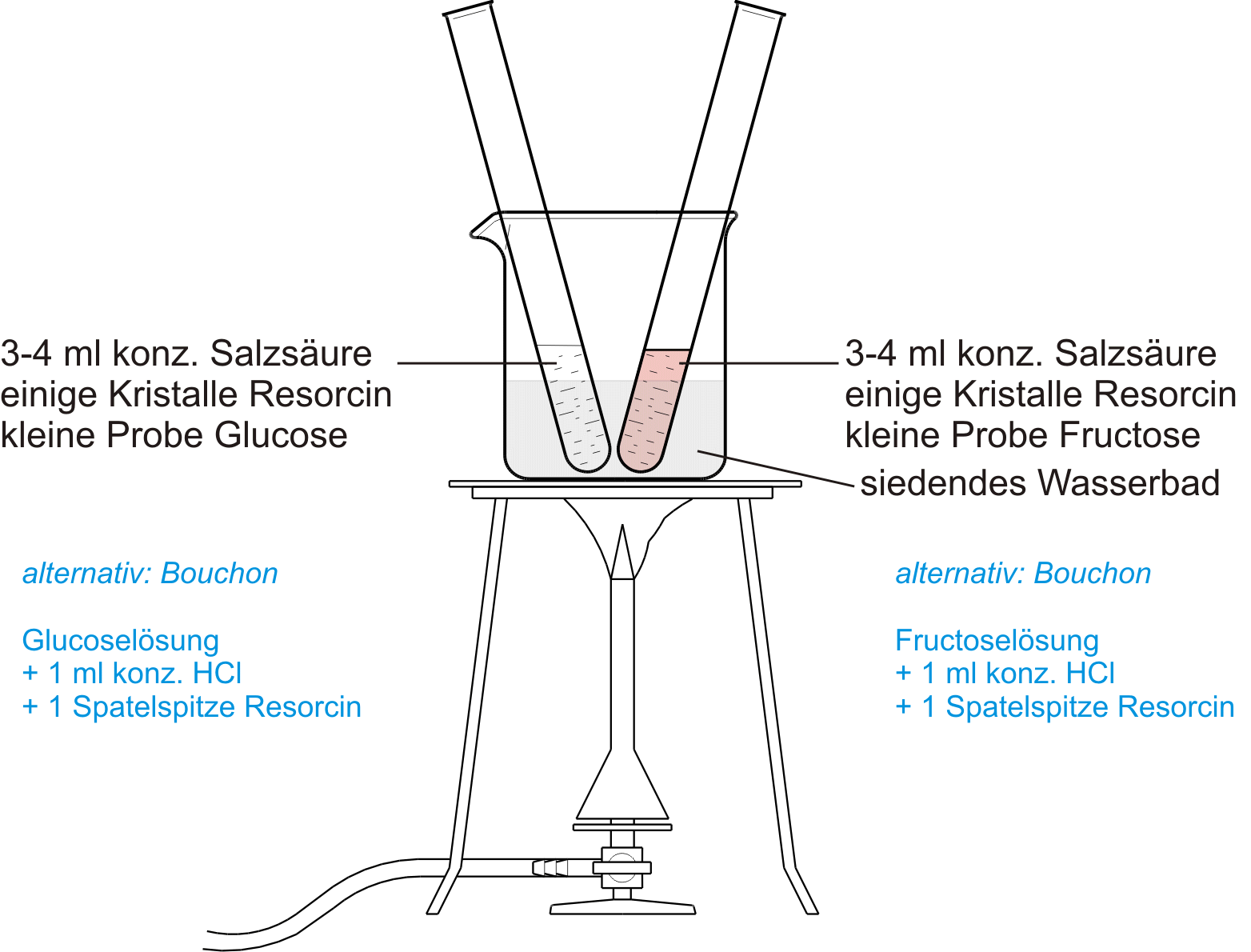
Nachweis, ob es sich bei Kohlenhydraten um Ketosen oder Aldosen handelt.
Ketose --> roter Farbstoff
Aldose --> keine/langsame Reaktion --> farblos
Info: Die Seliwanow-Reaktion ist ein Nachweis für Ketohexosen in der Furanose-Ringform. Da sie im sauren Milieu abläuft, kommt es nicht zur Keto-En(di)ol-Tautomerie. Mit Glucose fällt die Probe deshalb negativ aus.
Strukturformeln: Offenkettige und Ringbildung durch die Halbacetalbildung:
Fructose bildet wie Glucose Anomere. Neben der Kettenform des Moleküls enthält das Gleichgewicht zwei anomere Pyranosen ( β-D-Fructose und α-D-Fructose; Halbacetalbildung mit dem C5-Atom) und zwei anomere Furanosen ( β-D-Fructose und α-D-Fructose; Halbacetalbildung mit dem C6-Atom).
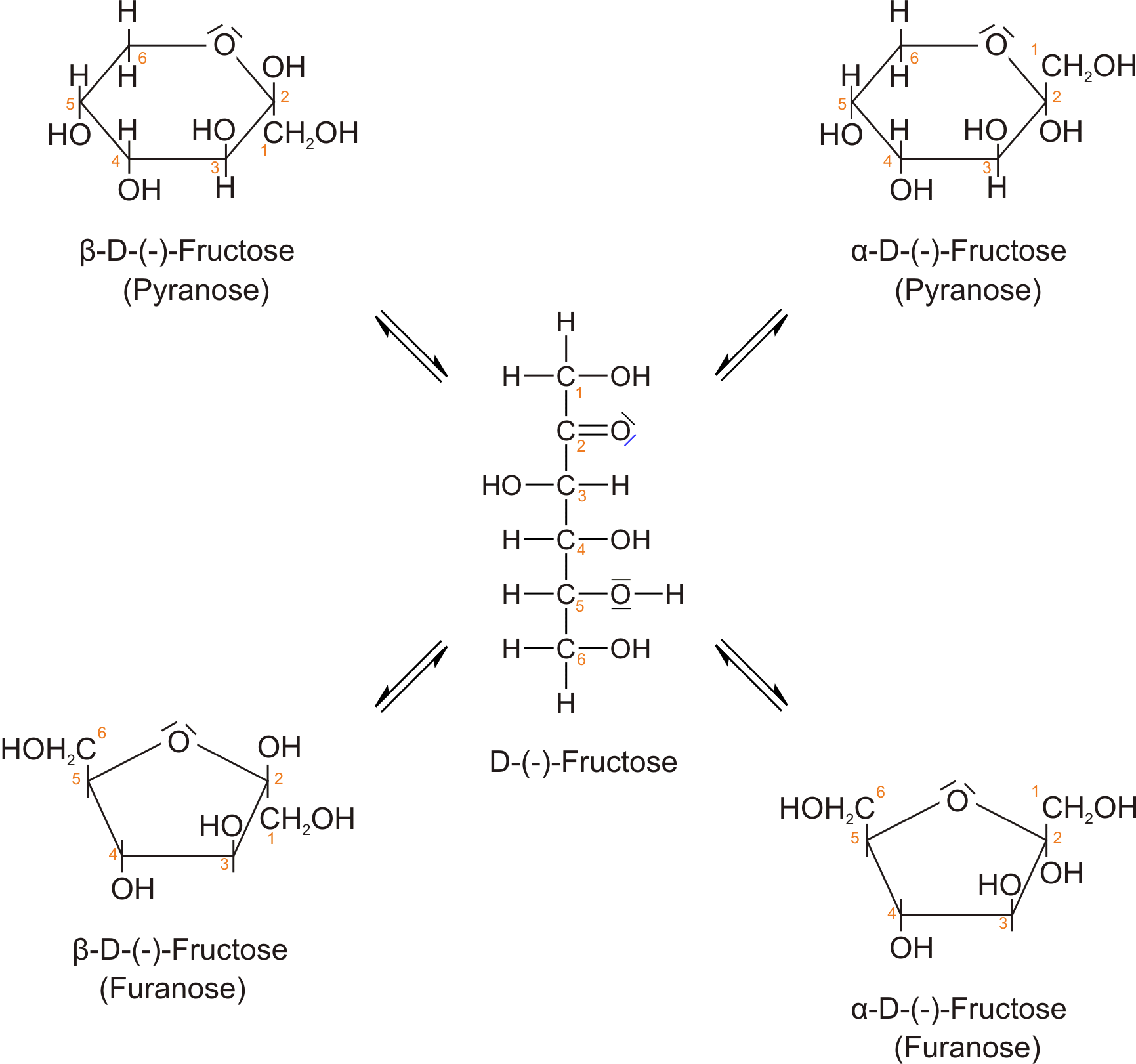
Keto-Enol -Tautomerie
Versuche mit Fructose:- Fehling → positiv
- Tollens → positiv
- GOD (Glucose-Nachweis) + Lauge → positiv
Funktioniert nicht mit einer Ketogruppe, da diese nicht weiter oxidiert werden kann. Grund, warum die Nachweise trotzdem positiv verlaufen: Innermolekulare Umlagerung unter Protonenwanderung und Elektronenverschiebung.

Genauer:
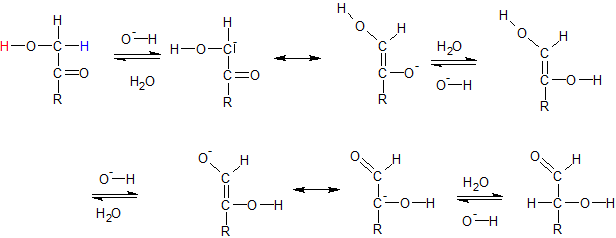
Glucose und Fructose stehen im Gleichgewicht (Glucose überwiegt); bei der Oxidation von Glucose wird Glucose aus dem GG entfernt → Fructose wird aufgebraucht.
-
2.1.6 Isomerien von Alkenen
2.1.6 Isomerien bei Ethenderivaten
Von Dichlorethen gibt es drei isomere Verbindungen:
2.1.7 cis-trans-Isomerie (bzw. E/Z-Isomerie
Die Doppelbindung blockiert die Drehbarkeit um die C-C-Bindungsachse. Die cis-trans-isomeren Verbindungen unterscheiden sich in ihrem physikalischen (und chemischen) Verhalten.

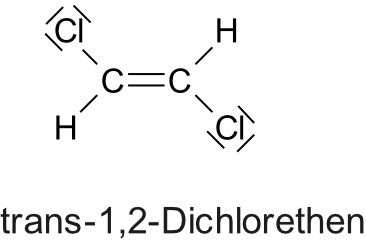
Dipol
- stärkere zwischenmolekulare Wechselwirkungenhöhere
- Siedetemperatur: 60,3 °C
kein Dipol (symmetrisch)
- schwächere zwischenmolekulare wechselwirkungenniedrigere
- Siedetemperatur: 47,7 °C
a) trans (lat) = hinüberschreiten, jenseits heute als (E)-IsomerieDie wichtigen Substituenten (Alkylgruppen, Halogen-Atome, Hydroxylgruppe,...) liegen auf der gegenüberliegenden Seite der Doppelbindung.
Heutzutage bezeichnet man es auch als (E)-Isomere, wobei (E) für entgegen gemerkt werden kann.Beispiel: trans-But-2-en (= trans-2-Buten) = (E)-But-2-en.
c) cis (lat) = diesseits heute auch als (Z)-Isomere
Die wichtigen Substituenten liegen auf der gleichen Seite der Doppelbindung.
Heute auch als (Z)-Isomere von zusammen.Beispiel: cis-But-2-en (=cis-2-Buten) = (Z)-But-2-en
Eselbrücke: cis: Ein cis-Molekül hat die Form wie ein "C" von "cis".